Содержание
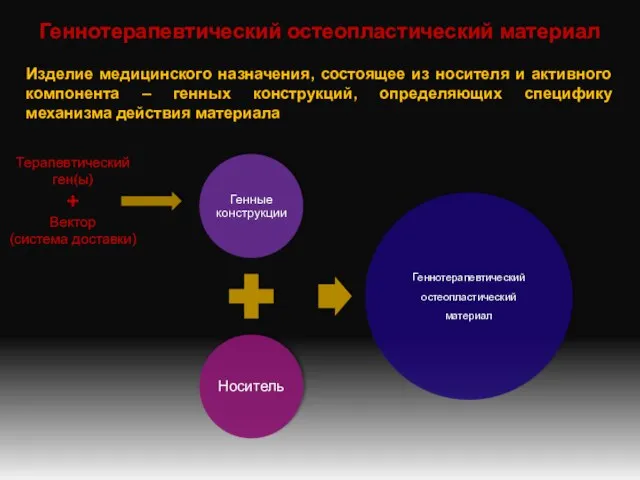
- 2. Геннотерапевтический остеопластический материал Изделие медицинского назначения, состоящее из носителя и активного компонента – генных конструкций, определяющих
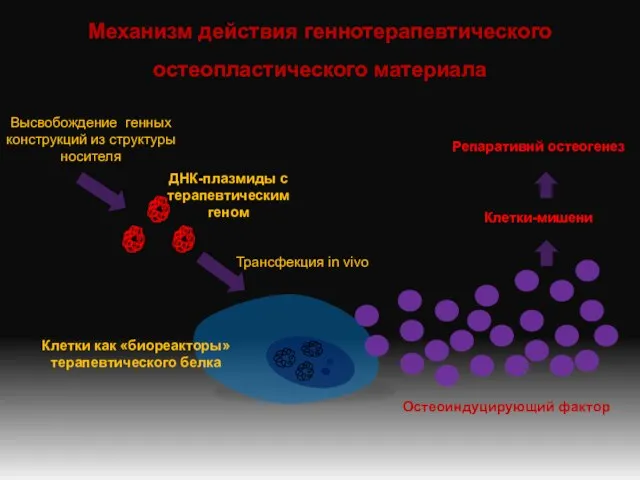
- 3. Механизм действия геннотерапевтического остеопластического материала Трансфекция in vivo ДНК-плазмиды с терапевтическим геном Клетки как «биореакторы» терапевтического
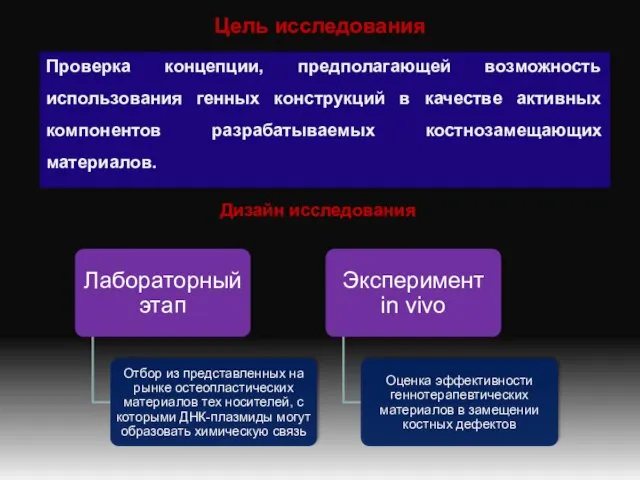
- 4. Цель исследования Проверка концепции, предполагающей возможность использования генных конструкций в качестве активных компонентов разрабатываемых костнозамещающих материалов.
- 5. Материалы и методы 1. Генные конструкции на основе субстанции «Камбиогенплазмид», представляющую собой сверхскрученную плазмидную ДНК с
- 6. Результаты лабораторного этапа Концентрация рVEGF165, образовавших химическую связь с носителем: 1. Синтетический β-трикальцийфосфат российского производства –
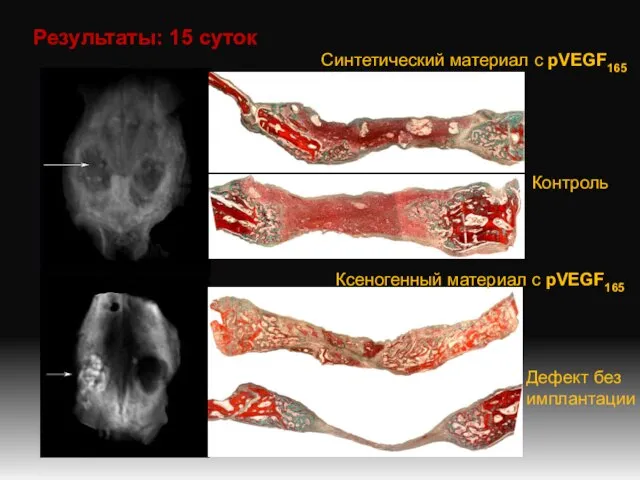
- 7. Результаты: 15 суток Синтетический материал с рVEGF165 Контроль Ксеногенный материал с рVEGF165 Дефект без имплантации
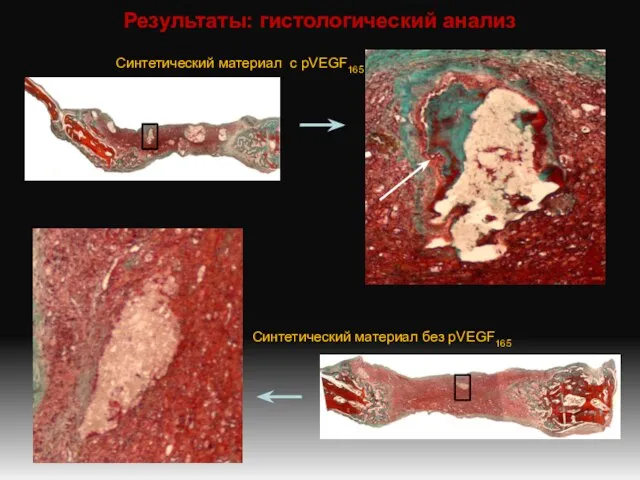
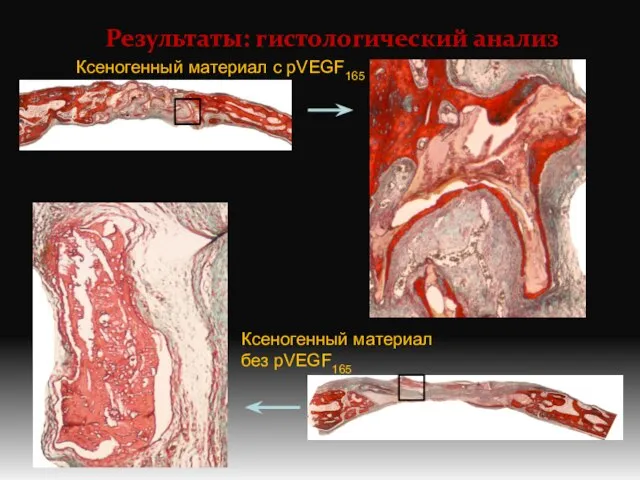
- 8. Результаты: гистологический анализ Синтетический материал с pVEGF165 Синтетический материал без pVEGF165
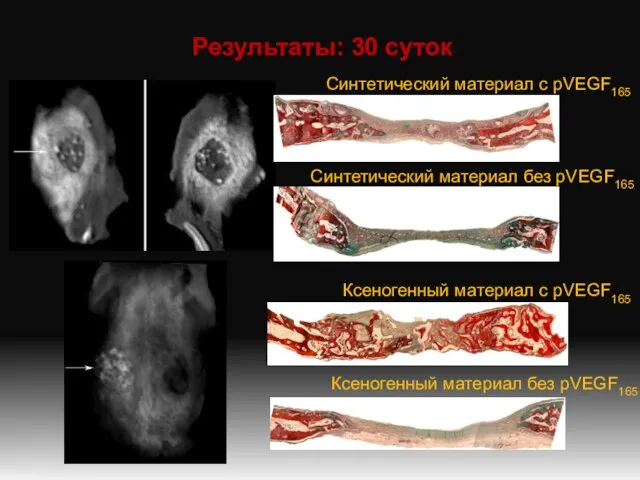
- 9. Результаты: 30 суток Синтетический материал с pVEGF165 Синтетический материал без pVEGF165 Ксеногенный материал с pVEGF165 Ксеногенный
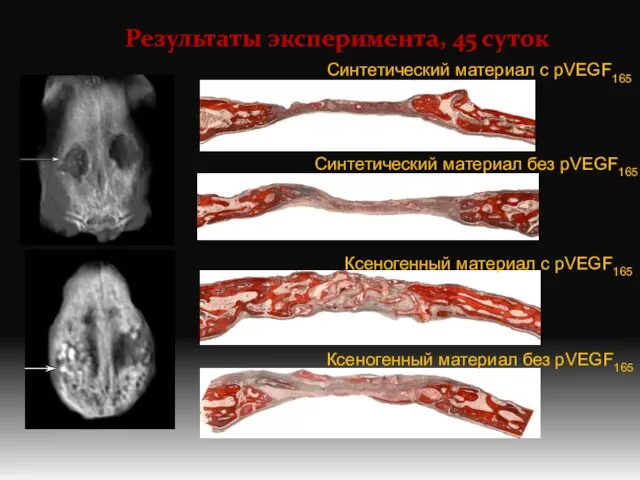
- 10. Результаты эксперимента, 45 суток Синтетический материал с pVEGF165 Синтетический материал без pVEGF165 Ксеногенный материал с pVEGF165
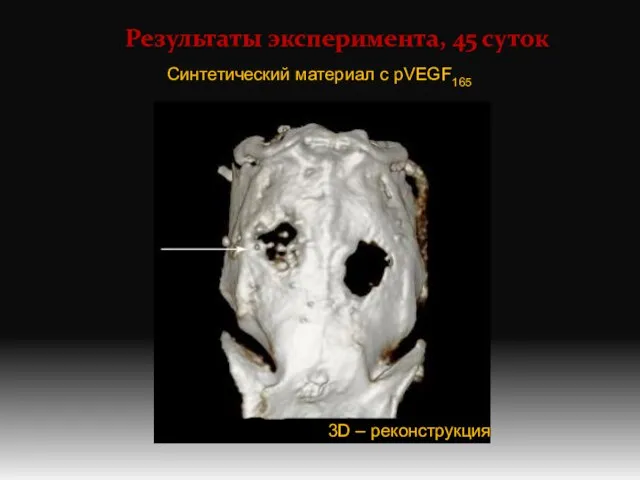
- 11. Результаты эксперимента, 45 суток Синтетический материал с pVEGF165 3D – реконструкция
- 12. Результаты: гистологический анализ Ксеногенный материал с pVEGF165 Ксеногенный материал без pVEGF165
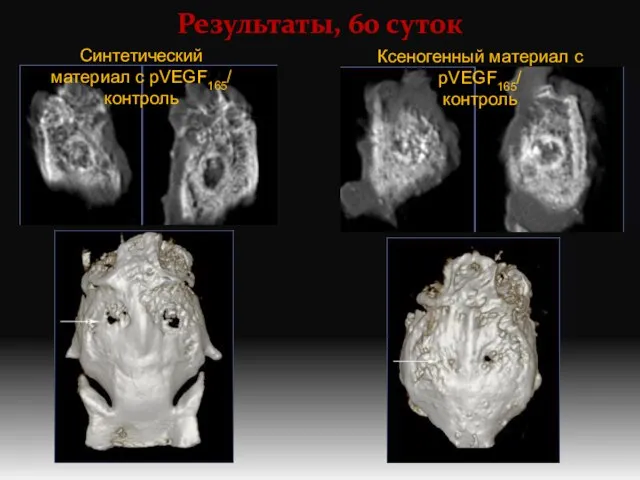
- 13. Результаты, 60 суток Синтетический материал с pVEGF165/ контроль Ксеногенный материал с pVEGF165/ контроль
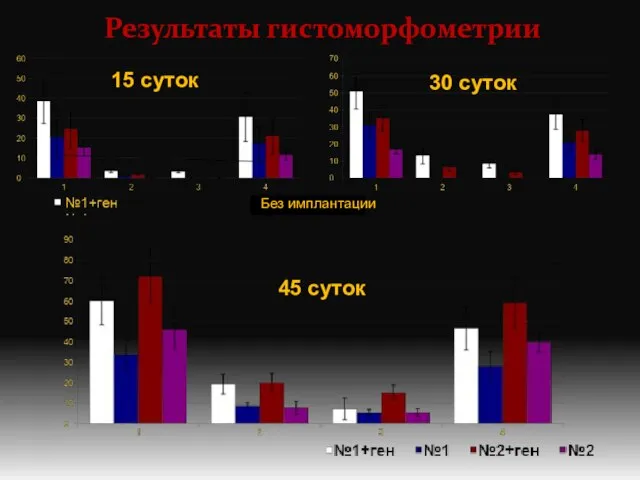
- 14. Результаты гистоморфометрии 15 суток 30 суток 45 суток Без имплантации
- 15. Выводы: Гипотеза о том, что генные конструкции в качестве активного компонента костнозамещающего материала способны усилить остеоиндуцирующий
- 17. Скачать презентацию


 От математики к красоте и гармонии
От математики к красоте и гармонии Презентация на тему Роман Герой нашего времени Лермантов
Презентация на тему Роман Герой нашего времени Лермантов Презентация по практике
Презентация по практике Создание единой образовательной среды
Создание единой образовательной среды Маркетинг: ценность лизинга устами клиентов
Маркетинг: ценность лизинга устами клиентов Компьютерное математическое моделирование
Компьютерное математическое моделирование Проект «Методика подготовки учащихся к изучению нового материала по теме: «Системы однородных уравнений»
Проект «Методика подготовки учащихся к изучению нового материала по теме: «Системы однородных уравнений» Закуски из рыбы
Закуски из рыбы Роль компьютера в жизни человека
Роль компьютера в жизни человека Организация дополнительного образования детей с ОВЗ технической направленности (проектная деятельность)
Организация дополнительного образования детей с ОВЗ технической направленности (проектная деятельность) Нам не страшен страшный страх
Нам не страшен страшный страх Значение животных в природе и в жизни человека
Значение животных в природе и в жизни человека Правонарушение и юридическая ответственность
Правонарушение и юридическая ответственность НОВЫЕ ИНФОРМАЦИОННЫЕ ТЕХНОЛОГИИ В ДЕЯТЕЛЬНОСТИ РОССИЙСКОЙ АССОЦИАЦИИЭЛЕКТРОННЫХ БИБЛИОТЕКwww.aselibrary.ru
НОВЫЕ ИНФОРМАЦИОННЫЕ ТЕХНОЛОГИИ В ДЕЯТЕЛЬНОСТИ РОССИЙСКОЙ АССОЦИАЦИИЭЛЕКТРОННЫХ БИБЛИОТЕКwww.aselibrary.ru Посвящение 65-й годовщине со дня Победы в Великой Отечественной войне 1941-1945 гг.
Посвящение 65-й годовщине со дня Победы в Великой Отечественной войне 1941-1945 гг. Законы урожая
Законы урожая Предпрофильная подготовка
Предпрофильная подготовка Грамматическое значение причастия
Грамматическое значение причастия Кровяное давление
Кровяное давление Изготовление композиций из белой бумаги
Изготовление композиций из белой бумаги Майнкрафт
Майнкрафт Социальная среда бизнеса и предпринимательства
Социальная среда бизнеса и предпринимательства Божественная Аврора и роковая Кармен – все была великолепная Майя Плисецкая
Божественная Аврора и роковая Кармен – все была великолепная Майя Плисецкая Этнические общности
Этнические общности Учет и хранение фондов музея образовательной организации
Учет и хранение фондов музея образовательной организации Год науки и технологий
Год науки и технологий СР-1 (Корейские шампуни)
СР-1 (Корейские шампуни) Реформы Александра II
Реформы Александра II