Слайд 2Среду водородного раствора можно охарактеризовать концентрацией ионов водорода Н+ или гидроксид-ионов ОН+
Существует

три типа среды:
Нейтральная
Кислотная
Щелочная
Слайд 3Нейтральная-
Это среда, в которой концентрация ионов водорода равна концентрации гидроксид-ионов:
[H+]=[OH-]=10-7 моль/л
![Нейтральная- Это среда, в которой концентрация ионов водорода равна концентрации гидроксид-ионов: [H+]=[OH-]=10-7 моль/л](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/380036/slide-2.jpg)
Слайд 4Кислотная-
Это среда, в которой концентрация ионов водорода больше концентрации гидроксид-ионов:
[H+]>[OH-], [H+]>10-7 моль/л
![Кислотная- Это среда, в которой концентрация ионов водорода больше концентрации гидроксид-ионов: [H+]>[OH-], [H+]>10-7 моль/л](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/380036/slide-3.jpg)
Слайд 5Щелочная-
Это среда, в которой концентрация ионов водорода меньше концентрации гидроксид-ионов:
[H+]<[OH-], [H+]< 10-7моль/л
![Щелочная- Это среда, в которой концентрация ионов водорода меньше концентрации гидроксид-ионов: [H+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/380036/slide-4.jpg)
Слайд 6Для характеристики сред растворов удобно использовать так называемый водородный показатель рн (пэ-аш),

введённый датским химиком Сёренсеном: р-начальная буква слова potenz- математическая степень, Н- химический знак водорода.
Водородным показателем РН называется отрицательный десятичный логарифм концентрации ионов водорода.
РН=-lg[H+]
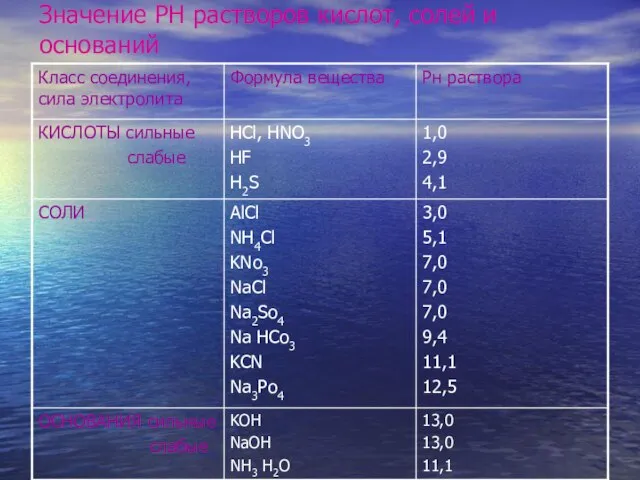
Слайд 7Значение РН растворов кислот, солей и оснований
Слайд 8Значение рн некоторых физиологических жидкостей


![Нейтральная- Это среда, в которой концентрация ионов водорода равна концентрации гидроксид-ионов: [H+]=[OH-]=10-7 моль/л](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/380036/slide-2.jpg)
![Кислотная- Это среда, в которой концентрация ионов водорода больше концентрации гидроксид-ионов: [H+]>[OH-], [H+]>10-7 моль/л](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/380036/slide-3.jpg)
![Щелочная- Это среда, в которой концентрация ионов водорода меньше концентрации гидроксид-ионов: [H+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/380036/slide-4.jpg)



 Особенности сжатого изложения
Особенности сжатого изложения Богатыри земли русской
Богатыри земли русской ПАРНОЕ ПРОГРАММИРОВАНИЕ
ПАРНОЕ ПРОГРАММИРОВАНИЕ Труд и собственность
Труд и собственность Программа развития системы дошкольного образования города Перми на 2019-2021 годы
Программа развития системы дошкольного образования города Перми на 2019-2021 годы Собственная презентация с триггерами
Собственная презентация с триггерами Общие способы получения металлов
Общие способы получения металлов Древнерусское государство, деятельность первых русских князей
Древнерусское государство, деятельность первых русских князей Ранний возраст 1 - 3 года
Ранний возраст 1 - 3 года Вопросы внедрения оценки жизненного цикла здания в строительстве. Как это скажется на развитии деревянного домостроения?
Вопросы внедрения оценки жизненного цикла здания в строительстве. Как это скажется на развитии деревянного домостроения? Книжная печатная графика
Книжная печатная графика Презентация на тему Человек в системе экономических отношений
Презентация на тему Человек в системе экономических отношений Бизнес-план по развитию крестьянского (фермерского) хозяйства начинающего фермера
Бизнес-план по развитию крестьянского (фермерского) хозяйства начинающего фермера In der Mensa
In der Mensa Соборы Московского Кремля
Соборы Московского Кремля Квартира по карте
Квартира по карте Варианты расчета бонуса за два месяца
Варианты расчета бонуса за два месяца Материальный баланс. Полусухой способ
Материальный баланс. Полусухой способ Дети и телевизорТем, кого боги хотят уничтожить, они сначала дают телевизорАртур Кларк
Дети и телевизорТем, кого боги хотят уничтожить, они сначала дают телевизорАртур Кларк Человек и природа в славянской мифологии
Человек и природа в славянской мифологии Слава России сквозь призму веков. Конституция и государственная символика Российской Федераци
Слава России сквозь призму веков. Конституция и государственная символика Российской Федераци Основные принципЫ устройства
Основные принципЫ устройства Интеллектуальная собственность
Интеллектуальная собственность «Административная реформа в Липецкой области. Создание многофункциональных центров предоставления государственных и муниципаль
«Административная реформа в Липецкой области. Создание многофункциональных центров предоставления государственных и муниципаль Рудименты демонтированы
Рудименты демонтированы Гражданское право. Юридические лица: понятие, признаки и виды
Гражданское право. Юридические лица: понятие, признаки и виды Пользование мобильным телефоном в общественных местах
Пользование мобильным телефоном в общественных местах Сущность, стадии и методы проектирования вертикальной планировки
Сущность, стадии и методы проектирования вертикальной планировки