Содержание
- 2. Документы, определяющие нормативно-правовую базу экзаменационной работы 1) Обязательный минимум содержания основного общего образования по химии (Приказ
- 3. На выполнение работы отводится 2 часа (120 минут) 2. Работа состоит из 3 частей, включающих 25
- 4. При выполнении работы можно пользоваться: Периодической системой химических элементов Д.И. Менделеева таблицей растворимости солей, кислот и
- 5. Рекомендации по распределению времени Часть 1: на выполнение одного задания – 2–3 минуты (итого 38-57 мин)
- 6. Система оценивания Часть 1 (max 19 баллов) 1 балл - при условии, если указан только один
- 7. Часть 3 (max 7 баллов) Каждый элемент задания оценивается 1 баллом Задание С1 - 4 балла,
- 8. Рекомендации по пересчету баллов за выполнение экзаменационной работы в отметки по пятибалльной шкале Полученные учащимся баллы
- 9. Условия проведения и проверки экзамена На экзамене в аудиторию не допускаются специалисты по химии Использование инструкции
- 10. Изменения в содержании экзаменационной работы 2010 года (по сравнению с 2009 годом) Часть 2 (задание В3)
- 11. Задание В3 2009 Выберите уравнения реакций, в которых углерод является окислителем. 1) C + 4Na =
- 12. Задание С1 2009 Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: CuCl2 → X
- 14. Скачать презентацию











 Авто - путешественники
Авто - путешественники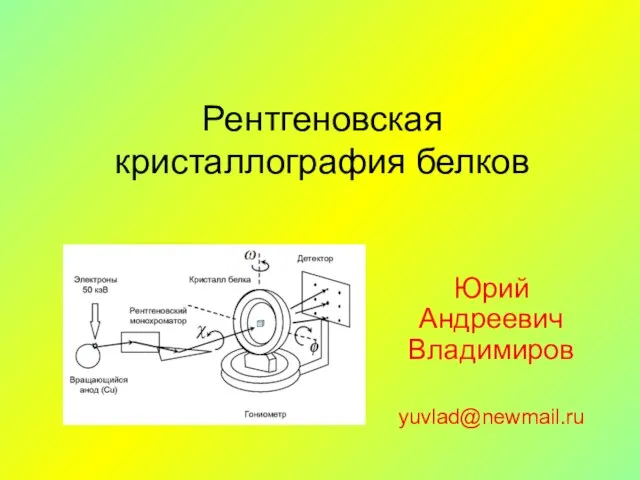 Рентгеновская кристаллография белков
Рентгеновская кристаллография белков Сөз таптары
Сөз таптары МОНИТОРИНГ ВОСПИТАТЕЛЬНОЙ ДЕЯТЕЛЬНОСТИ
МОНИТОРИНГ ВОСПИТАТЕЛЬНОЙ ДЕЯТЕЛЬНОСТИ Ответственность физических и юридических лиц в международном праве
Ответственность физических и юридических лиц в международном праве Развивающая эстетика – новый предмет в школьном образовании
Развивающая эстетика – новый предмет в школьном образовании Жизнь и творчество Л.Н. Толстого ( 1828-1910)
Жизнь и творчество Л.Н. Толстого ( 1828-1910) Презентация на тему Рождество Пресвятой Богородицы
Презентация на тему Рождество Пресвятой Богородицы  Урок здоровья
Урок здоровья Презентация _Межличностные отношения_ с заданиями практикума, обществознание, 6 класс (2)
Презентация _Межличностные отношения_ с заданиями практикума, обществознание, 6 класс (2) Курсовая работа Сказкотерапия как одно из средств формирования межличностных отношений в детском коллективе
Курсовая работа Сказкотерапия как одно из средств формирования межличностных отношений в детском коллективе Разделительные знаки Ъ и Ь
Разделительные знаки Ъ и Ь Презентация на тему Особенности средневековой моды
Презентация на тему Особенности средневековой моды Рынок труда в фармацевтике. Реалии посткризисного периода
Рынок труда в фармацевтике. Реалии посткризисного периода СА-ФИ-ДАНСЕ
СА-ФИ-ДАНСЕ Технология разработки профессиональных стандартов
Технология разработки профессиональных стандартов Моя семья. Фотоальбом
Моя семья. Фотоальбом Кишечная непроходимость
Кишечная непроходимость  Дистанционная торговля
Дистанционная торговля Этиловый спирт и его влияние на здоровье человека
Этиловый спирт и его влияние на здоровье человека Готовимся к экзаменам. Выявление способностей
Готовимся к экзаменам. Выявление способностей Правила поведения для детей
Правила поведения для детей Рекламные возможности сети «ВИКТОРИЯ» г. Москва На I-II кварталы 2011
Рекламные возможности сети «ВИКТОРИЯ» г. Москва На I-II кварталы 2011 Покорители Вершин
Покорители Вершин Дождь
Дождь Позициониране на Схемата за екомаркировка в държавната политика за устойчив туризъм ДЪРЖАВНА АГЕНЦИЯ ПО ТУРИЗЪМ Десислава Михалкова – Станимирова Гл. експерт в дирекция “Туристическа политика” 20 октомври, 2008 г, гр. София
Позициониране на Схемата за екомаркировка в държавната политика за устойчив туризъм ДЪРЖАВНА АГЕНЦИЯ ПО ТУРИЗЪМ Десислава Михалкова – Станимирова Гл. експерт в дирекция “Туристическа политика” 20 октомври, 2008 г, гр. София Specialaus apgyvendinimo paslaugos
Specialaus apgyvendinimo paslaugos Группа истерических психопатов
Группа истерических психопатов