Содержание
- 2. Литература Рачевский Б.С., «Сжиженные углеводородные газы» – М., Нефть и газ, 2009. Стаскевич Н. Л., Вигдоричик
- 3. Природный газ Природный газ (Natural gas, natural fuel gas) ГОСТ 5542-2014 «Газы горючие природные промышленного и
- 4. Сжиженные газы СУГ - сжиженные углеводородные газы, LPG ( Liquefied petroleum gas) ГОСТ Р 52087-2018 «Газы
- 5. Определение СУГ Это углеводороды или их смеси, которые при нормальном давлении и температуре окружающего воздуха находятся
- 6. Определение СПГ Криогенная жидкость представляющая собой многокомпонентную смесь, которая состоит в основном из метана, а также
- 7. Определение КПГ Природный топливный компримированный газ получают из горючего природного газа, транспортируемого по магистральным газопроводам или
- 8. Способы хранения СУГ
- 9. Способы хранения СПГ
- 10. Способы хранения КПГ
- 11. Свойства ПГ, КПГ, СПГ
- 12. Свойства СУГ, СПГ
- 13. Законы, применяемые для сжиженных газов
- 14. Закон Бойля-Мариотта (a1662, ф1676) Объем газа при постоянной температуре обратно пропорционален давлению PV=const . T=const
- 15. Закон Гей-Люссака (ф1802) Объем постоянной массы газа пропорционален абсолютной температуры при постоянном давлении. . . P=const
- 16. Закон Авогадро (и1811) В равных объемах различных газов при одинаковой температуре и давлении находится одинаковое количество
- 17. Закон Клапейрона-Менделеева (ф1834р1875) . . . R – универсальная газовая постоянная, Дж/(моль К). Для реальных газов
- 18. Закон Дальтона (а 1803-1805) Давление в смеси газов равно сумме парциальных давлений газов - объемное (молекулярное)
- 19. Закон Рауля (ф1887) Парциальное давление насыщенного пара компонентов жидкости пропорционально его массовой доле (концентрации) в жидкости
- 20. Примеры решения задач
- 21. Задача №1 По газопроводу за полчаса поступает 1500м3 газа при давлении 0,25 МПа и температуре 220С.
- 22. Задача №2 Баллон с газом при температуре 250С и давлении 0,5 МПа нагрели до 500С. Необходимо
- 23. Задача №3 Определить парциальные давления компонентов, входящих в газовую смесь следующего состава: СН4 – 2%, С3Н8
- 24. Задача №4 Определить плотность газа при температуре 250С и давлении 1,0 МПа, если его плотность при
- 25. Задача №5 В емкость 200м3 поместили 50м3 С4Н10 при давлении 0,4 МПа, добавили С3Н8 120м3 при
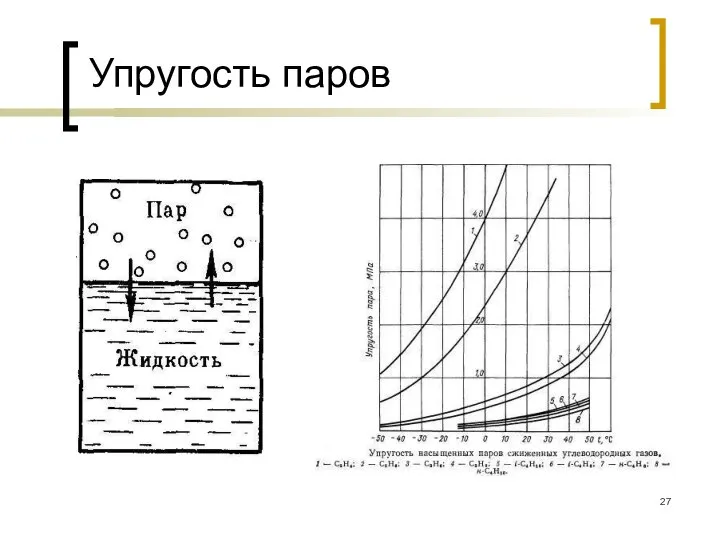
- 26. Давление насыщенных паров Давление, при котором жидкость находится в равновесном состоянии с паром при данной температуре,
- 27. Упругость паров
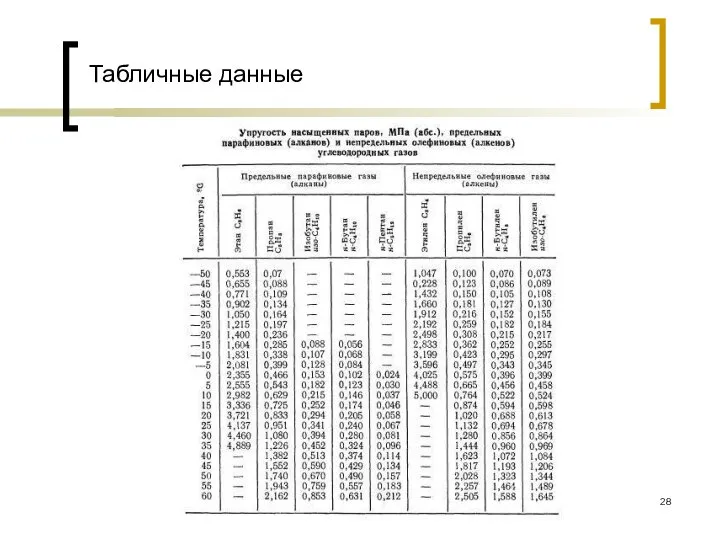
- 28. Табличные данные
- 29. Примеры решения задач
- 30. Задача №6 Определить состав смеси газов равновесной паровой фазы при температуре 300С и следующем молярном составе
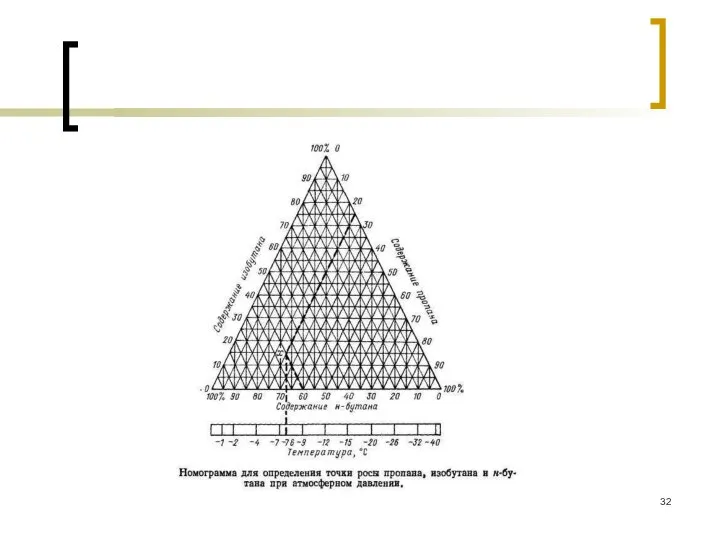
- 31. Точка росы Температура, при которой начинается конденсация насыщенных паров газа при заданном давлении называется точной росы.
- 33. Примеры решения задач
- 34. Задача №7 Определить точку росы смеси газа следующего состава: пропан – 25%, н-бутан –60%, изобутан –
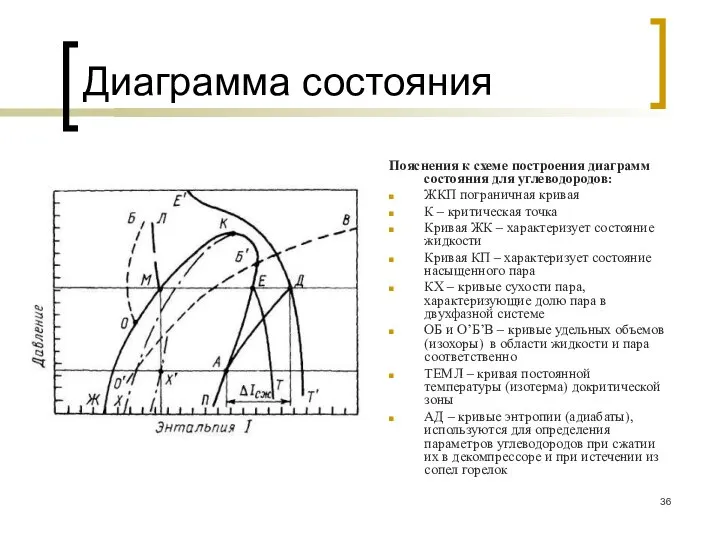
- 35. Диаграмма состояния Диаграмма состояния это графическое отображения состояния и физических свойств газов. Диаграмма строится на полулогарифмической
- 36. Диаграмма состояния Пояснения к схеме построения диаграмм состояния для углеводородов: ЖКП пограничная кривая К – критическая
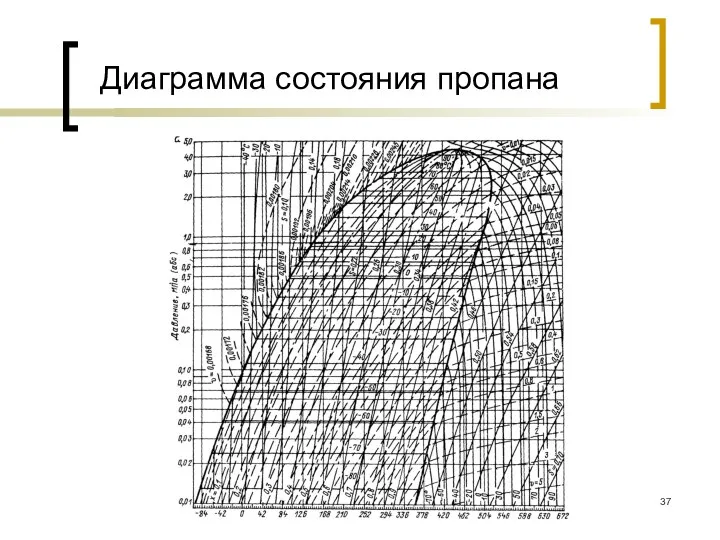
- 37. Диаграмма состояния пропана
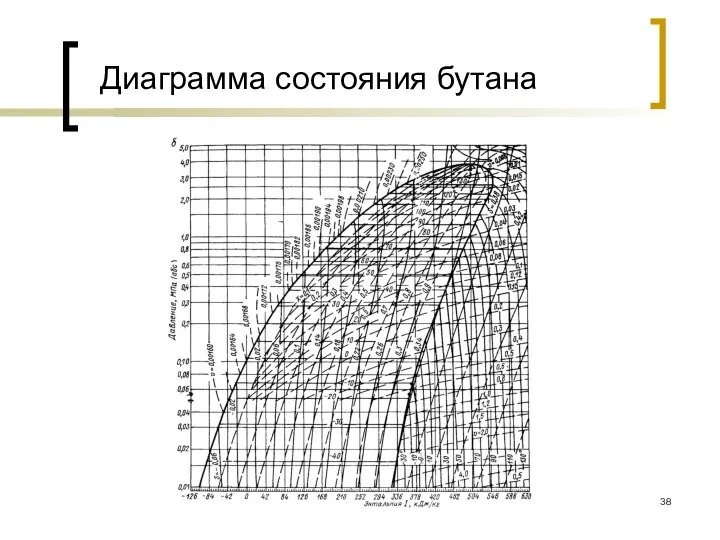
- 38. Диаграмма состояния бутана
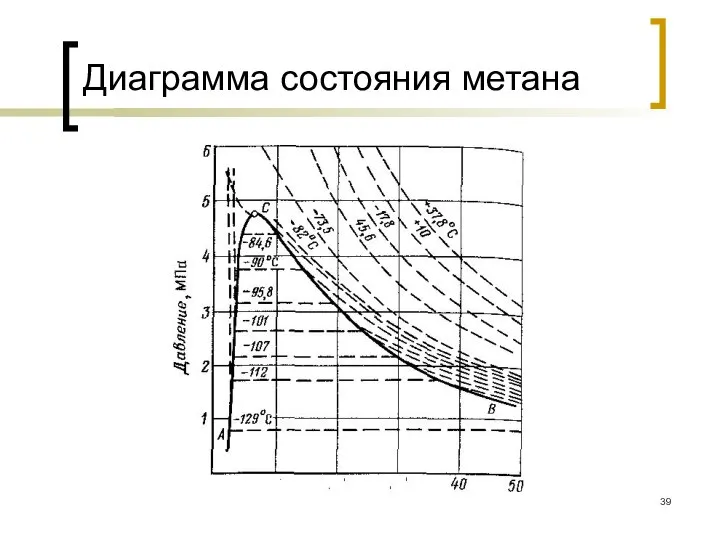
- 39. Диаграмма состояния метана
- 40. Примеры решения задач
- 41. Задача №8 Определить упругость насыщенных паров жидкого пропана, находящегося в резервуаре при температуре минус 100С. Находим
- 42. Задача №9 Определить удельный объем и плотность жидкой и паровой фаз пропана в сосуде при температуре
- 43. Задача №10 После заполнения баллона пропаном объем жидкой фазы составил 85% от объема баллона при температуре
- 44. Задача №10 Общая масса в баллоне . Определим плотность жидкости, когда она заполнит весь объем .
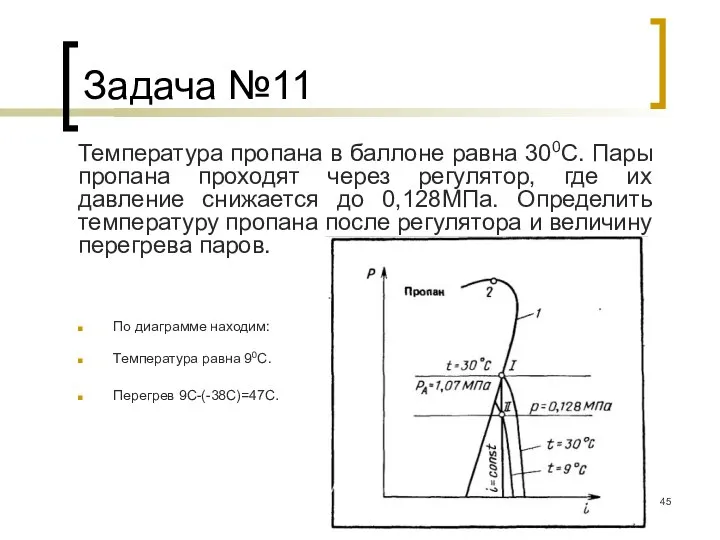
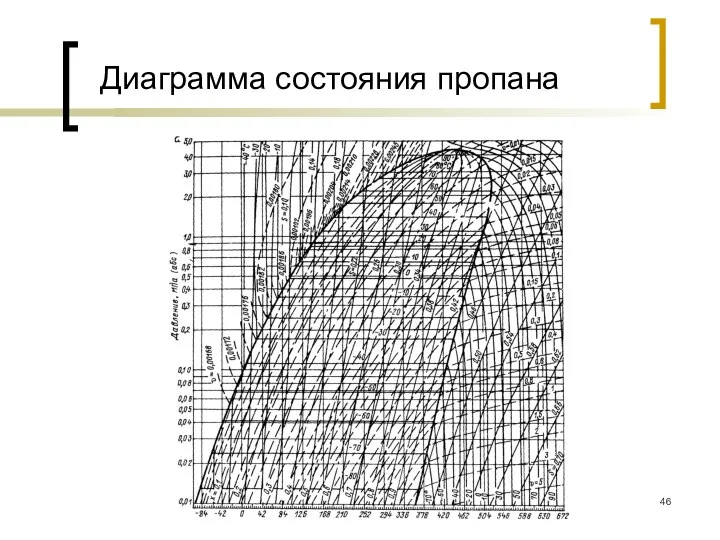
- 45. Задача №11 Температура пропана в баллоне равна 300С. Пары пропана проходят через регулятор, где их давление
- 46. Диаграмма состояния пропана
- 48. Скачать презентацию




































 ГЛАВА №7
ГЛАВА №7 Классный час
Классный час Представление методической темы: Общие методические рекомендации к решению задач по генетике.
Представление методической темы: Общие методические рекомендации к решению задач по генетике. Токарные работы
Токарные работы Скандинавская ходьба
Скандинавская ходьба Презентация на тему Планета Венера
Презентация на тему Планета Венера Неосторожная преступность
Неосторожная преступность Технические средства мультимедиа.Компьютерные презентации
Технические средства мультимедиа.Компьютерные презентации РАЗРЯДЫ ПРИЛАГАТЕЛЬНЫХ
РАЗРЯДЫ ПРИЛАГАТЕЛЬНЫХ Ассоциация ОИРОМ (объединение исследователей рынка и общественного мнения)
Ассоциация ОИРОМ (объединение исследователей рынка и общественного мнения) Урок презентация Кровеносная система человека 4 класс
Урок презентация Кровеносная система человека 4 класс  Презентация на тему: Выборочное изложение по тексту Е.В. Мурашовой
Презентация на тему: Выборочное изложение по тексту Е.В. Мурашовой Наука и образование
Наука и образование ЕГИПЕТСКИЙ ТРЕУГОЛЬНИК
ЕГИПЕТСКИЙ ТРЕУГОЛЬНИК Методы автоматической обработки тем сообщений в потоках новостных сообщений
Методы автоматической обработки тем сообщений в потоках новостных сообщений Мы готовим детей к неизвестным профессиям будущего
Мы готовим детей к неизвестным профессиям будущего Вклад Ломоносова в формирование и развитие русского литературного языка
Вклад Ломоносова в формирование и развитие русского литературного языка Проектирование корпоративных информационных систем
Проектирование корпоративных информационных систем Арт-терапия в начальной школе
Арт-терапия в начальной школе Половое воспитание ребенка
Половое воспитание ребенка Учитель физики высшей категории
Учитель физики высшей категории Алгоритм решения задач по химии
Алгоритм решения задач по химии Презентация на тему Число 3
Презентация на тему Число 3 Презентация на тему: Основные причины возникновения пожара в быту
Презентация на тему: Основные причины возникновения пожара в быту Услуги персонального менеджера
Услуги персонального менеджера Вредным привычкам скажем: «Нет!»
Вредным привычкам скажем: «Нет!» Моделирование и формализация
Моделирование и формализация Что такое родина (1 класс)
Что такое родина (1 класс)