Содержание
- 2. БЕЛКИ - органические биополимеры
- 3. «Жизнь – есть способ существования белковых тел» Ф. Энгельс
- 4. Полипептидную теорию строения белков предложил в 1907 году немецкий ученый Э.Фишер. Полипептидную теорию строения белков предложил
- 5. Выдающим достижением органической химии стал синтез окситоцина – белкового гормона, который стимулирует выделение молока молочными железами.
- 6. В 1945 году английский биохимик Фредерик Сенгер приступил к изучению природного белка – инсулина (гормон поджелудочной
- 7. Сенгер расшифровал строение инсулина. Он состоит из двух полипептидных цепей, связанных в двух местах дисульфидными мостиками.
- 8. Выход нашел американский химик Меррифилд, он открыл метод синтеза белков на полимерных носителях. В 1969 году
- 9. Определение, состав, строение белков
- 10. Белки - сложные высокомолекулярные природные соединения, построенные из остатков α-аминокислот. Аминокислоты в белках связаны пептидными связями.
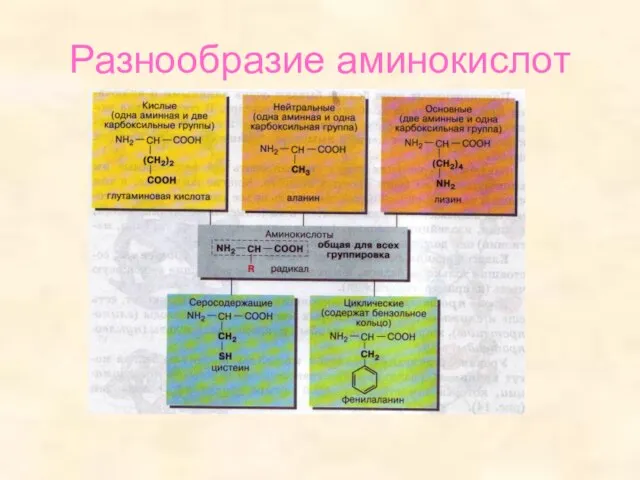
- 11. Разнообразие аминокислот
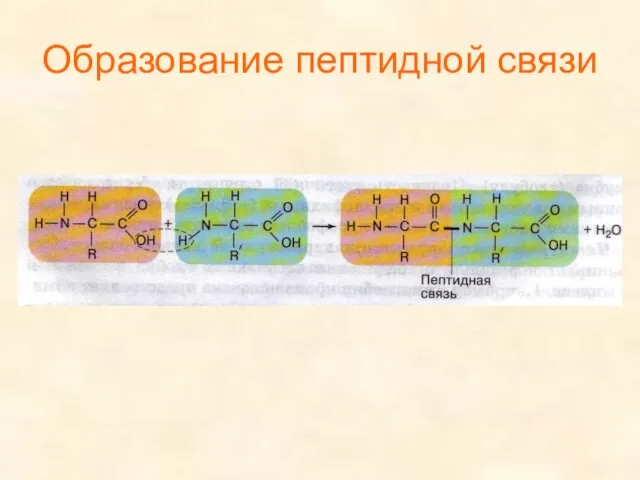
- 12. Образование пептидной связи
- 13. Есть белки, растворимые (например, фибриноген) и нерастворимые (например, фибрин) в воде. Есть белки очень устойчивые (например,
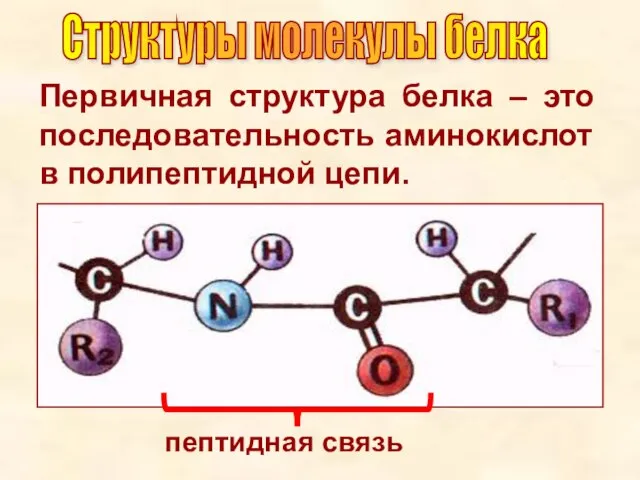
- 14. Первичная структура белка – это последовательность аминокислот в полипептидной цепи. пептидная связь Структуры молекулы белка
- 15. Вторичная структура - спираль, удерживаемая водородными связями. Структуры молекулы белка
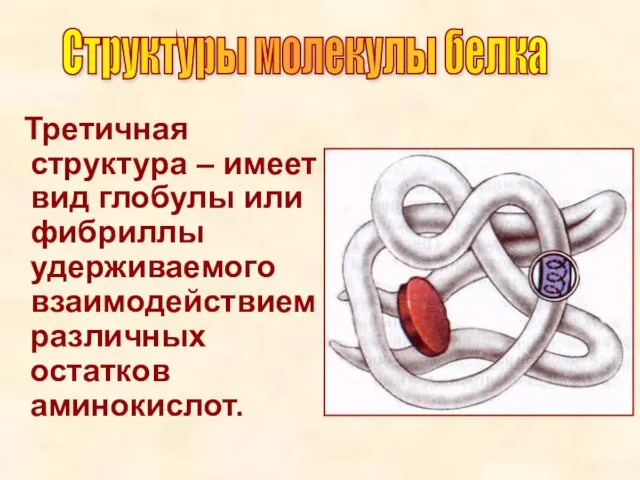
- 16. Третичная структура – имеет вид глобулы или фибриллы удерживаемого взаимодействием различных остатков аминокислот. Структуры молекулы белка
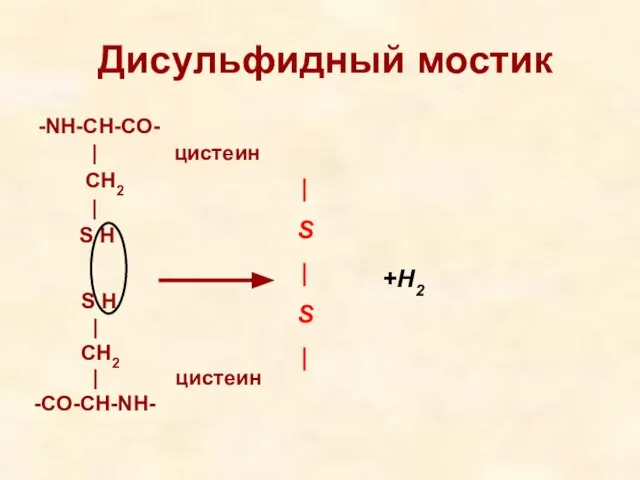
- 17. Дисульфидный мостик -NH-CH-CO- | цистеин CH2 | S H | S | S | +H2 S
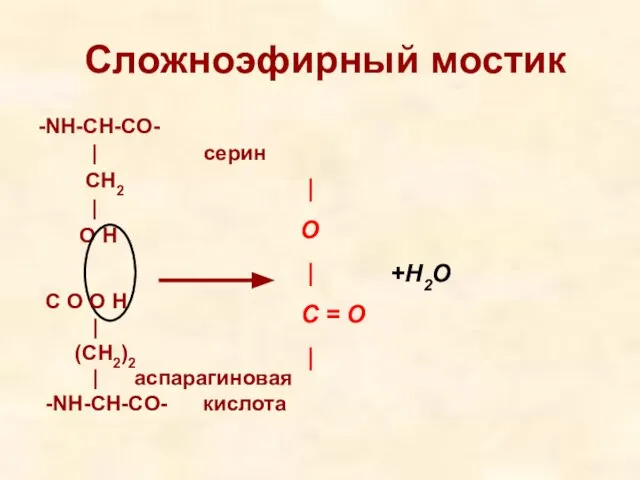
- 18. Сложноэфирный мостик -NH-CH-CO- | серин CH2 | O H | O | C = O |
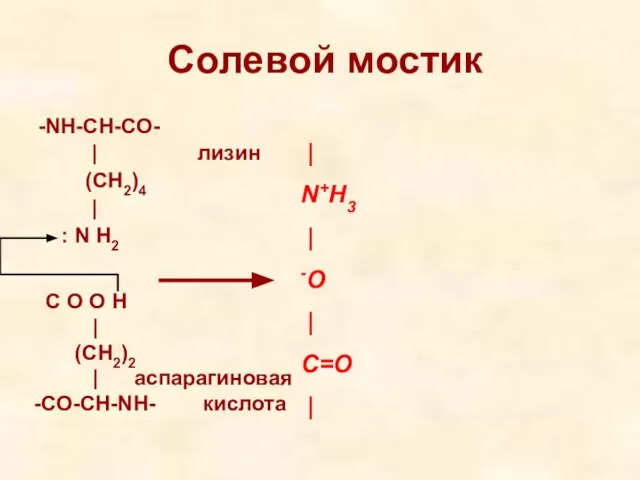
- 19. Солевой мостик -NH-CH-CO- | лизин (CH2)4 | : N H2 | N+H3 | -O | C=O
- 20. Четвертичная структура – характерна только для некоторых белков, соединяет несколько полипептидных цепей. Структуры молекулы белка
- 21. Гидролиз Денатурация и ренатурация Цветные реакции Свойства белков
- 22. Гидролиз
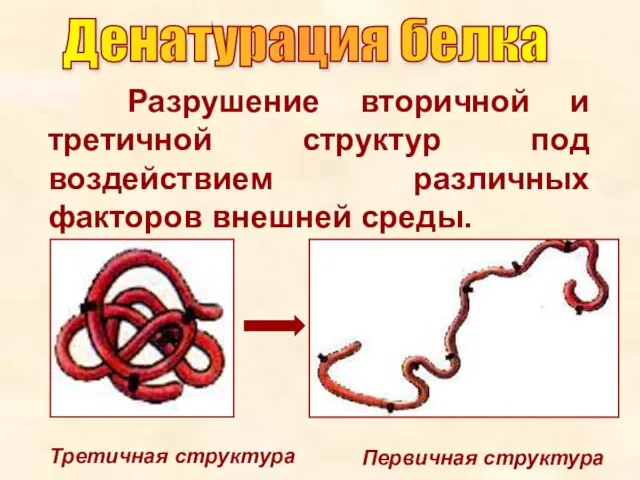
- 23. Разрушение вторичной и третичной структур под воздействием различных факторов внешней среды. Третичная структура Первичная структура Денатурация
- 24. Денатурация белка под воздействием высоких температур Opera - [Свертывание белков при нагревании]
- 25. Под действием химических веществ – щелочей, кислот, солей тяжелых металлов, спиртов. school-collection.iv-edu.ru/catalog/rubr/528b6fb1-98e4-9a27-5ae1-2f785b646a41/23929/ Денатурация белка
- 26. Ксантопротеиновая реакция – желтое окрашивание в присутствии НNO3 при нагревании. Opera - [Органическая химия. Видеоопыты] Биуретовая
- 27. Цветные реакции
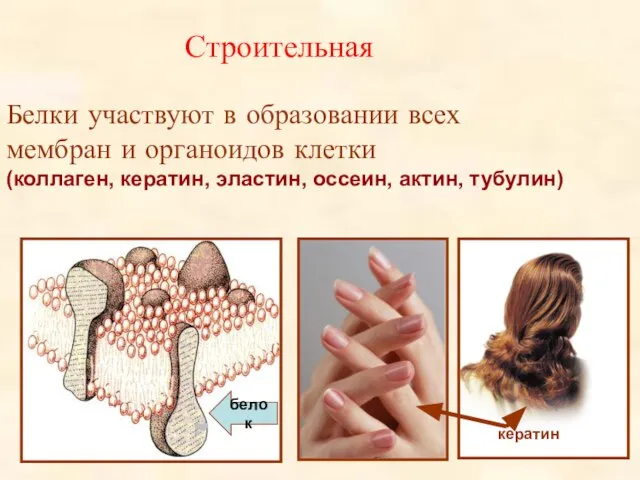
- 28. Строительная Белки участвуют в образовании всех мембран и органоидов клетки (коллаген, кератин, эластин, оссеин, актин, тубулин)
- 29. Каталитическая В каждой клетке имеются сотни ферментов. Они помогают осуществлять биохимические реакции, действуя как катализаторы (белки
- 30. Регуляторная Белки гормоны регулируют различные физиологические процессы (инсулин, гормон роста) Например, инсулин регулирует уровень углеводов в
- 31. Сократительная (двигательная) Белки - участвуют в сокращении мышечных волокон сократительные белки вызывают всякое движение (реснички, жгутики,
- 32. Транспортная Белки связывают и переносят различные вещества и внутри клетки, и по всему организму (альбумин, глобулин,
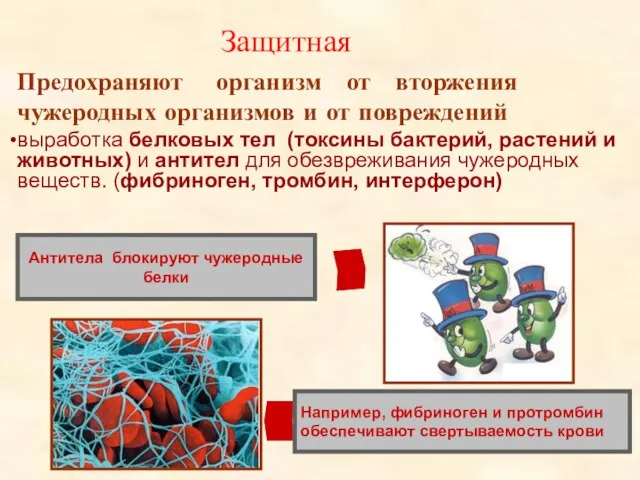
- 33. Защитная Например, фибриноген и протромбин обеспечивают свертываемость крови Антитела блокируют чужеродные белки Предохраняют организм от вторжения
- 34. Энергетическая 1г белка - 17.6 кДж При недостатке углеводов или жиров окисляются молекулы аминокислот При полном
- 35. Рецепторная Реакция на внешний раздражитель
- 36. Домашнее задание §11, вопросы на с. 46, записи в тетради (биология) §27 (белки), с.26 повторить (химия)
- 38. Скачать презентацию













![Денатурация белка под воздействием высоких температур Opera - [Свертывание белков при нагревании]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/459636/slide-23.jpg)







 Реализация проекта. План проекта мебель-трансформер
Реализация проекта. План проекта мебель-трансформер Урок презентация на тему Храм Василия Блаженного
Урок презентация на тему Храм Василия Блаженного  EISBERG MODELL
EISBERG MODELL «Преобразование транспортно-коммуникационных пространств городов. Санкт-Петербург. Площадь Балтийского вокзала»
«Преобразование транспортно-коммуникационных пространств городов. Санкт-Петербург. Площадь Балтийского вокзала» История одного города
История одного города Опыт использования учебников «Органическая химия» и «Общая химия» для обучения школьников на профильном уровне
Опыт использования учебников «Органическая химия» и «Общая химия» для обучения школьников на профильном уровне Презентация на тему Секреты долголетия
Презентация на тему Секреты долголетия Профсоюзы
Профсоюзы Налоговая реформа княгини Ольги
Налоговая реформа княгини Ольги Здоровьесберегающие образовательные технологии в педиатрии
Здоровьесберегающие образовательные технологии в педиатрии  Управление качеством образования на основе совершенствования научно-методической работы
Управление качеством образования на основе совершенствования научно-методической работы Практика стратегического анализа в российских городах
Практика стратегического анализа в российских городах МИСПИ(1)
МИСПИ(1) Анна Ахматова
Анна Ахматова Ребёнок один в машине
Ребёнок один в машине Китайские картины
Китайские картины Презентация на тему Требования к оформлению презентации
Презентация на тему Требования к оформлению презентации Требования к курсовой работе
Требования к курсовой работе Быстрая настройка рекламы в свадебной сфере!
Быстрая настройка рекламы в свадебной сфере! Калькулювання виробничой собівартості продукціи (робіт, послуг)
Калькулювання виробничой собівартості продукціи (робіт, послуг) СКОРО В ПРОДАЖЕ Артикул: 116012 Размер: 56,62 Лот 8 шт. Цвет: желтый, розовый, голубой, белый Полотно: капитон Примечания: застежка – кнопки
СКОРО В ПРОДАЖЕ Артикул: 116012 Размер: 56,62 Лот 8 шт. Цвет: желтый, розовый, голубой, белый Полотно: капитон Примечания: застежка – кнопки Street-Art et immeubles peints
Street-Art et immeubles peints Выбор ниши
Выбор ниши Презентация на тему Детство Пушкина (9 класс)
Презентация на тему Детство Пушкина (9 класс)  Полевые транзисторы. Самостоятельная работа
Полевые транзисторы. Самостоятельная работа Презентация на тему Жизнь и творчество А.Т. Твардовского
Презентация на тему Жизнь и творчество А.Т. Твардовского  Модерн в природе
Модерн в природе Закономерности эволюции
Закономерности эволюции