Содержание
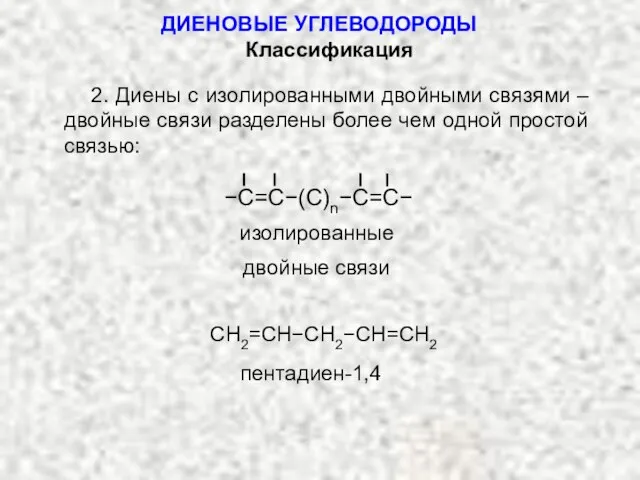
- 2. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ 2. Диены с изолированными двойными связями – двойные связи разделены более чем одной простой
- 3. 3. Диены с непосредственно примыкающими друг к другу двойными связями – кумулированые двойные связи (аллены): CH2=C=CH2
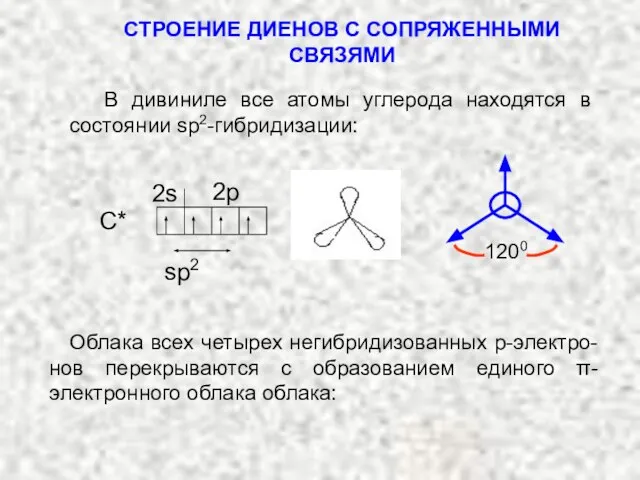
- 4. В дивиниле все атомы углерода находятся в состоянии sp2-гибридизации: 1200 Облака всех четырех негибридизованных р-электро-нов перекрываются
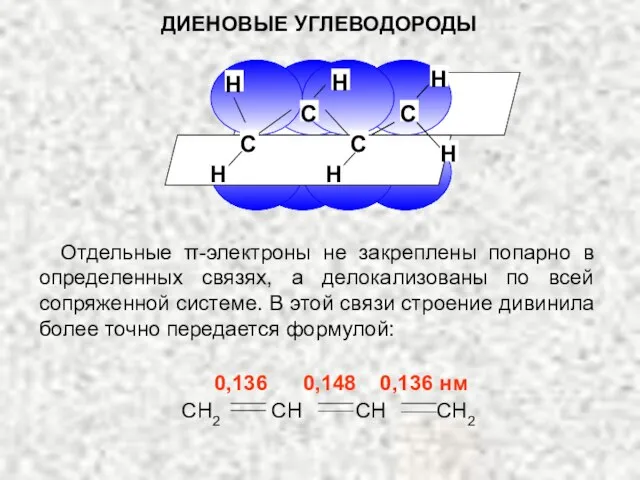
- 5. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ Отдельные π-электроны не закреплены попарно в определенных связях, а делокализованы по всей сопряженной системе.
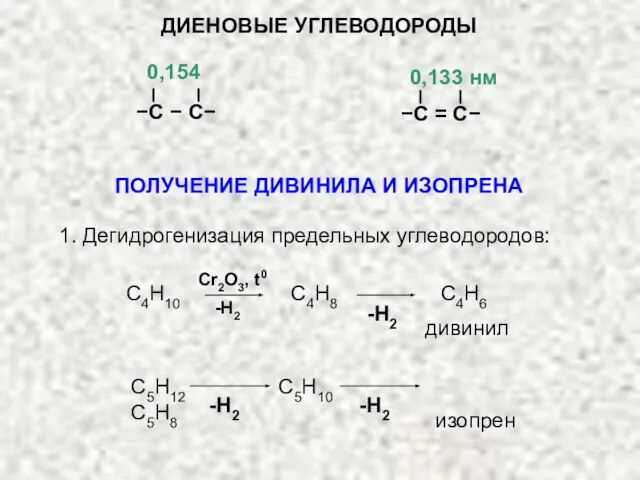
- 6. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ 0,154 −С − С− 0,133 нм −С = С− ПОЛУЧЕНИЕ ДИВИНИЛА И ИЗОПРЕНА 1.
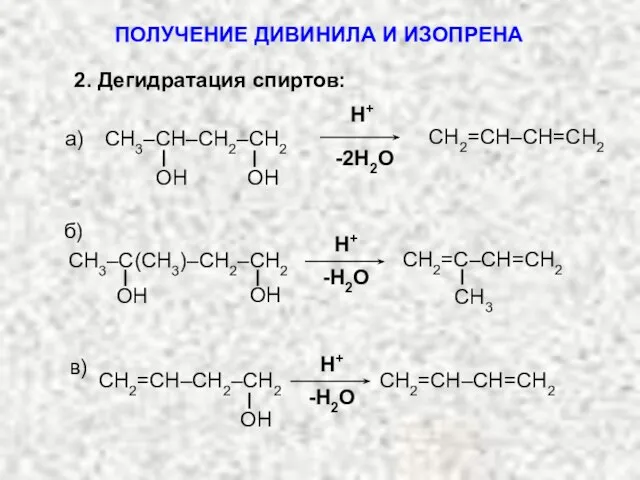
- 7. H+ -2H2O CH2=CH–CH=CH2 OH OH СH3–CH–CH2–CH2 а) -H2O CH3 CH2=C–CH=CH2 OH OH CH3–C(CH3)–CH2–CH2 H+ CH2=CH–CH=CH2 OH
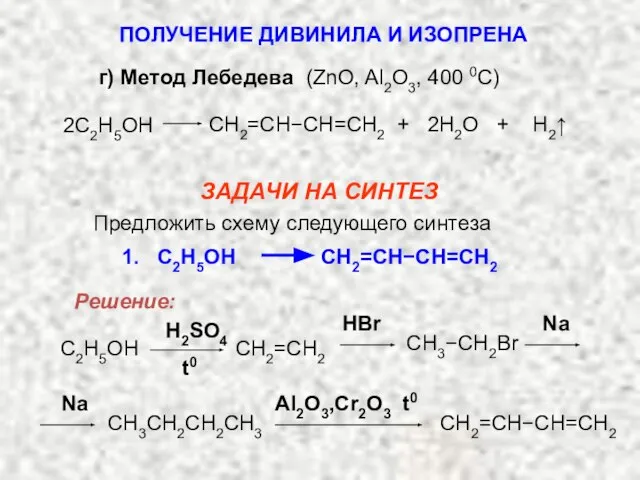
- 8. г) Метод Лебедева (ZnO, Al2O3, 400 0C) СH2=CH−CH=CH2 + 2H2O + H2↑ 2C2H5OH ЗАДАЧИ НА СИНТЕЗ
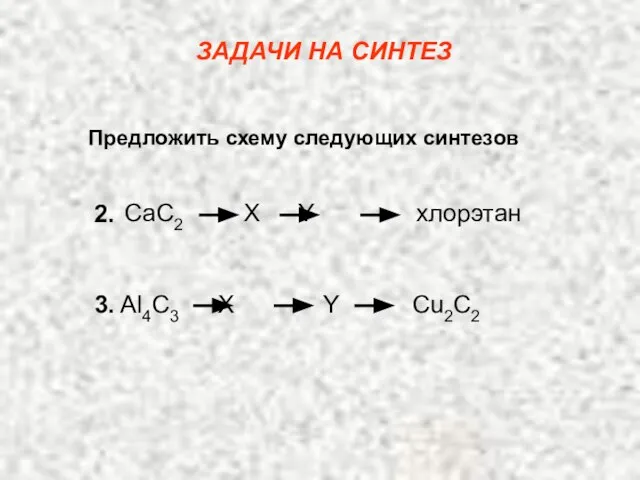
- 9. Предложить схему следующих синтезов ЗАДАЧИ НА СИНТЕЗ CaC2 X Y хлорэтан 2. 3. Al4C3 X Y
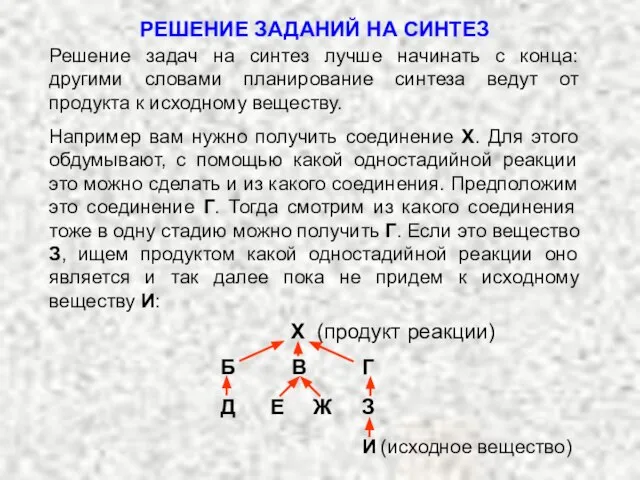
- 10. РЕШЕНИЕ ЗАДАНИЙ НА СИНТЕЗ Решение задач на синтез лучше начинать с конца: другими словами планирование синтеза
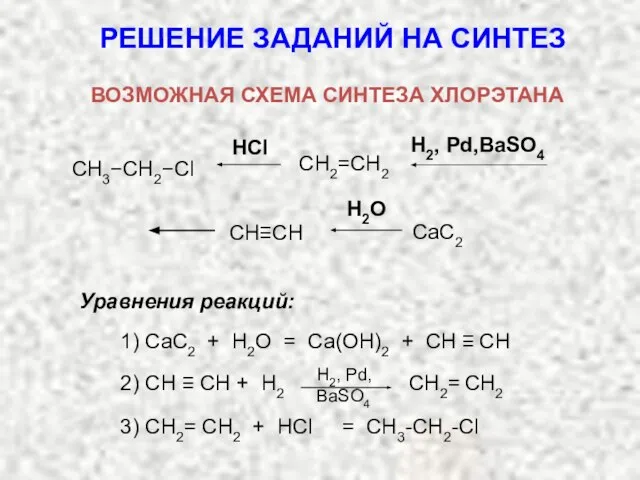
- 11. HCl H2, Pd,BaSO4 CH2=CH2 CH3−CH2−Cl H2O CaC2 CH≡CH РЕШЕНИЕ ЗАДАНИЙ НА СИНТЕЗ ВОЗМОЖНАЯ СХЕМА СИНТЕЗА ХЛОРЭТАНА
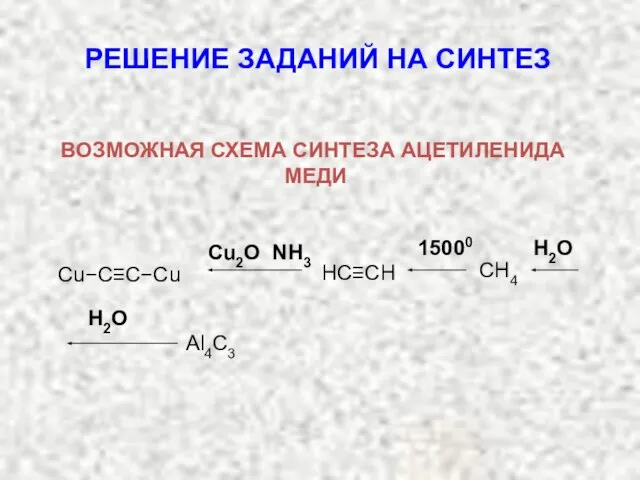
- 12. Cu2O NH3 15000 H2O CH4 HC≡CH Cu−C≡C−Cu РЕШЕНИЕ ЗАДАНИЙ НА СИНТЕЗ ВОЗМОЖНАЯ СХЕМА СИНТЕЗА АЦЕТИЛЕНИДА МЕДИ
- 13. ХИМИЧЕСКИЕ СВОЙСТВА ДИЕНОВ Типичными реакциями для диенов, как и для алкенов являются реакции электрофильного присоединения. При
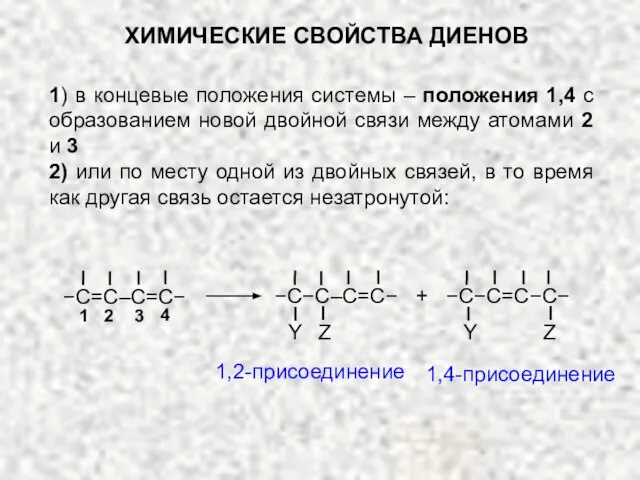
- 14. 1,2-присоединение 1,4-присоединение Z Y + −C−C=C−C− Z Y −C−C–C=C− −C=C–C=C− ХИМИЧЕСКИЕ СВОЙСТВА ДИЕНОВ 1) в концевые
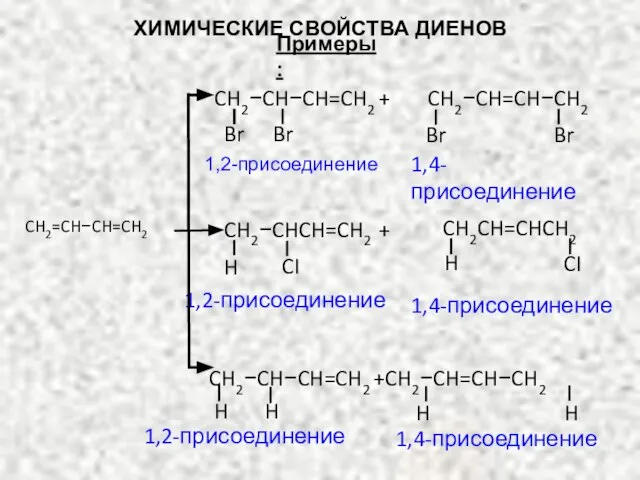
- 15. Примеры: CH2=CH−CH=CH2 1,2-присоединение 1,4-присоединение 1,2-присоединение 1,4-присоединение 1,2-присоединение 1,4-присоединение CH2−CH−CH=CH2 + Br Br CH2−CH=CH−CH2 Br Br H
- 16. Механизм электрофильного присоединения к диенам Ранее было показано, что электрофильное присоеди-нение представляет собой двухстадийный процесс и
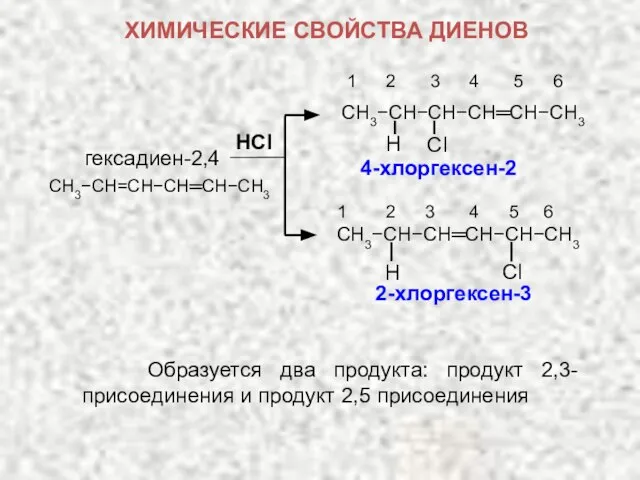
- 17. HСl гексадиен-2,4 4-хлоргексен-2 1 2 3 4 5 6 CH3−CH−CH−CH═CH−CH3 Сl H 2-хлоргексен-3 1 2 3
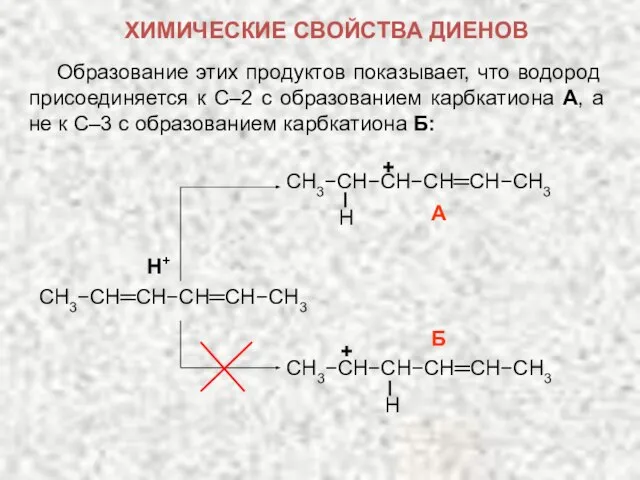
- 18. Образование этих продуктов показывает, что водород присоединяется к С–2 с образованием карбкатиона А, а не к
- 19. Оба карбкатиона являются вторичными, но А устойчивее, чем Б. Карбкатион А является не просто вторичным карбкатионом:
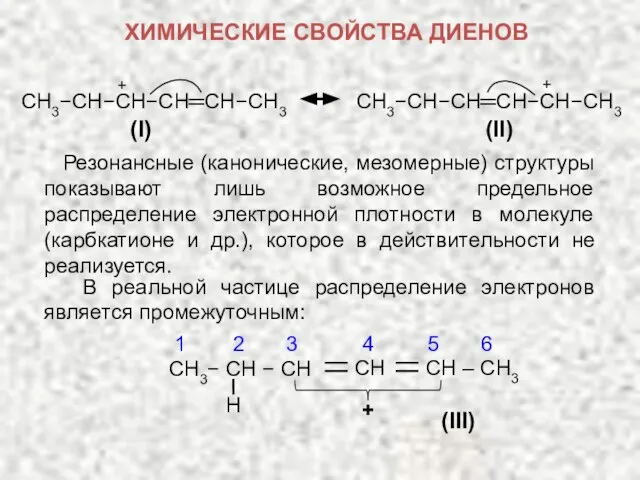
- 20. CH3−CH−CH−CH═CH−CH3 (I) CH3−CH−CH═CH−CH−CH3 (II) Резонансные (канонические, мезомерные) структуры показывают лишь возможное предельное распределение электронной плотности в
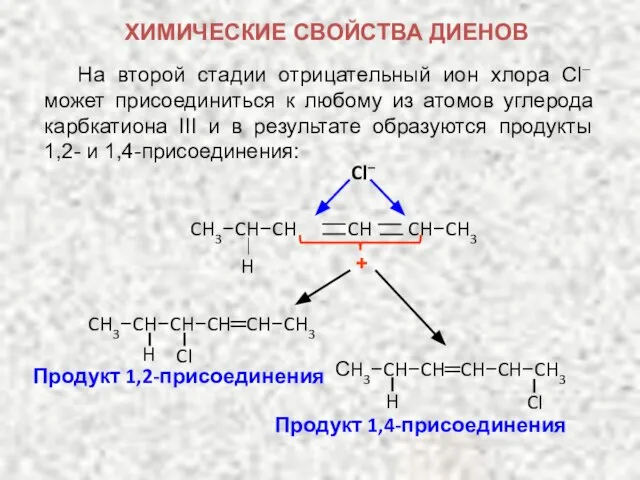
- 21. На второй стадии отрицательный ион хлора Cl– может присоединиться к любому из атомов углерода карбкатиона III
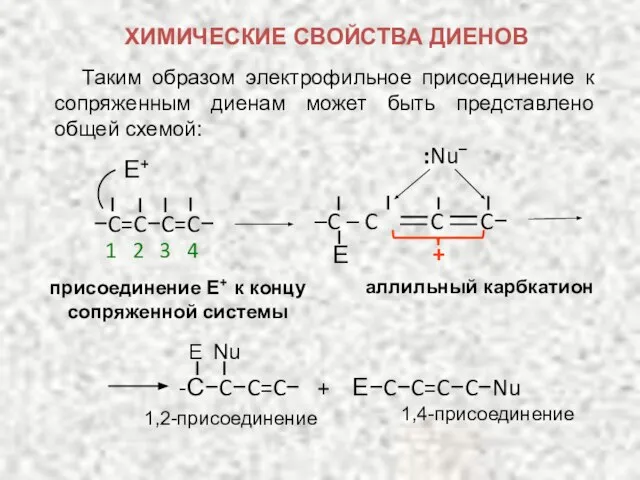
- 22. Таким образом электрофильное присоединение к сопряженным диенам может быть представлено общей схемой: присоединение Е+ к концу
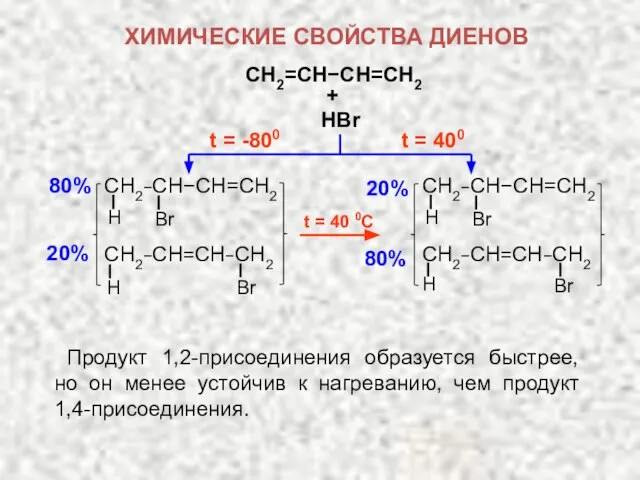
- 23. 20% t = 40 0C 80% Продукт 1,2-присоединения образуется быстрее, но он менее устойчив к нагреванию,
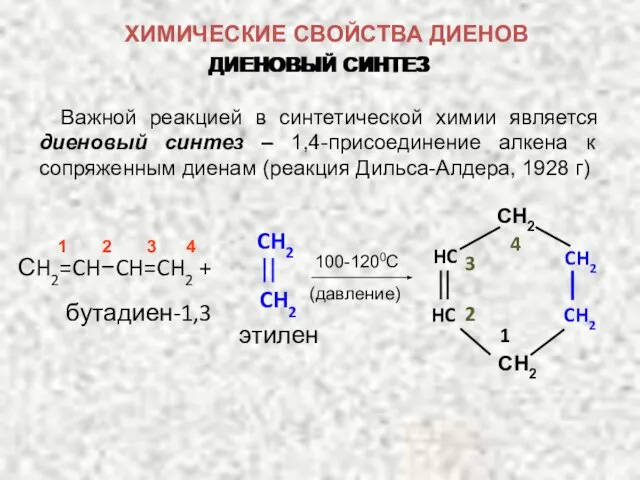
- 24. ДИЕНОВЫЙ СИНТЕЗ Важной реакцией в синтетической химии является диеновый синтез – 1,4-присоединение алкена к сопряженным диенам
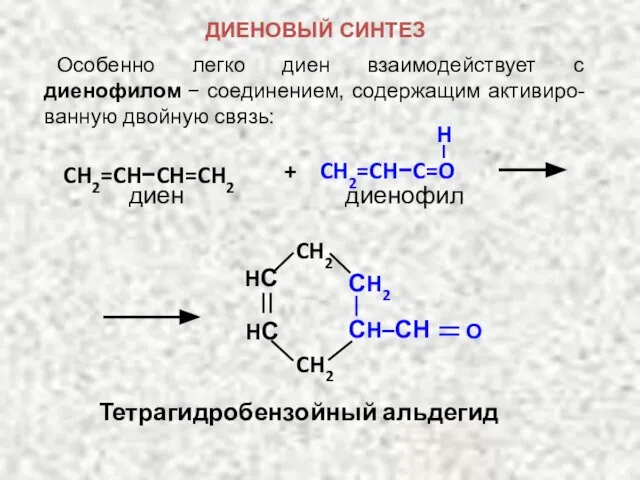
- 25. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ Особенно легко диен взаимодействует с соедиением, содержащим активированную двойную связь − с диенофилом:
- 26. диенофил диен H + CH2=CH−C=O CH2=CH−CH=CH2 Тетрагидробензойный альдегид CH2 CH2 О HС HС СH2 СH–СН ДИЕНОВЫЙ
- 27. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ ПОЛИМЕРИЗАЦИЯ СОПРЯЖЕННЫХ ДИЕНОВ Сравнение алкенов и диенов: n∙ АЛКЕН АЛКАН n∙ ДИЕН продукт с
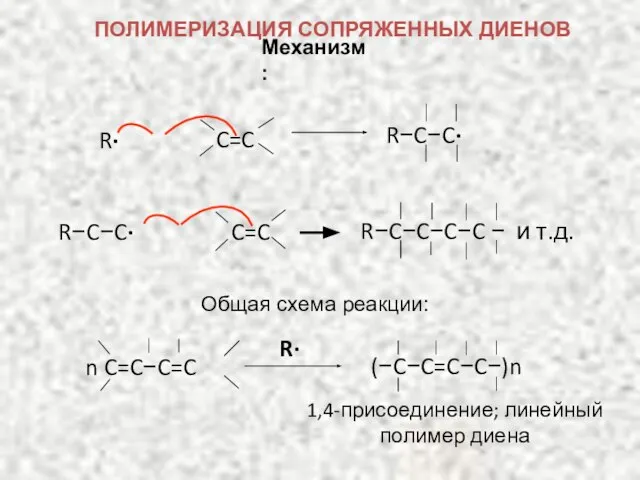
- 28. Механизм: R−C−C∙ R∙ R−C−C−C−C − и т.д. R−C−C∙ Общая схема реакции: 1,4-присоединение; линейный полимер диена (−C−C=C−C−)n
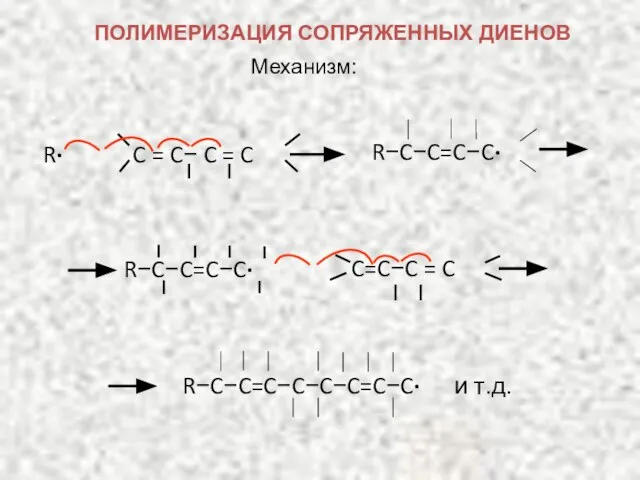
- 29. Механизм: R−C−C=C−C∙ R∙ C = C− C = C C=C−C = C R−C−C=C−C∙ ПОЛИМЕРИЗАЦИЯ СОПРЯЖЕННЫХ ДИЕНОВ
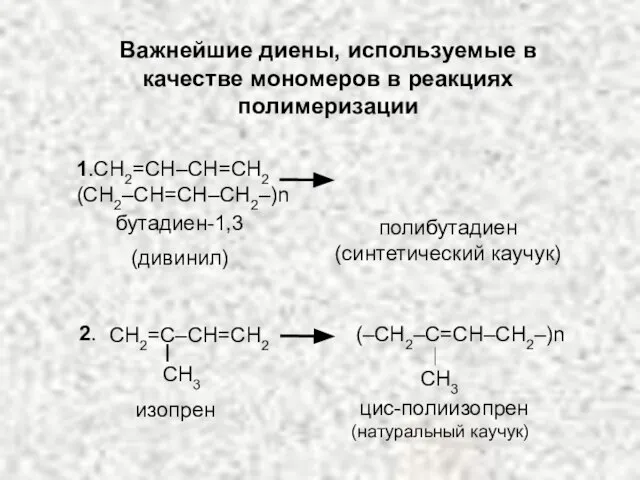
- 30. Важнейшие диены, используемые в качестве мономеров в реакциях полимеризации 1.СH2=CH–CH=CH2 (CH2–CH=CH–CH2–)n бутадиен-1,3 (дивинил) полибутадиен (синтетический каучук)
- 32. Скачать презентацию






 Пошаговая инструкция по изготовлению бетонных поделок Гриб и лебедь
Пошаговая инструкция по изготовлению бетонных поделок Гриб и лебедь Toyota TRD TGB
Toyota TRD TGB 02_09_22Презентация_Математическая_викторина_для_6_класса
02_09_22Презентация_Математическая_викторина_для_6_класса Установка контролера
Установка контролера «Крестики – нолики» литературная игра VI отборочный тур
«Крестики – нолики» литературная игра VI отборочный тур Проект Страна Бразилия Выполнила: Ильмушкина Диана, ученица7 «
Проект Страна Бразилия Выполнила: Ильмушкина Диана, ученица7 « Футбол
Футбол 365046
365046 Технология токарных работ по металлу. Режущий инструмент
Технология токарных работ по металлу. Режущий инструмент химия в медицине
химия в медицине EISBERG MODELL
EISBERG MODELL Рекомендации по содержанию странички ППО на сайте ОУ
Рекомендации по содержанию странички ППО на сайте ОУ Тело в кинематографе
Тело в кинематографе Методы исследований в менеджменте. Введение в дисциплину
Методы исследований в менеджменте. Введение в дисциплину fa2994ac-6d4d-45dc-97c2-1c805aa21d0a (2)
fa2994ac-6d4d-45dc-97c2-1c805aa21d0a (2) PLACENSE Описание проекта
PLACENSE Описание проекта Смычковые инструменты
Смычковые инструменты Презентация на тему Сердечно-легочная реанимация
Презентация на тему Сердечно-легочная реанимация ВАКЦИНЫ ДЛЯ ПЛАНОВОЙ ПРОФИЛАКТИКИ
ВАКЦИНЫ ДЛЯ ПЛАНОВОЙ ПРОФИЛАКТИКИ  Подведение итогов деятельности совета старшеклассников Тельмановского района за 2020-2021 учебный год
Подведение итогов деятельности совета старшеклассников Тельмановского района за 2020-2021 учебный год Бумажные шарики
Бумажные шарики Трудности подросткового возраста
Трудности подросткового возраста Презентация на тему Правописание сочетаний Чк чн
Презентация на тему Правописание сочетаний Чк чн ПОРТФОЛИО УЧИТЕЛЯ БИОЛОГИИ
ПОРТФОЛИО УЧИТЕЛЯ БИОЛОГИИ Светотехнический расчет заданного помещения в заданном районе строительства
Светотехнический расчет заданного помещения в заданном районе строительства Жанры ИЗО
Жанры ИЗО Рассолы для колбас. Lofink grupp
Рассолы для колбас. Lofink grupp Практика по психологии
Практика по психологии