Содержание
- 2. это процессы, в результате которых из одних веществ образуются другие, отличающиеся от них по составу и
- 3. По числу и составу реагирующих и образующихся веществ По изменению степени окисления атомов элементов По использованию
- 4. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие без изменения состава веществ. В
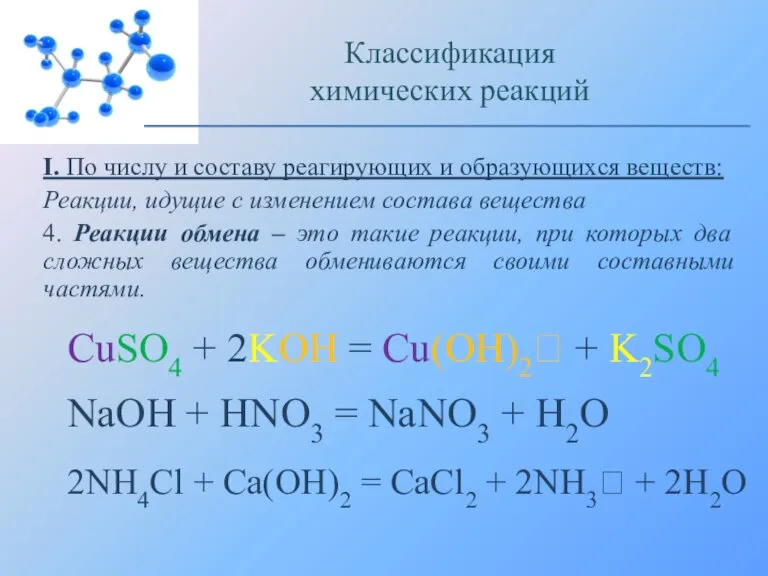
- 5. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 1.
- 6. Горение серы в кислороде: Классификация химических реакций
- 7. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 2.
- 8. Получение кислорода из перманганата калия: Классификация химических реакций
- 9. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 3.
- 10. Взаимодействие натрия с водой: Классификация химических реакций
- 11. I. По числу и составу реагирующих и образующихся веществ: Реакции, идущие с изменением состава вещества 4.
- 12. Получение аммиака из нашатыря Классификация химических реакций
- 13. II. По изменению степеней окисления химических элементов: 1. Окислительно-восстановительные реакции – реакции, идущие с изменением степеней
- 14. Взаимодействие железа с медным купоросом: Классификация химических реакций
- 15. III. По использованию катализатора: 1. Некаталитические реакции – реакции, идущие без участия катализатора: Классификация химических реакций
- 16. III. По использованию катализатора: 1. Каталитические реакции – реакции, идущие с участием катализатора: Классификация химических реакций
- 17. Разложение пероксида водорода: Классификация химических реакций
- 18. IV. По направлению: 1. Необратимые реакции протекают в данных условиях только в одном направлении: Классификация химических
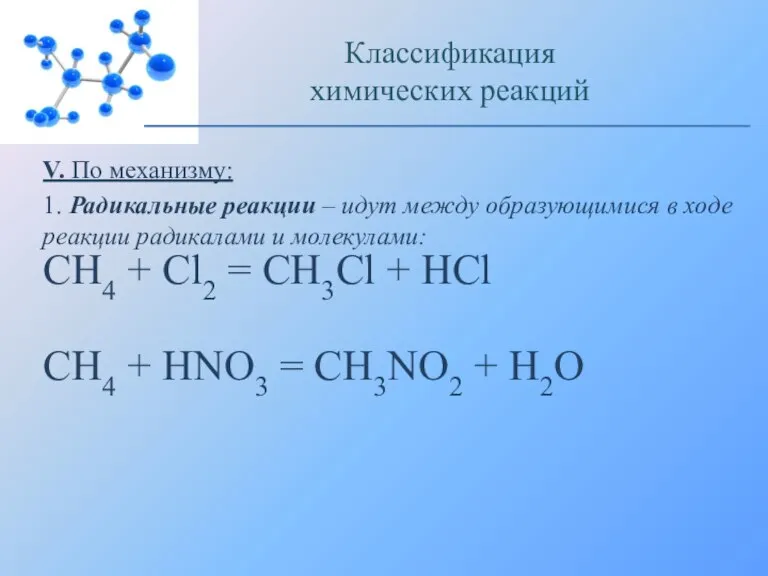
- 19. V. По механизму: 1. Радикальные реакции – идут между образующимися в ходе реакции радикалами и молекулами:
- 20. V. По механизму: 2. Ионные реакции – идут между уже имеющимися или образующимися в ходе реакции
- 21. VI. По тепловому эффекту: 1. Экзотермические реакции протекают с выделением энергии: Классификация химических реакций 4P +
- 22. Горение фосфора в кислороде: Классификация химических реакций
- 23. VI. По тепловому эффекту: 2. Эндотермические реакции протекают с поглощением энергии: Классификация химических реакций N2 +
- 24. Разложение оксида ртути: Классификация химических реакций
- 25. VII. По виду энергии, инициирующей реакцию: Фотохимические реакции инициируются световой энергией. Радиационные реакции инициируются излучениями большой
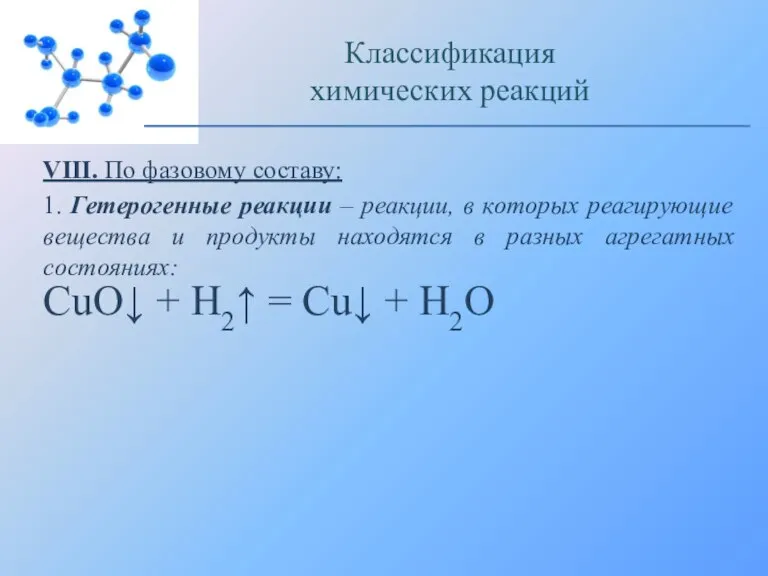
- 26. VIII. По фазовому составу: 1. Гетерогенные реакции – реакции, в которых реагирующие вещества и продукты находятся
- 27. Восстановление оксида меди (II) водородом: Классификация химических реакций
- 29. Скачать презентацию























 Титульный лист
Титульный лист Учителями славится Россия ,ученики приносят славу ей…
Учителями славится Россия ,ученики приносят славу ей… Авторское право и дизайн
Авторское право и дизайн ПРОЕКТ«ШКОЛЬНЫЙ ДВОР»МОУ СОШ № 18 г.Костромы
ПРОЕКТ«ШКОЛЬНЫЙ ДВОР»МОУ СОШ № 18 г.Костромы Экономическое развитие. Экономическая деятельность и условия её эффективности.
Экономическое развитие. Экономическая деятельность и условия её эффективности. Космические модули. Конфуций
Космические модули. Конфуций Бухгалтерский учёт и налоговый контроль
Бухгалтерский учёт и налоговый контроль Маркетинговые исследования. Тема 3
Маркетинговые исследования. Тема 3 2 людей тратят больше времени на общение в интернете, чем в реальной жизни 57 % крупных компаний США планируют использовать в продвиж
2 людей тратят больше времени на общение в интернете, чем в реальной жизни 57 % крупных компаний США планируют использовать в продвиж ПРОЕКТ«ИСТОРИЯ В ЮГУ»
ПРОЕКТ«ИСТОРИЯ В ЮГУ» Набор в секции. Отделение сложно-координационных видов
Набор в секции. Отделение сложно-координационных видов Предлагаем Вам рассмотреть коммерческое предложение на поставку самосвалов SHACMAN SX3255DR384 6x4 336 л.с. (технология МAN)
Предлагаем Вам рассмотреть коммерческое предложение на поставку самосвалов SHACMAN SX3255DR384 6x4 336 л.с. (технология МAN) Эпиграфы урока Человек – это звучит гордо ! Существует только человек, всё остальное – дело его рук, его мозга. М. Горький « На дне »
Эпиграфы урока Человек – это звучит гордо ! Существует только человек, всё остальное – дело его рук, его мозга. М. Горький « На дне »  Тема:220 г. до н.э. Чжан Чжунцзин публикует «Шань Хань Лунь»-самый древний полный учебник по медицине, уделяющий внимание диагностик
Тема:220 г. до н.э. Чжан Чжунцзин публикует «Шань Хань Лунь»-самый древний полный учебник по медицине, уделяющий внимание диагностик Основы психологии и педагогики
Основы психологии и педагогики Государственное управление комплексом черной металлургии
Государственное управление комплексом черной металлургии Мир увлечений
Мир увлечений Преступление и уголовная ответственность
Преступление и уголовная ответственность Школьная площадка МБОУ Марининской СОШ № 16
Школьная площадка МБОУ Марининской СОШ № 16 Информационные образовательные ресурсы нового поколения
Информационные образовательные ресурсы нового поколения Основы подготовки к военной службе. Практикумы
Основы подготовки к военной службе. Практикумы Однолетние цветковые растения
Однолетние цветковые растения Незаконный оборот наркотических веществ
Незаконный оборот наркотических веществ Отчет о финансовых результатах (форма №2)
Отчет о финансовых результатах (форма №2) Роль физической культуры в укреплении здоровья
Роль физической культуры в укреплении здоровья Mit App Inventor
Mit App Inventor ОДО ФЛиС
ОДО ФЛиС Население России. История переписи населения
Население России. История переписи населения