Слайд 2Оксиды
Образованы двумя химическими элементами
Один из элементов кислород, имеющий степень окисления

-2
Примеры: MgO, H2O
Слайд 3Оксидами являются оба вещества в паре
1)MgO и H2O2
2)Na 2O2 и BaO
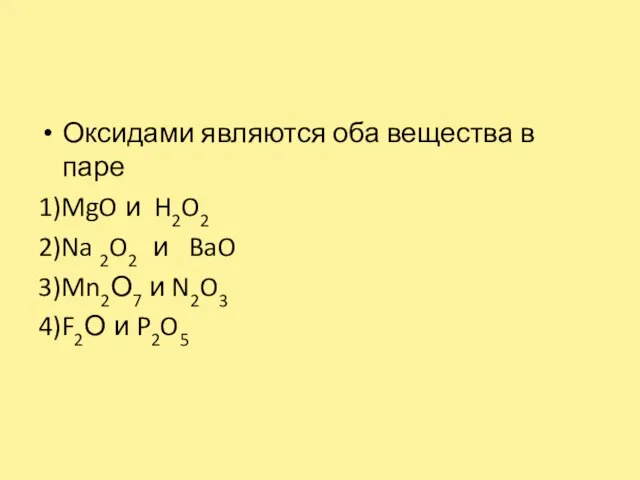
3)Mn2О7 и N2O3
4)F2О и P2O5
Слайд 4Классификация оксидов
Несолеобразующие (безразличные)
NO
CO
N2O
Солеобразующие
Основные
Кислотные
Амфотерные

Слайд 5Основные оксиды
Оксиды металлов, в которых металл имеет степень окисления +1 или +2

как правило
Основным оксидам соответствуют основания (основные гидроксиды):
Na2O – NaOH
MgO – Mg(OH)2
Слайд 6Свойства основных оксидов
Реагируют с кислотами:
MgO + H2SO4 = MgSO4 +

H2O
Некоторые реагируют с водой (оксиды щелочных и щелочно-земельных металлов):
Na2O + H2O = 2NaOH
Реагируют с кислотными оксидами:
CaO + CO2 = CaCO3
Слайд 7Кислотные оксиды
Оксиды неметаллов и металлов, в которых элемент имеет степень окисления

+4 и выше как правило
Кислотным оксидам соответствуют кислоты (кислотные гидроксиды):
CO2 – H2CO3 Mn2O7 – HMnO4
SO3 – H2SO4 CrO3 – H2CrO4, H2Cr2O7
Слайд 8Свойства кислотных оксидов
Реагируют со щелочами (растворимыми в воде основаниями):
CO2 + 2NaOH

= Na2CO3 + H2O
Большинство реагирует с водой:
SO3 + H2O = H2SO4
Реагируют с основными оксидами:
P2O5 + 3CaO = Ca3(PO4)2
Слайд 9Амфотерные оксиды
Оксиды металлов, в которых металл проявляет степень окисления +3 или

+4 как правило
Амфотерным оксидам соответствуют амфотерные гидроксиды:
Al2O3 – Al(OH)3 ZnO – Zn(OH)2
Cr2O3 – Cr(OH)3 BeO – Be(OH)2
MnO2 – Mn(OH)4
Слайд 10Свойства амфотерных оксидов
Амфотерность – двойственность свойств
Реагируют с кислотами, проявляя свойства основных

оксидов:
Al2O3 + 6HCl = 2AlCl3 + 3H2O
Реагируют со щелочами, проявляя свойства кислотных оксидов:
Al2O3 + 2NaOH + 3H2O= 2Na[Al(OH)4]
Al2O3 + 2NaOH = 2NaAlO2 + H2O (при сплавлении)
Слайд 11С водой реагируют оксиды:
1)BaO и SiO2
2)СuO и SO3
3)BaO и SO3
4)FeO и

СО2
Слайд 12Оксид серы (IV) взаимодействует с каждым из двух веществ:
1)H2O и KCl
2)Ba(OH)2 и

CaO
3)CaCO3 и ZnSO3
4)Ca(OH)2 и N2
Слайд 13С соляной кислотой реагируют каждый из двух оксидов
1)K2O и SO3
2)Al2O3 и CaO

3)CO2 и ZnO
4)CrO3 и Na2O
Слайд 14И с раствором гидроксида натрия и с серной кислотой реагирует
1)ВаO

2) Cr2O3
3) SiO2
4) MgO
Слайд 15Гидроксиды
Основные – основания (щелочи и нерастворимые в воде)
Кислотные – кислоты кислородсодержащие
Амфотерные

Слайд 16Только кислоты расположены в ряду
1)HNO3, Ca(NO3)2, NO2
2)KHCO3, Ba(HSO4)2, Zn(OH)Cl
3)HNO2, HNO3, CH3COONa
4)H2S, Н2SO3,

CH3COOH
Слайд 17Оцените правильность следующих суждений:
А) Гидроксиды по свойствам делятся на кислоты, основания и

амфотерные гидроксиды.
Б) Гидроксиды элементов главных подгрупп первой и второй групп Периодической системы – растворимые основания (щелочи).
1)верно только А
2)верно только Б
3)верны оба суждения
4)оба суждения неверны
Слайд 18Щелочи – растворимые в воде основания
Щелочи образуют металлы 1 группы главной подгруппы

(щелочные металлы) и щелочноземельные металлы (Ca, Sr, Ba)
Примеры: NaOH, Ca(OH)2
Слайд 19Свойства щелочей
Реагируют с кислотами:
2NaOH + H2SO4 = Na2SO4 + 2H2O
Реагируют с

кислотными оксидами:
2NaOH + CO2 = Na2CO3 + H2O
Реагируют с растворами солей, если выпадает осадок:
2NaOH+ CuSO4 = Cu(OH)2↓ + Na2SO4
Реагируют с металлами, образующими амфотерные оксиды и гидроксиды:
2NaOH + Zn +2H2O = Na2[Zn(OH)4] + Н2
Слайд 20Нерастворимые в воде основания
Реагируют с кислотами:
Mg(OH)2 + 2HNO3 = Mg(NO3)2 +2H2O
Разлагаются при
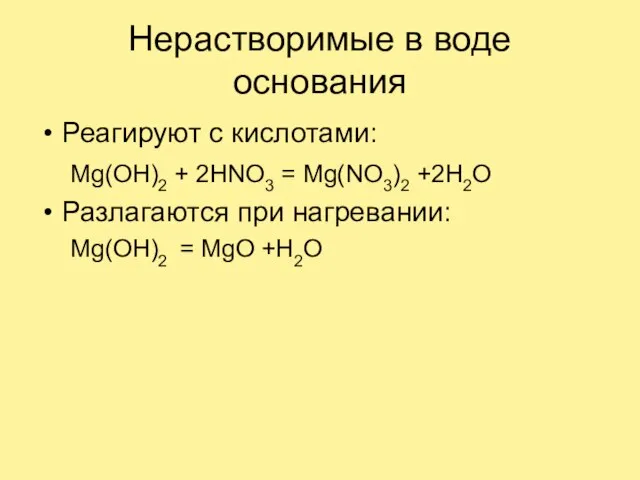
нагревании:
Mg(OH)2 = MgO +H2O
Слайд 21Кислотные гидроксиды – кислородсодержащие кислоты
Реагируют с основаниями:
KOH + HNO3 = KNO3 +

H2O
Реагируют с основными оксидами:
MgO + H2SO4 = MgSO4 + H2O
Реагируют с металлами, стоящими в ряду напряжений до водорода:
Mg + H2SO4 = MgSO4 + H2
Реагируют с солями:
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2
Слайд 22Амфотерные гидроксиды
Реагируют с кислотами, проявляя свойства оснований:
Al(OH)3 + 3HCl = AlCl3 +

3H2O
Реагируют со щелочами, проявляя свойства кислот:
Al(OH)3 + NaOH = Na[Al(OH)4]
Слайд 23Гидроксид натрия не взаимодействует с
1)CuCl2
2)SO2
3)PbS
4)HNO3

Слайд 24Гидроксид натрия реагирует со всеми веществами ряда:
1)Zn, Na 2CO3, CuO
2)CO2, H3 PO4

CuO
3)S O3, H3PO 4, AI2O3
4)SO3, MgO, H3PO4,
Слайд 25Гидроксид калия реагирует со всеми веществами группы
1)Zn, SiO2, H2O
2)HNO3, Na2CO3, Mg
3)CuSO4, SO3,

H3PO4
4)CuO, Cа(OH)2, N2O5
Слайд 26В ряду превращений:
CuO→CuCl2→Cu(OH)2 вещества X и Y соответственно
1)НСl и

NaOH
2)HCl и Fe(OH)3
3)NaCl и Н2O
4)Cl2 и H2O
Слайд 27В ряду превращений
NaOH→Na 2CO3→CO2
веществa X и Y соответственно
1)Н2CO3
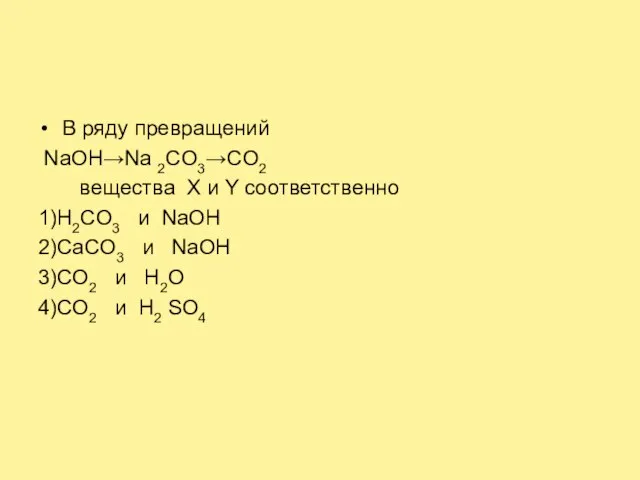
и NaOH
2)CaCO3 и NaOH
3)CO2 и H2O
4)CO2 и H2 SO4
Слайд 28Каждое из перечисленных веществ: CuCl2, SO3, H3PO4, Zn(OH)2
реагирует с
1)серной кислотой 2)водой

3)гидроксидом натрия 4)оксидом углерода(VI)
Слайд 29 При действии избытка раствора гидроксида натрия на раствор сульфата цинка образуется
1)

ZnO
2) Zn(OH)2
3) Na2ZnO2
4)Na2[Zn(OH)4]




























 Асель на связи
Асель на связи Источники права
Источники права Публичный доклад
Публичный доклад Создание коллекции одежды по мотивам архитектуры Нью-Йорка, стиль арт-деко и коллекция по мотивам народного костюма
Создание коллекции одежды по мотивам архитектуры Нью-Йорка, стиль арт-деко и коллекция по мотивам народного костюма Analiz_FKR_Lukyanchikova_A_V_323gr
Analiz_FKR_Lukyanchikova_A_V_323gr «Пилотный проекторганизации сетевой службы интеграционных консультантов для инвалидов в городе Москве»
«Пилотный проекторганизации сетевой службы интеграционных консультантов для инвалидов в городе Москве» Grandfos
Grandfos Как сварить мыло
Как сварить мыло Программа весеннего Дня Открытых Дверей
Программа весеннего Дня Открытых Дверей Методика работы над простой задачей
Методика работы над простой задачей Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Чешская Нефильтрованная Велоосень 2013
Чешская Нефильтрованная Велоосень 2013 Введение в грамматику японского языка???????
Введение в грамматику японского языка??????? Презентация на тему Клятва пятиклассника
Презентация на тему Клятва пятиклассника  Конфликты и пути их преодоления
Конфликты и пути их преодоления Типовые неисправности различных видов подвижного состава
Типовые неисправности различных видов подвижного состава Труд
Труд Управление качеством
Управление качеством Презентация для проекта
Презентация для проекта Ваш ребенок идет в школу
Ваш ребенок идет в школу Антимонопольное регулирование на оптовом рынке электроэнергии
Антимонопольное регулирование на оптовом рынке электроэнергии Биотехнологии и прогресс человечества
Биотехнологии и прогресс человечества Размножение гидроидных. Регенерация
Размножение гидроидных. Регенерация Презентация (2)
Презентация (2) Стивен Кинг
Стивен Кинг Библиотеки Урмарского района в зеркале цифр и информации (2005 год)
Библиотеки Урмарского района в зеркале цифр и информации (2005 год) Презентация на тему Шри-Ланка
Презентация на тему Шри-Ланка  Герой России
Герой России