Слайд 2Стани твердих речовин
За внутрішньою будовою і фізичними властивостями розрізняють два стани твердих
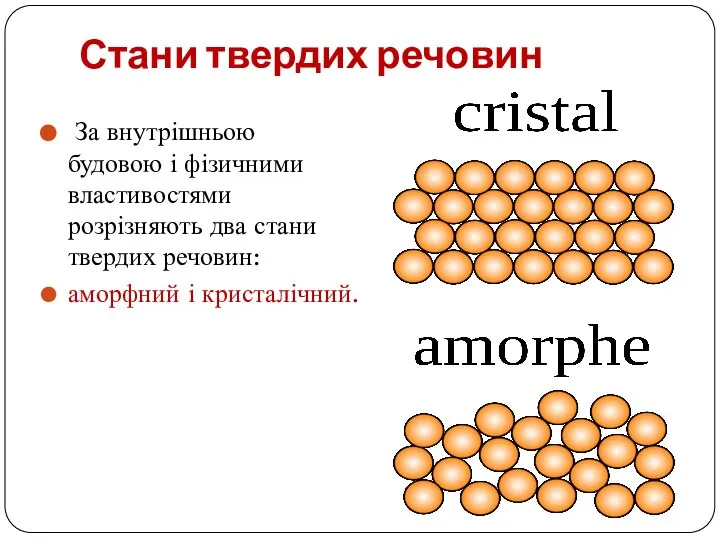
речовин:
аморфний і кристалічний.
Слайд 3Кристалічні речовини:
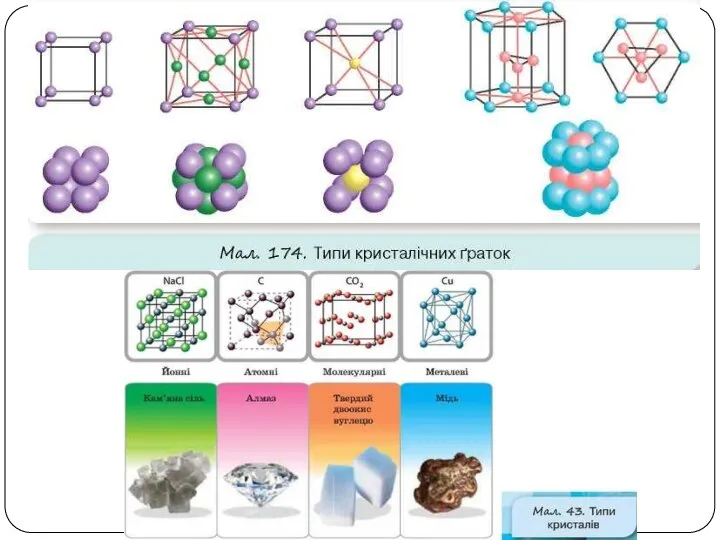
• структурні одиниці розташовані в чіткому порядку — утворюють кристалічні ґратки;
•

мають певну температуру плавлення;
• утворюють кристали певної форми;
• у разі руйнування кристалічної речовини кристали розпадаються на окремі шматочки, кожен із яких зберігає хоча б частково форму початкового кристала;
• приклади речовин: природні мінерали, кухонна сіль, цукор.
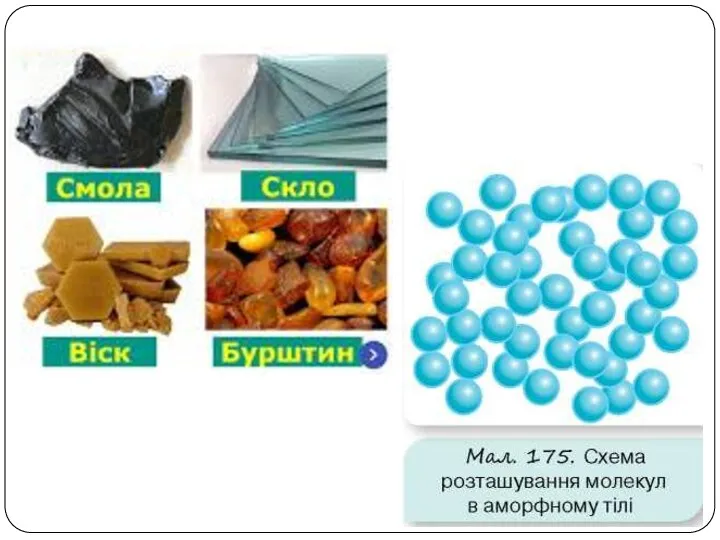
Слайд 5Аморфні речовини:
• не мають чіткої просторової структури — структурні одиниці розташовані невпорядковано;
•

плавляться в певному діапазоні температур;
• за нагрівання спочатку розм’якшуються;
• у разі руйнування утворюються уламки неправильної форми, зазвичай із нерівною поверхнею країв сколу;
• приклади речовин: скло, смоли, бурштин, застиглі лаки, клеї, каучук.
Слайд 8Взаємоперетворення:
За певних умов речовина може з кристалічної перетворюватися на аморфну, і навпаки.

Звичайне скло — аморфна речовина, але з часом силіцій(IV) оксид у його складі набуває кристалічної форми. Через це старі склянки під час наливання в них окропу лопаються набагато частіше, ніж нові. Цукор — кристалічна речовина. Але якщо його розплавити та швидко охолодити, то він застигає в аморфному стані. З такого цукру можна виготовляти льодяники, карамельки тощо.
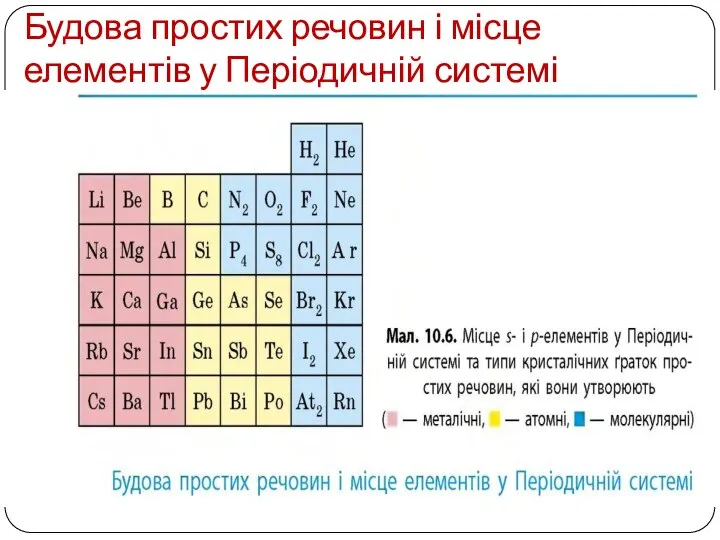
Слайд 9Будова простих речовин і місце елементів у Періодичній системі






 ФЗ-390. Ежегодный план проведения плановых проверок
ФЗ-390. Ежегодный план проведения плановых проверок Нормативная база деятельности учителя математики
Нормативная база деятельности учителя математики ГИПОДИНАМИЯ – БОЛЕЗНЬ 21 века
ГИПОДИНАМИЯ – БОЛЕЗНЬ 21 века Джон Уи́льям Уо́терхаус
Джон Уи́льям Уо́терхаус Растениеводство в нашем крае
Растениеводство в нашем крае Магнітне поле. Взаємодія магнітів
Магнітне поле. Взаємодія магнітів Государственные и народные праздники
Государственные и народные праздники Bloemenpracht in Gent
Bloemenpracht in Gent Отчет по факту разрушения капотов автомобилей Урал Next
Отчет по факту разрушения капотов автомобилей Урал Next Трудности в обучении
Трудности в обучении Презентация на тему Инфракрасное излучение
Презентация на тему Инфракрасное излучение  Город сквозь времена и страны. Образно-стилевой язык архитектуры прошлого
Город сквозь времена и страны. Образно-стилевой язык архитектуры прошлого Базовый курс по электротехнике
Базовый курс по электротехнике Искусство иконописи Византии
Искусство иконописи Византии Работа с окнами в Windows
Работа с окнами в Windows Бухгалтерский учет. (Лекция 4)
Бухгалтерский учет. (Лекция 4) Игра к 70 летию Костромской области
Игра к 70 летию Костромской области CS Sape Master: универсальный клиент для биржи SAPE
CS Sape Master: универсальный клиент для биржи SAPE Һөйләмдең баш һәм эйәрсән киҫәктәре
Һөйләмдең баш һәм эйәрсән киҫәктәре Презентация на тему Превращение энергии
Презентация на тему Превращение энергии Развивающие задачи
Развивающие задачи проблемы
проблемы Лексика-раздел науки о языке
Лексика-раздел науки о языке Профилактика кризисных состояний у детей и подростков в образовательных организациях
Профилактика кризисных состояний у детей и подростков в образовательных организациях Моление Даниила Заточника
Моление Даниила Заточника АМК
АМК Филиал Политеха – территория успеха. Первый выпуск кафедры экономики БФ ПГТУ ЭиУ-93 (1993-1998)
Филиал Политеха – территория успеха. Первый выпуск кафедры экономики БФ ПГТУ ЭиУ-93 (1993-1998) Презентация на тему Опасные ситуации на дорогах и тротуарах
Презентация на тему Опасные ситуации на дорогах и тротуарах