Содержание
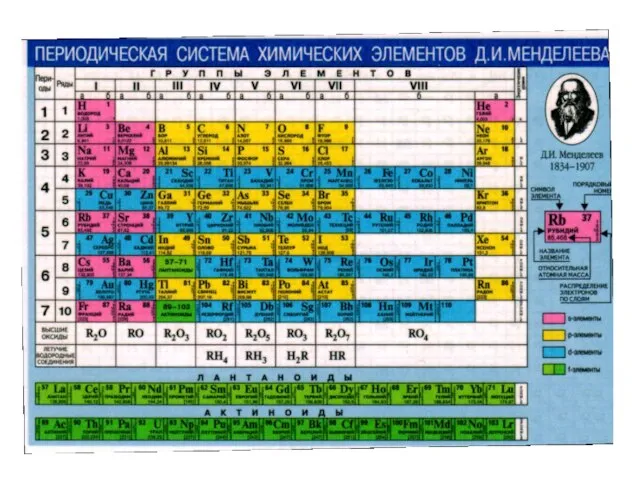
- 3. Общность свойств металлов 1) как правило, атомы металлов имеют небольшое число электронов на внешнем уровне электронной
- 4. Отличает металлическую связь от ковалентной отсутствие направленности связи и меньшая прочность. Энергия металлической связи в 3÷4
- 5. Мерой энергии связи – является величина энергии атомизации металла Энергия атомизации (Еатом.) – это та энергия,
- 6. Температура плавления – мера прочности связи в кристаллической решетке металла
- 7. Металлы – понятие химическое и физическое одновременно. В химическом аспекте металл это донор электронов (восстановитель):
- 8. а) высокая тепло-электропроводность; б) пластичность; в) металлический блеск (связанный с высокой отражательной способностью и непрозрачностью). В
- 9. Диаграмма состояния металлов в координатах (P,T)
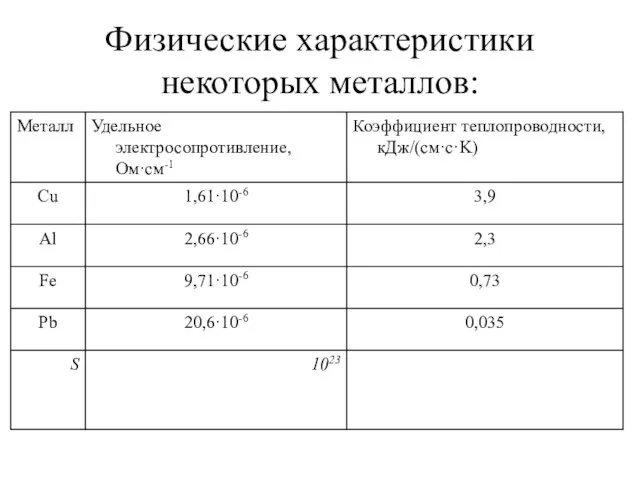
- 10. Физические характеристики некоторых металлов:
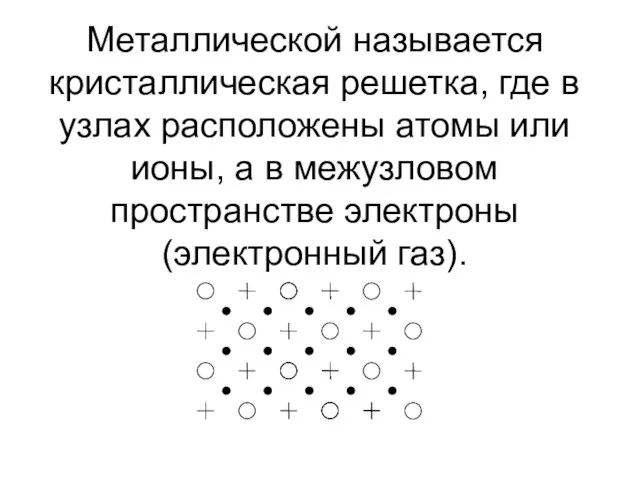
- 11. Металлической называется кристаллическая решетка, где в узлах расположены атомы или ионы, а в межузловом пространстве электроны
- 12. О свободе электронов: электроны выбиваются с поверхности металла: а) при облучении металлов ультрафиолетом – фотоэффект Столетова;
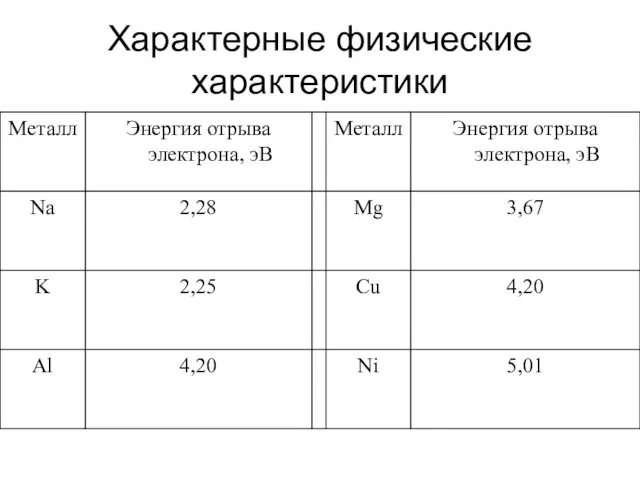
- 13. Характерные физические характеристики
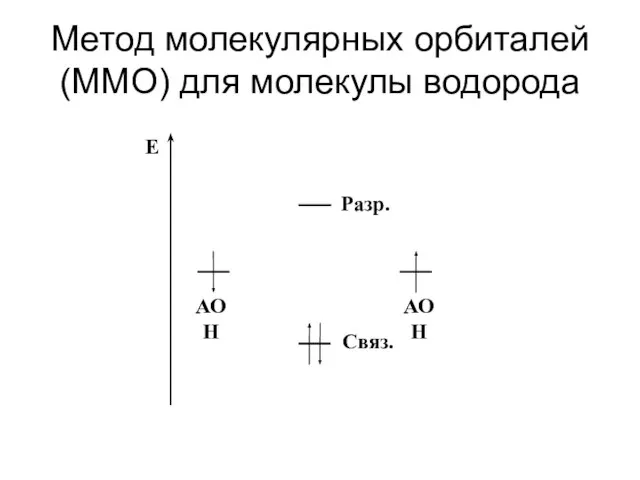
- 14. Метод молекулярных орбиталей (ММО) для молекулы водорода
- 15. При взаимодействии n – атомов зона разрешенных состояний расширяется, уменьшается разность между дискретными уровнями.
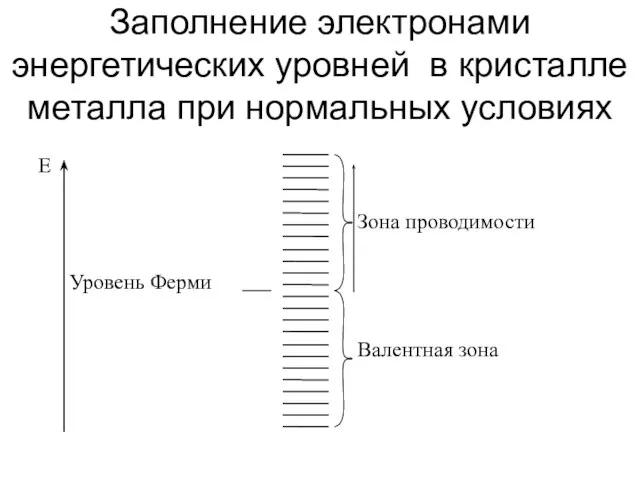
- 16. Заполнение электронами энергетических уровней в кристалле металла при нормальных условиях
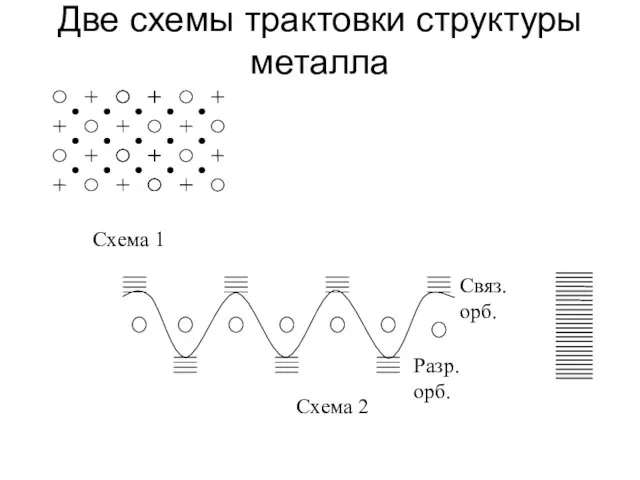
- 17. Две схемы трактовки структуры металла
- 18. Электронная проводимость Кристаллов простых веществ
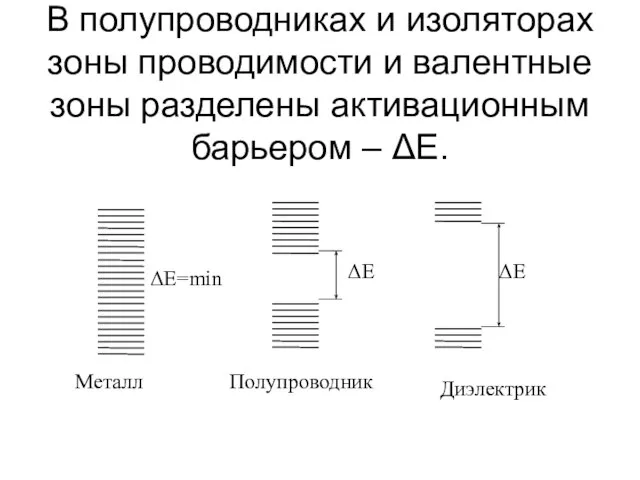
- 19. В полупроводниках и изоляторах зоны проводимости и валентные зоны разделены активационным барьером – ΔE.
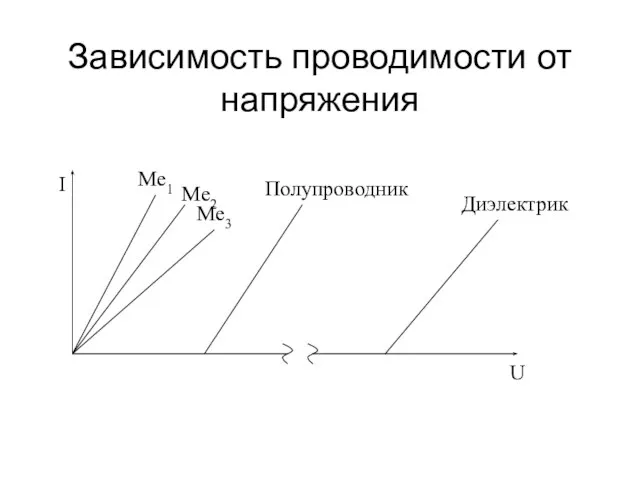
- 20. Зависимость проводимости от напряжения
- 21. Получение металлов из руд. Различают: самородные металлы (Au, Ag, Hg, Cu, Pt); металлы в связанном состоянии
- 22. Остальные металлы получают химической переработкой руд следующими методами: Пирометаллургия – получение металлов при высокой температуре с
- 25. Применение металлов. Металлы применяют как конструкционные материалы и в виде комбинированных материалов (железобетон, металлокерамика, металлопластика и
- 26. Влияние чистоты металла на применение металлы высокой чистоты (для каждого металла своя степень чистоты) используются в
- 27. Сплавы. Выделяют сплавы трех модификаций: сплав – механическая смесь кристаллитов (простая эвтектика); твердые растворы; сплавы с
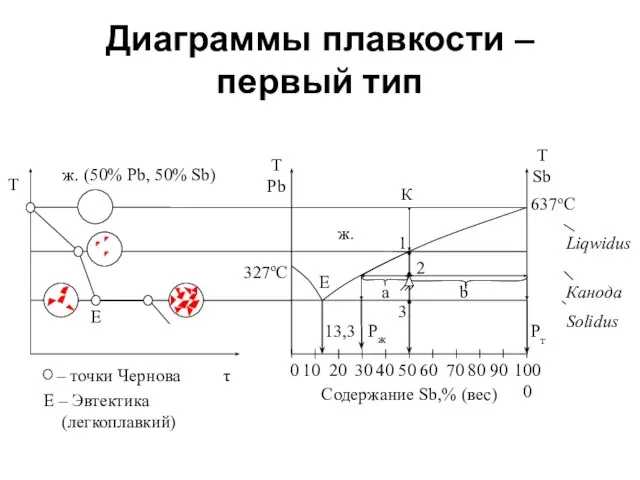
- 28. Диаграммы плавкости – первый тип
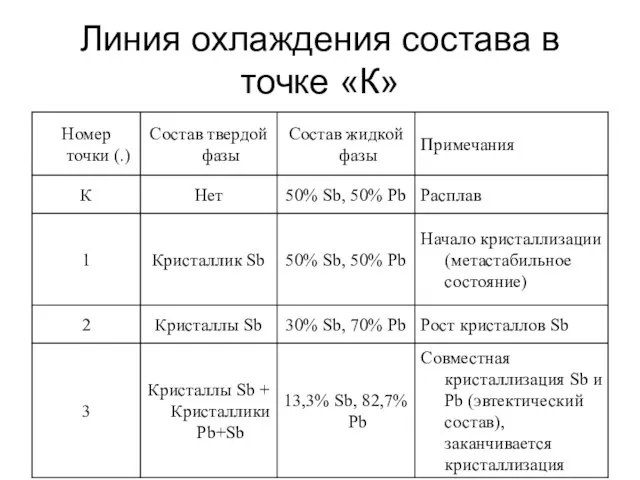
- 29. Линия охлаждения состава в точке «К»
- 30. Для точки 2 справедливо соотношение: – правило рычага
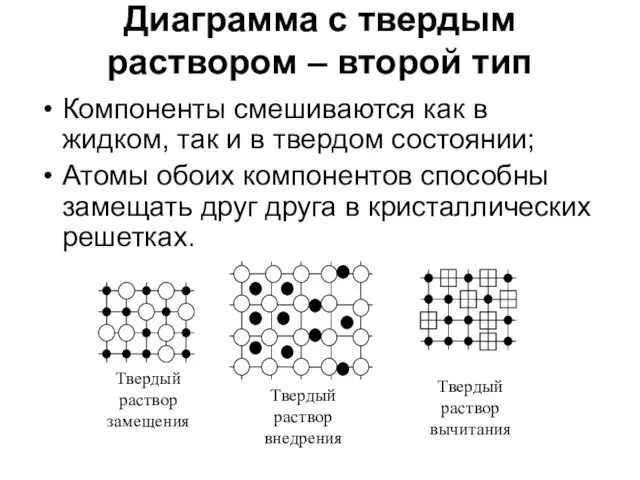
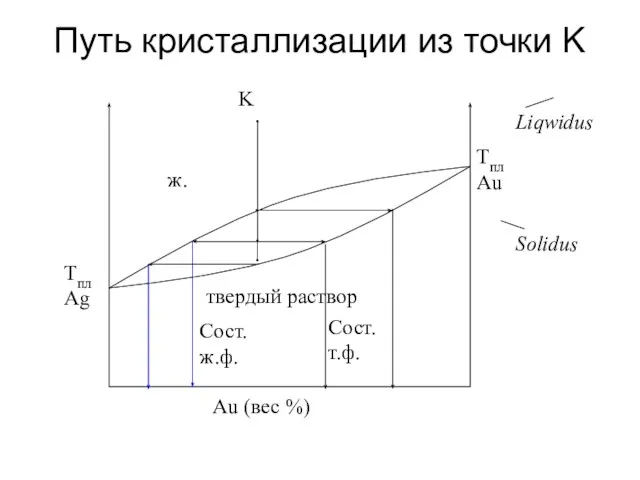
- 31. Диаграмма с твердым раствором – второй тип Компоненты смешиваются как в жидком, так и в твердом
- 32. Путь кристаллизации из точки K
- 33. Условие образования твердых растворов: компоненты должны иметь одинаковые по типу кристаллические решетки; различие в атомных размерах
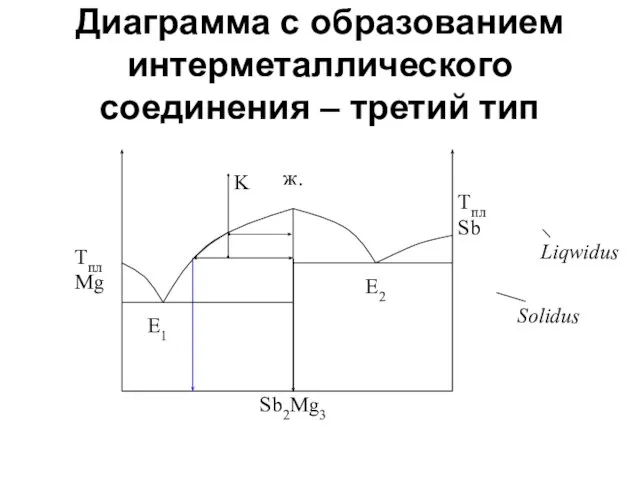
- 34. Диаграмма с образованием интерметаллического соединения – третий тип
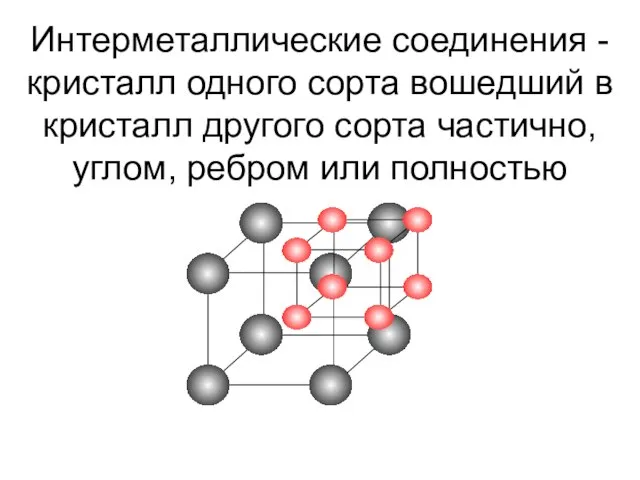
- 35. Характерные особенности интерметаллического соединения атомы в решетке располагаются, упорядочено, т.е. атомы одного элемента закономерно и в
- 36. Интерметаллические соединения - кристалл одного сорта вошедший в кристалл другого сорта частично, углом, ребром или полностью
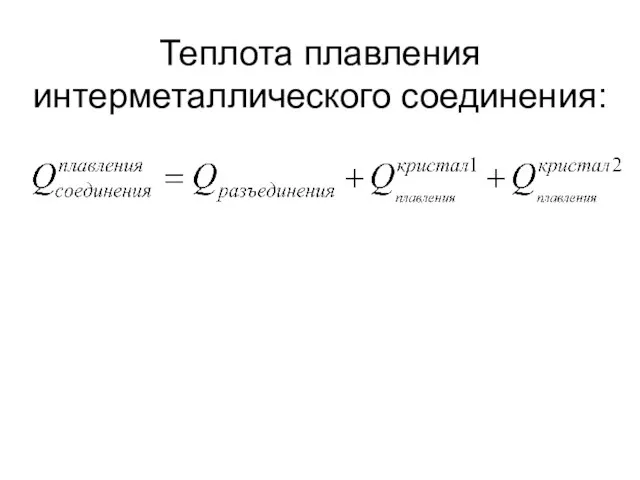
- 37. Теплота плавления интерметаллического соединения:
- 38. Химические свойства металлов s-,p-,d- элементов Для получения металлов использовался ряд активности металлов Бекетова: Легкость разряда катиона
- 40. Скачать презентацию





















 Service_Training_safety
Service_Training_safety Предыстория информатики
Предыстория информатики Презентация на тему Здоровая нация – счастливая Россия 9-11 класс
Презентация на тему Здоровая нация – счастливая Россия 9-11 класс Библиотека виртуальных загадок и головоломок
Библиотека виртуальных загадок и головоломок Правописание корней с чередованием Е-И
Правописание корней с чередованием Е-И «О проводимой в Ростовской области профилактике социального сиротства среди несовершеннолетних»
«О проводимой в Ростовской области профилактике социального сиротства среди несовершеннолетних» Презентация на тему Как отличить глагол от других частей речи?
Презентация на тему Как отличить глагол от других частей речи? Построение урока на основе системно-деятельностного подхода
Построение урока на основе системно-деятельностного подхода ОРУЖИЕ ПОБЕДЫ
ОРУЖИЕ ПОБЕДЫ Кормление кроликов
Кормление кроликов Подход к инвентаризации углеродных выбросов и методология расчета углеродного следа для Олимпиады Сочи-2014
Подход к инвентаризации углеродных выбросов и методология расчета углеродного следа для Олимпиады Сочи-2014 AZ CLUB 2019
AZ CLUB 2019 Модернизация и развитие участка волочения тугоплавких металлов и сплавов
Модернизация и развитие участка волочения тугоплавких металлов и сплавов Несуществующие животные
Несуществующие животные Выборы в государственную думу РФ 2021г
Выборы в государственную думу РФ 2021г Презентация на тему Организация деятельности по формированию смыслового чтения в образовательном процессе посредством элементо
Презентация на тему Организация деятельности по формированию смыслового чтения в образовательном процессе посредством элементо Древние образы и символы в народном искусстве.Часть 1
Древние образы и символы в народном искусстве.Часть 1 Презентация на тему Творчество Чайковского
Презентация на тему Творчество Чайковского  20170601_prezentatsiya_microsoft_powerpoint
20170601_prezentatsiya_microsoft_powerpoint ВПР общ за 7 кл много
ВПР общ за 7 кл много Летний пейзаж карандашами
Летний пейзаж карандашами Презентация на тему Растения – производители. («Окружающий мир» А.А.Вахрушев и др., 3 класс)
Презентация на тему Растения – производители. («Окружающий мир» А.А.Вахрушев и др., 3 класс) Правила отношений
Правила отношений Настройка экспозиции в фотоаппарате
Настройка экспозиции в фотоаппарате Сочинение по художественному тексту в формате ЕГЭ(на примере текста А.П. Владимирова «Косуля»)
Сочинение по художественному тексту в формате ЕГЭ(на примере текста А.П. Владимирова «Косуля») СредаПромышленной Разработки Программного Обеспечения
СредаПромышленной Разработки Программного Обеспечения ВЫДАЮЩИЕСЯ ЛЮДИ КАФЕДРЫ
ВЫДАЮЩИЕСЯ ЛЮДИ КАФЕДРЫ Электронная почта
Электронная почта