Содержание
- 2. 1. Катион – это: а) ион меди; б) атом серы; в) ион серы; г) атом меди.
- 3. 1. Катион – это: а) ион меди; б) атом серы; в) ион серы; г) атом меди.
- 4. Расположить в порядке увеличения силы электролита: HF K=7.10-4 HCN K=8.10-10 HNO2 K=5,1.10-4 NH4OH K=2.10-5
- 5. Расположить в порядке увеличения кислотных свойств: H2O HCl H2 SO3 NH3
- 6. Расположить в порядке увеличения основных свойств: NH3 C6H5-NH2 C6H5-NH-C6H5 CH3-NH2
- 7. Укажи, допущены ли ошибки в тексте: 1. На процесс диссоциации влияет растворение или расплавление вещества. 2.
- 8. Укажи, допущены ли ошибки в тексте: 1. На процесс диссоциации влияет растворение или расплавление вещества. 2.
- 10. Скачать презентацию
Слайд 21. Катион – это:
а) ион меди; б) атом серы; в) ион серы;
1. Катион – это: а) ион меди; б) атом серы; в) ион серы;

г) атом меди.
2. Анион – это: а) ион натрия; б) ион аммония; в) карбонат-ион; г) ион водорода.
3. Окраска фенолфталеина в растворе, полученном при взаимодействии калия с водой: а) синяя; б) малиновая; в) желтая; г) бесцветная.
4. Формула вещества, образующего при диссоциации сульфат-ионы: а) Na2S; б) SO3; в) Na2SO4; г) BaSO4.
5. Формула вещества, образующего при диссоциации сульфат-ионы и ионы водорода: а) КНS; б) КНSO3; в) Na2S; г) NaHSO4.
2. Анион – это: а) ион натрия; б) ион аммония; в) карбонат-ион; г) ион водорода.
3. Окраска фенолфталеина в растворе, полученном при взаимодействии калия с водой: а) синяя; б) малиновая; в) желтая; г) бесцветная.
4. Формула вещества, образующего при диссоциации сульфат-ионы: а) Na2S; б) SO3; в) Na2SO4; г) BaSO4.
5. Формула вещества, образующего при диссоциации сульфат-ионы и ионы водорода: а) КНS; б) КНSO3; в) Na2S; г) NaHSO4.
Выберите правильные ответы:
Слайд 31. Катион – это:
а) ион меди; б) атом серы; в) ион серы;
1. Катион – это: а) ион меди; б) атом серы; в) ион серы;

г) атом меди.
2. Анион – это: а) ион натрия; б) ион аммония; в) карбонат-ион; г) ион водорода.
3. Окраска фенолфталеина в растворе, полученном при взаимодействии калия с водой: а) синяя; б) малиновая; в) желтая; г) бесцветная.
4. Формула вещества, образующего при диссоциации сульфат-ионы: а) Na2S; б) SO3; в) Na2SO4; г) BaSO4.
5. Формула вещества, образующего при диссоциации сульфат-ионы и ионы водорода: а) КНS; б) КНSO3; в) Na2S; г) NaHSO4.
2. Анион – это: а) ион натрия; б) ион аммония; в) карбонат-ион; г) ион водорода.
3. Окраска фенолфталеина в растворе, полученном при взаимодействии калия с водой: а) синяя; б) малиновая; в) желтая; г) бесцветная.
4. Формула вещества, образующего при диссоциации сульфат-ионы: а) Na2S; б) SO3; в) Na2SO4; г) BaSO4.
5. Формула вещества, образующего при диссоциации сульфат-ионы и ионы водорода: а) КНS; б) КНSO3; в) Na2S; г) NaHSO4.
Выберите правильные ответы:
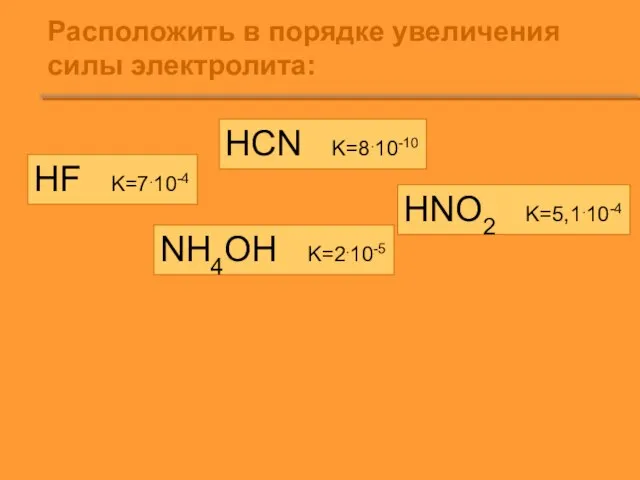
Слайд 4Расположить в порядке увеличения силы электролита:
HF K=7.10-4
HCN K=8.10-10
HNO2 K=5,1.10-4
NH4OH K=2.10-5
Расположить в порядке увеличения силы электролита:
HF K=7.10-4
HCN K=8.10-10
HNO2 K=5,1.10-4
NH4OH K=2.10-5
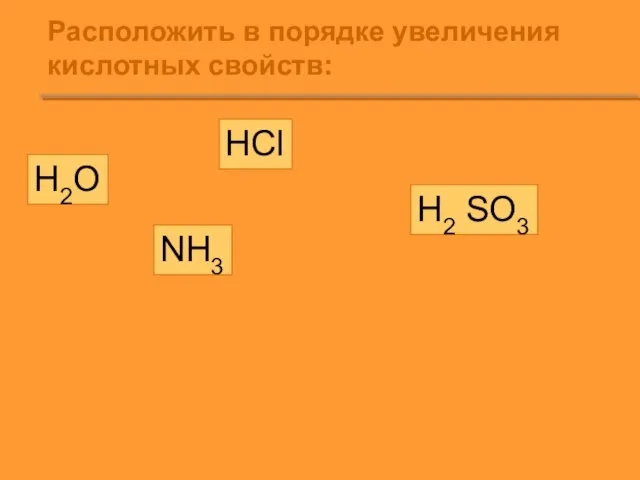
Слайд 5Расположить в порядке увеличения кислотных свойств:
H2O
HCl
H2 SO3
NH3
Расположить в порядке увеличения кислотных свойств:
H2O
HCl
H2 SO3
NH3
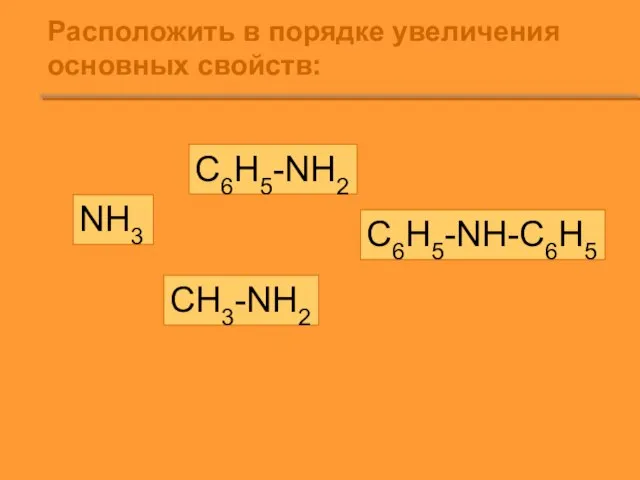
Слайд 6Расположить в порядке увеличения основных свойств:
NH3
C6H5-NH2
C6H5-NH-C6H5
CH3-NH2
Расположить в порядке увеличения основных свойств:
NH3
C6H5-NH2
C6H5-NH-C6H5
CH3-NH2
Слайд 7Укажи, допущены ли ошибки в тексте:
1. На процесс диссоциации влияет растворение или
Укажи, допущены ли ошибки в тексте:
1. На процесс диссоциации влияет растворение или

расплавление вещества.
2. Сернистая кислота – слабая, потому что она распадается на сернистый газ и воду.
3. Основность кислоты не всегда совпадает с числом не всегда совпадает с числом атомов водорода в ней.
4. Все щелочи – сильные электролиты.
5. Константа диссоциации вещества по первой ступени всегда больше, чем по второй.
6. Степень диссоциации зависит от температуры и концентрации электролита.
7. Диссоциация электролитов – обратимый процесс.
8. Это реакция ионного обмена: 2КОН+SiO2 = K2SiO3 + H2O.
9. Отражает ли сущность реакции Cu(OH)2 + 2 HCl = CuCl2 + 2H2O сокращенное ионное уравнение: H+ + OH- = H2O.
10. Реакции ионного обмена идут до конца (практически необратимо), если ионы, соединяясь друг с другом, образуют нерастворимые, малодиссоциирующие и газообразные вещества.
2. Сернистая кислота – слабая, потому что она распадается на сернистый газ и воду.
3. Основность кислоты не всегда совпадает с числом не всегда совпадает с числом атомов водорода в ней.
4. Все щелочи – сильные электролиты.
5. Константа диссоциации вещества по первой ступени всегда больше, чем по второй.
6. Степень диссоциации зависит от температуры и концентрации электролита.
7. Диссоциация электролитов – обратимый процесс.
8. Это реакция ионного обмена: 2КОН+SiO2 = K2SiO3 + H2O.
9. Отражает ли сущность реакции Cu(OH)2 + 2 HCl = CuCl2 + 2H2O сокращенное ионное уравнение: H+ + OH- = H2O.
10. Реакции ионного обмена идут до конца (практически необратимо), если ионы, соединяясь друг с другом, образуют нерастворимые, малодиссоциирующие и газообразные вещества.
Слайд 8Укажи, допущены ли ошибки в тексте:
1. На процесс диссоциации влияет растворение или
Укажи, допущены ли ошибки в тексте:
1. На процесс диссоциации влияет растворение или

расплавление вещества.
2. Сернистая кислота – слабая, потому что она распадается на сернистый газ и воду.
3. Основность кислоты не всегда совпадает с числом атомов водорода в ней.
4. Все щелочи – сильные электролиты.
5. Константа диссоциации слабой кислоты по первой ступени всегда больше, чем по второй.
6. Степень диссоциации зависит от температуры и концентрации электролита.
7. Диссоциация электролитов – обратимый процесс.
8. Это реакция ионного обмена: 2КОН+SiO2 = K2SiO3 + H2O.
9. Отражает ли сущность реакции Cu(OH)2 + 2 HCl = CuCl2 + 2H2O сокращенное ионное уравнение: H+ + OH- = H2O.
10. Реакции ионного обмена идут до конца (практически необратимо), если ионы, соединяясь друг с другом, образуют нерастворимые, малодиссоциирующие и газообразные вещества.
2. Сернистая кислота – слабая, потому что она распадается на сернистый газ и воду.
3. Основность кислоты не всегда совпадает с числом атомов водорода в ней.
4. Все щелочи – сильные электролиты.
5. Константа диссоциации слабой кислоты по первой ступени всегда больше, чем по второй.
6. Степень диссоциации зависит от температуры и концентрации электролита.
7. Диссоциация электролитов – обратимый процесс.
8. Это реакция ионного обмена: 2КОН+SiO2 = K2SiO3 + H2O.
9. Отражает ли сущность реакции Cu(OH)2 + 2 HCl = CuCl2 + 2H2O сокращенное ионное уравнение: H+ + OH- = H2O.
10. Реакции ионного обмена идут до конца (практически необратимо), если ионы, соединяясь друг с другом, образуют нерастворимые, малодиссоциирующие и газообразные вещества.
- Предыдущая
Hotpoint|Ariston FS ЛегеднаСледующая -
Плавание судов Террористические организации
Террористические организации Викторина по русским народным сказкам и сказкам А.Пушкина
Викторина по русским народным сказкам и сказкам А.Пушкина Какой я
Какой я Развитие психики и сознания
Развитие психики и сознания Рони Ритшель
Рони Ритшель Концептуальное основание современного В2В маркетинга. Концепция маркетинга взаимодействия
Концептуальное основание современного В2В маркетинга. Концепция маркетинга взаимодействия Защита информации от несанкционированного доступа
Защита информации от несанкционированного доступа Стратегический менеджмент в условиях спонтанных изменений
Стратегический менеджмент в условиях спонтанных изменений Я - личный помощник. Измени себя и свою жизнь
Я - личный помощник. Измени себя и свою жизнь Зодчество Древней Греции.
Зодчество Древней Греции. Презентация на тему Сущность и основные понятия этики. Мораль. Типы этики
Презентация на тему Сущность и основные понятия этики. Мораль. Типы этики  Мы познакомимся с чудной страной, Не признающий застой и покой. В этой стране можем деньги вложить И производство свое запустить В
Мы познакомимся с чудной страной, Не признающий застой и покой. В этой стране можем деньги вложить И производство свое запустить В  Карликовая игрунка или пальчиковая обезьяна (Finger Monkey)
Карликовая игрунка или пальчиковая обезьяна (Finger Monkey) ТЕМА 3
ТЕМА 3 МАТЕРИНСТВО И ОТЦОВСТВО
МАТЕРИНСТВО И ОТЦОВСТВО Глагол. Урок-обобщение
Глагол. Урок-обобщение Проект 3: Развитие инновационной деятельности в Технологическом институте, г. Эрдэнэт. - презентация
Проект 3: Развитие инновационной деятельности в Технологическом институте, г. Эрдэнэт. - презентация Люблю берёзку русскую
Люблю берёзку русскую Основные причины психологического бесплодия. Онлайн курс по подготовке к ЭКО
Основные причины психологического бесплодия. Онлайн курс по подготовке к ЭКО Фотоклуб Перспектива
Фотоклуб Перспектива Die Aufgabe “d”
Die Aufgabe “d” Практика в Горьковской дирекции по ремонту пути, подработка в период летних каникул
Практика в Горьковской дирекции по ремонту пути, подработка в период летних каникул Основы грузовой и коммерческой работы
Основы грузовой и коммерческой работы Молодежный инновационный конвент способствует поддержке и повышению престижа молодого ученого в обществе Комитет по молодежной
Молодежный инновационный конвент способствует поддержке и повышению престижа молодого ученого в обществе Комитет по молодежной  13 признаков учителя
13 признаков учителя Тема: Повесть Н.В.Гоголя «Тарас Бульба». Отец и сыновья. Характеры главных героев
Тема: Повесть Н.В.Гоголя «Тарас Бульба». Отец и сыновья. Характеры главных героев Термические ожоги (5 класс)
Термические ожоги (5 класс) Культура Древнего Востока Выполнила ученица 10 класса «В» Коньшина Настя
Культура Древнего Востока Выполнила ученица 10 класса «В» Коньшина Настя