Очень древний я металл, Счет столетьям потерял; Наблюдатель египтянин имя дал «небесный камень» Был нескромным я в меру, Тысячи лет
Содержание
- 2. Очень древний я металл, Счет столетьям потерял; Наблюдатель египтянин имя дал «небесный камень» Был нескромным я
- 3. ЖЕЛЕЗО
- 4. Технологическая карта
- 5. Историческая справка о железе Слово «железо» произошло от санскритских слов «джальжа» (металл, руда) или «жель» (блистать,
- 6. Изотопы железа
- 7. Строение атома железа. Fe (железо) Порядковый номер: 26 Период: IV Группа: VIII Подгруппа: В Электронное строение
- 8. Распространение в природе Содержание в земной коре. В земной коре содержится 4,65%(по массе) железа. По распространенности
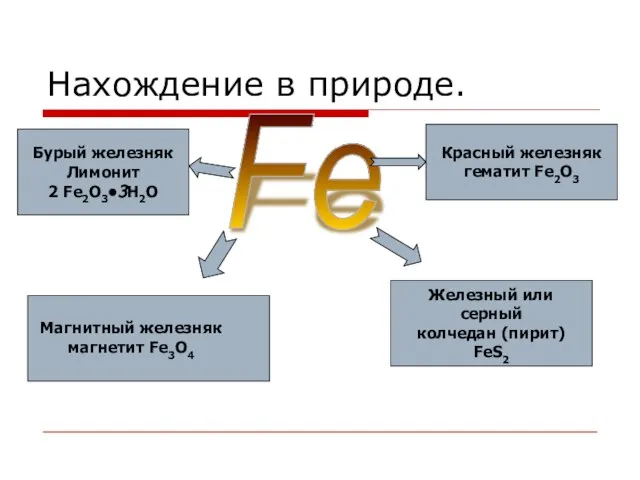
- 9. Нахождение в природе. Fe Магнитный железняк магнетит Fe3O4 Красный железняк гематит Fe2O3 Бурый железняк Лимонит 2
- 10. Пирит Химическая формула FeS2 Сингония:кубическая Удельный вес: (г/см3)5—5,2 Цвет:соломенно-желтый, иногда с побежалостью. Цвет, черты:зеленовато-черная Блеск:металлический Излом:раковистый
- 11. Сидерит Химическая формула FеСО3 Сингония:тригональная Удельный вес:(г/см3)3,7—3,9 Цвет:желтый, желтовато-серый, буровато-серый, буровато-желтый, черный Цвет, черты:бесцветная, у измененных
- 12. Гематит Химическая формула Fе2O3 Сингония:тригональная Удельный вес: (г/см3)5,3 Цвет:от черного в крупнокристаллических агрегатах до ярко-красного в
- 13. Магнетит Химическая формула FеFе2O4 Сингония:кубическая Удельный вес: (г/см3)5,2 Цвет:железо-черный, иногда с синей побежалостью Цвет, черты:черная Блеск:металлический
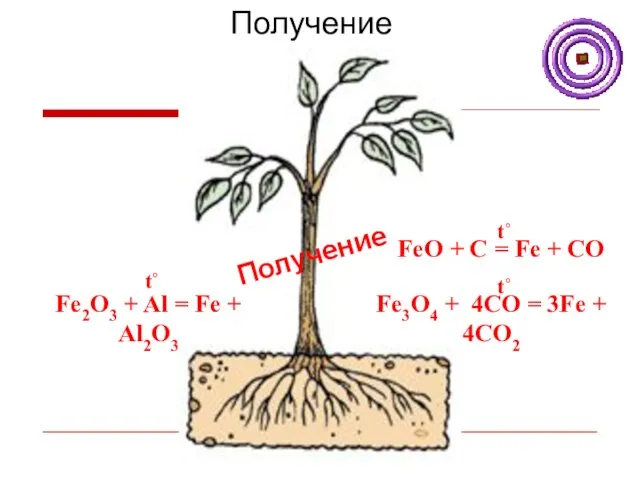
- 14. Получение железа FeO + C = Fe + CO t˚ Fe3O4 + 4CO = 3Fe +
- 15. Физические свойства Железо - сравнительно мягкий ковкий серебристо-серый металл. Температура плавления – 1535 0С Температура кипения
- 16. Химические свойства железа 1. Железо реагирует с неметаллами: Fe + S = FeS При нагревании до
- 17. Химические свойства железа 2. Железо реагирует с кислотами. Fe+H2SO4=FeSO4+H2 Fe +2 HCl = FeCl2 + H2
- 18. Химические свойства железа. 3. Реагирует с растворами солей металла согласно электрохимическому ряду напряжений металлов. Fe +
- 19. Биологическая роль железа: Железо — наиболее распространенный в организме d-элемент. В организме человека его содержится около
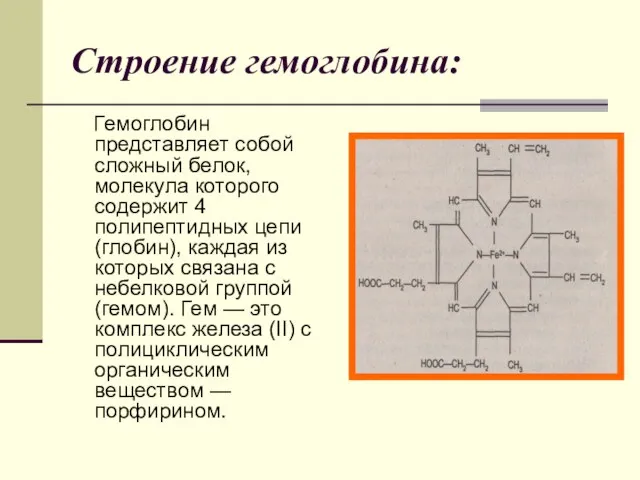
- 20. Строение гемоглобина: Гемоглобин представляет собой сложный белок, молекула которого содержит 4 полипептидных цепи (глобин), каждая из
- 21. Ферментативная роль железа: Железо входит также в состав большой группы ферментов, катализирующих процесс переноса электронов в
- 22. Применение железа и его соединений в медицине: Железный купорос FеSО4 • 7Н2О используют при лечении анемии,
- 23. Применение железа: «Чистое железо способно быстро намагничиваться и размагничиваться, поэтому его применяют для изготовления сердечников, трансфо-,
- 24. Технологическая карта
- 25. Химический диктант 1. Железо – это активный щелочной металл 2. Железо легко куется. 3. Железо взаимодействует
- 27. Скачать презентацию





















 Автономные канализации TopolWater
Автономные канализации TopolWater Российские Олимпиады 1913 и 1914 годов
Российские Олимпиады 1913 и 1914 годов Первые проблемы подросткового возраста
Первые проблемы подросткового возраста Олимпиадное движение:итоги, проблемы, перспективы
Олимпиадное движение:итоги, проблемы, перспективы Орфограммы в корне слова
Орфограммы в корне слова VK group: сообщество инфобизнесменов
VK group: сообщество инфобизнесменов 9 декабря 2003г прошла сессия на тему:«Права человека и российская конституция»
9 декабря 2003г прошла сессия на тему:«Права человека и российская конституция» Туристические центры Ростовской области
Туристические центры Ростовской области Children’s fashion
Children’s fashion Football is a most popular game in our world
Football is a most popular game in our world Художники - сказочники
Художники - сказочники Московский детско-юношеский центр экологии, краеведения и туризма
Московский детско-юношеский центр экологии, краеведения и туризма Какую роль играет вкус,зрение,обоняние в жизнедеятельности человека
Какую роль играет вкус,зрение,обоняние в жизнедеятельности человека Форма и материал. Роль и значение материала в конструкции
Форма и материал. Роль и значение материала в конструкции Искусство и религия
Искусство и религия Цена за год обучения Международные отношения 2000 USD. - презентация
Цена за год обучения Международные отношения 2000 USD. - презентация Великие правители - внеклассное мероприятие по истории
Великие правители - внеклассное мероприятие по истории ВКР: Разработка сервисной деятельности салона красоты в городе Таганрог
ВКР: Разработка сервисной деятельности салона красоты в городе Таганрог Презентация на тему Федеральное агентство по рыболовству
Презентация на тему Федеральное агентство по рыболовству  Библейские сказания в искусстве
Библейские сказания в искусстве История открытия Латинское aluminium происходит от латинского же alumen, означающего квасцы (сульфат алюминия и калия KAl(SO4)2·12H2O), которые и
История открытия Латинское aluminium происходит от латинского же alumen, означающего квасцы (сульфат алюминия и калия KAl(SO4)2·12H2O), которые и Презентация программы Альберт ЗвирингРуководитель проектаиюнь 2012
Презентация программы Альберт ЗвирингРуководитель проектаиюнь 2012 Презентация на тему Классы неорганических веществ
Презентация на тему Классы неорганических веществ Educational system in Kazakhstan
Educational system in Kazakhstan  ЧИСТАЯ ВОДА ДЛЯ ВСЕХ
ЧИСТАЯ ВОДА ДЛЯ ВСЕХ The Design of Colossus
The Design of Colossus ПРЕДМЕТ, ЗАДАЧИ И ОСНОВНЫЕ ПРОБЛЕМЫ ИСТОЧНИКОВЕДЕНИЯ-2
ПРЕДМЕТ, ЗАДАЧИ И ОСНОВНЫЕ ПРОБЛЕМЫ ИСТОЧНИКОВЕДЕНИЯ-2 Финансовые проекты Восточного направления
Финансовые проекты Восточного направления