Содержание
- 2. Понятие окислительно-восстановительных реакций Химические реакции, протекающие с изменением степени окисления элементов, входящих в состав реагирующих веществ,
- 3. Окисление - процесс отдачи электронов атомом, молекулой или ионом. Атом превращается в положительно заряженный ион: Zn0
- 4. Восстановление - процесс присоединения электронов атомом, молекулой или ионом. Атом превращается в отрицательно заряженный ион S0
- 5. Восстановители - атомы, молекулы или ионы, отдающие электроны. Они в процессе ОВР окисляются Типичные восстановители: ●
- 6. Окислители - атомы, молекулы или ионы, присоединяющие электроны. Они в процессе ОВР восстанавливаются Типичные окислители: ●
- 7. На проявление окислительно-восстановительных свойств влияет такой фактор, как устойчивость молекулы или иона. Чем прочнее частица, тем
- 8. Например, азот имеет высокую электроотрицательность и мог бы быть сильным окислителем в виде простого вещества, но
- 9. Или НСLO более сильный окислитель в растворе, чем НСLO4, так как НСLO – менее устойчивая кислота.
- 10. Если химический элемент находится в промежуточной степени окисления, то он проявляет свойства и окислителя, и восстановителя.
- 11. Степени окисления серы: -2,0,+4,+6 Н2S-2 - восстановитель 2Н2S+3O2=2H2O+2SO2 S0,S+4O2 – окислитель и восстановитель S+O2=SO2 2SO2+O2=2SO3 (восстановитель)
- 12. Определение степеней окисления атомов химических элементов С.о. атомов х/э в составе простого вущества = 0 Алгебраическая
- 13. Классификация окислительно-восстановительных реакций Реакции межмолекулярного окисления 2Al0 + 3Cl20 → 2Al+3 Cl3-1 Реакции внутримолекулярного окисления 2KCl+5O3-2
- 14. Это полезно знать Степени окисления элементов в составе аниона соли такие же, как и в кислоте,
- 15. Окислительные свойства концентрированной серной кислоты Продукты восстановления серы: H2SO4 + оч.акт. металл (Mg, Li, Na…) →
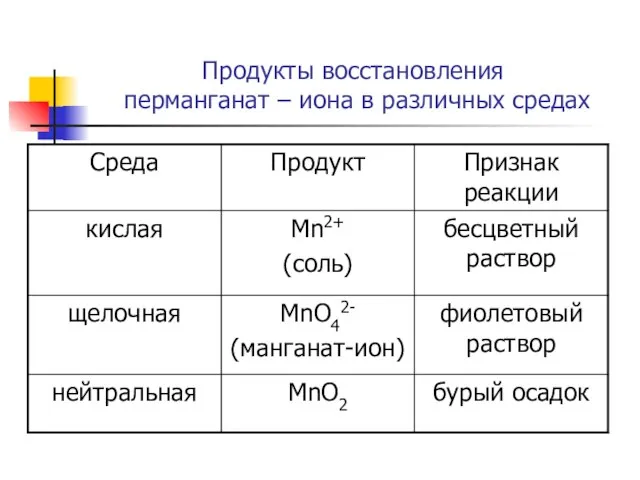
- 16. Продукты восстановления перманганат – иона в различных средах
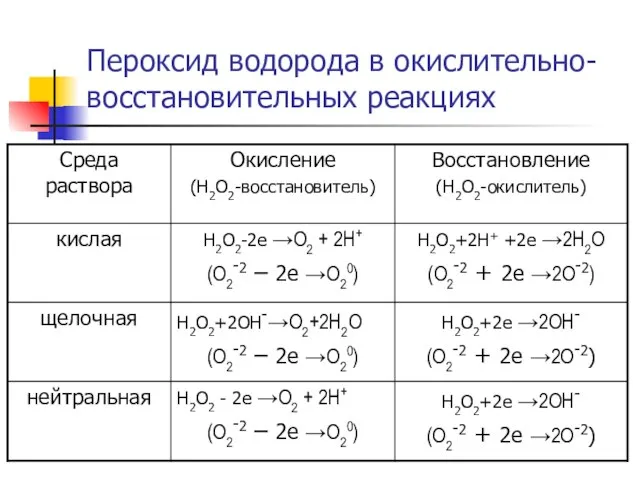
- 17. Пероксид водорода в окислительно-восстановительных реакциях
- 18. Азотная кислота в окислительно-восстановительных реакциях Продукты восстановления азота: Концентрированная HNO3: N+5 +1e → N+4 (NO2) (Ni,
- 20. Скачать презентацию















 Утилизация шлама в оксид магния и карналлит
Утилизация шлама в оксид магния и карналлит Суточный биоритм
Суточный биоритм Тазове передлежання плода: ведення вагітності та пологів
Тазове передлежання плода: ведення вагітності та пологів  Методические рекомендации по работе над творческим проектом
Методические рекомендации по работе над творческим проектом Очистители топливной системы, впускного клапана и распылителя форсунки
Очистители топливной системы, впускного клапана и распылителя форсунки до встречи 1 сентября!
до встречи 1 сентября! Welcome box. Наша история
Welcome box. Наша история Кризисные ситуации и методы их преодоления ( нет подростковому суициду)
Кризисные ситуации и методы их преодоления ( нет подростковому суициду) К ЗВЕЗДАМ !
К ЗВЕЗДАМ ! Итальянская школа Геоэкономики
Итальянская школа Геоэкономики ва
ва Искусство – образная модель мира
Искусство – образная модель мира БИБЛИОТЕКА ГОУ ДПО ПОИПКРО
БИБЛИОТЕКА ГОУ ДПО ПОИПКРО Технические регламенты
Технические регламенты открытая тз (2)
открытая тз (2) Логистическая компания АРЭС
Логистическая компания АРЭС The Incredible Sun
The Incredible Sun  Государственная символика РОССИИ и КБР
Государственная символика РОССИИ и КБР Презентация на тему Ограниченность ресурсов. Кривая производственных возможностей
Презентация на тему Ограниченность ресурсов. Кривая производственных возможностей Растения сада
Растения сада Декоративный натюрморт Коми мотив
Декоративный натюрморт Коми мотив Гидроизоляция блочного фундамента (включая демонтаж)
Гидроизоляция блочного фундамента (включая демонтаж) Моя малая родина – село Красный Яр
Моя малая родина – село Красный Яр Рыцари средневековья
Рыцари средневековья Презентация на тему Теория вероятностей
Презентация на тему Теория вероятностей  Модуль вывода унифицированных аналоговых сигналов ТПТС55.1663
Модуль вывода унифицированных аналоговых сигналов ТПТС55.1663 Mykola Platonovich Bazhan
Mykola Platonovich Bazhan Индукционный нагрев
Индукционный нагрев