Содержание
- 3. Понятие атом возникло ещё в античном мире для обозначения частиц вещества.
- 4. Ученые древности о строении вещества Древнегреческий ученый Демокрит 2500 лет назад считал, что любое вещество состоит
- 5. СТОНЕИ (Стони) Джордж Джонстон (Stoney George Johnstone) (15.II.1826 – 5.VII.1911) — ирландский физик и математик, член
- 6. История открытия строения атома. Уильям Крукс В 1879 году открыл катодные лучи.
- 7. Джозеф Томсон и Жан Перрен доказали, что электроны несут на себе отрицательный заряд Джозеф Томсон Жан
- 8. История открытия строения атома. Дж. Томсон. Доказал, что электроны несут на себе отрицательный заряд, определил массу
- 10. Открытие радиоактивности Анри Беккерель Расщепление радиоактивного излучения
- 11. Эрнест Резерфорд В 1910 г. Эрнест Резерфорд со своими учениками и коллегами изучал рассеивание альфа-частиц, проходящих
- 12. Доказал, что атом имеет плотное ядро. Предложил планетарную теорию строения атома. Э. Резерфорд
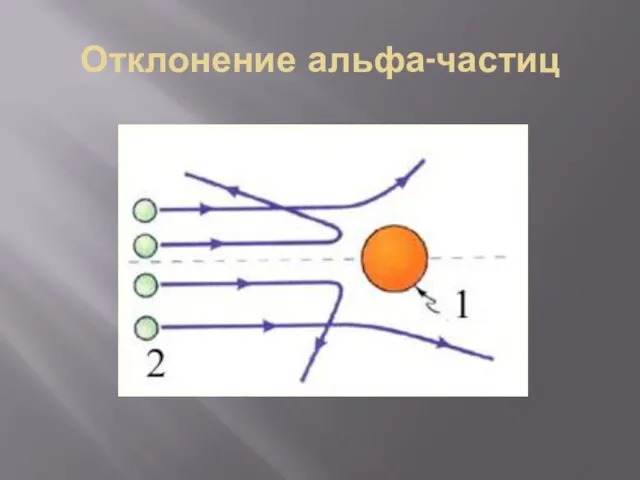
- 15. Отклонение альфа-частиц
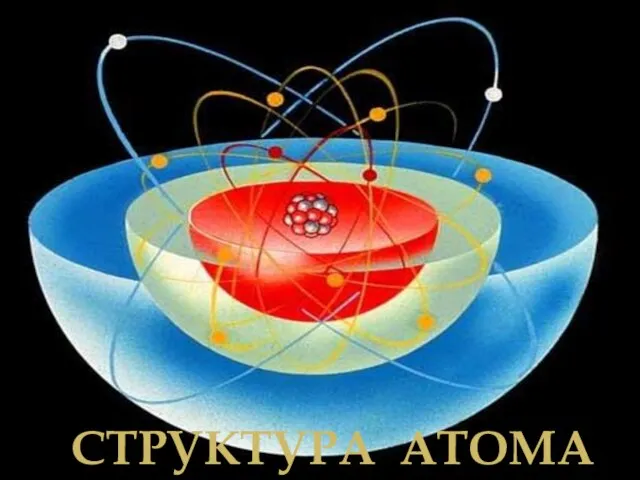
- 16. СТРУКТУРА АТОМА
- 17. В 1911 г. английский ученый Э. Резерфорд доказал ,что в центре атома имеется положительно заряженное ядро.
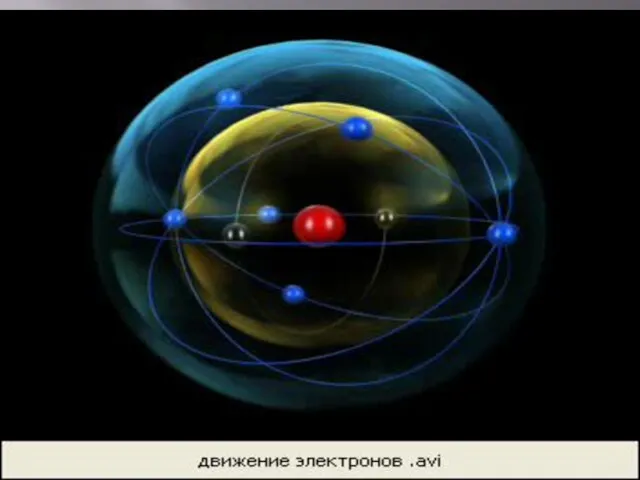
- 18. Планетарная модель строения атома РЕЗЕРФОРД ПРЕДПОЛОЖИЛ, ЧТО АТОМ УСТРОЕН ПОДОБНО ПЛАНЕТАРНОЙ СИСТЕМЕ. СУТЬ МОДЕЛИ СТРОЕНИЯ АТОМА
- 19. Водород
- 21. Характеристики элементарных частиц
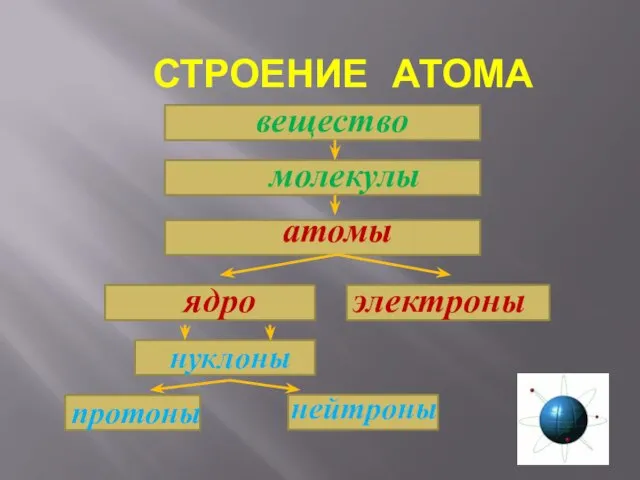
- 22. СТРОЕНИЕ АТОМА вещество молекулы атомы нуклоны
- 23. Число протонов в атоме равно порядковому номеру. Число электронов в атоме равно числу протонов. Число нейтронов
- 24. Изменение в составе ядер атомов химических элементов. Ядерные реакции. Изотопы
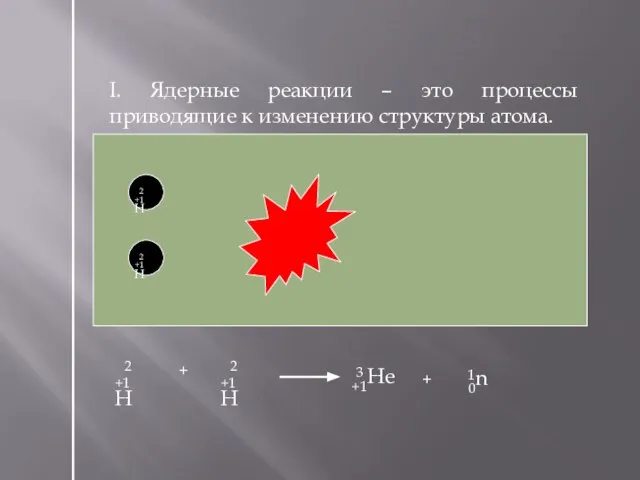
- 25. I. Ядерные реакции – это процессы приводящие к изменению структуры атома. +1Н 2 +1Н 2 +1Не
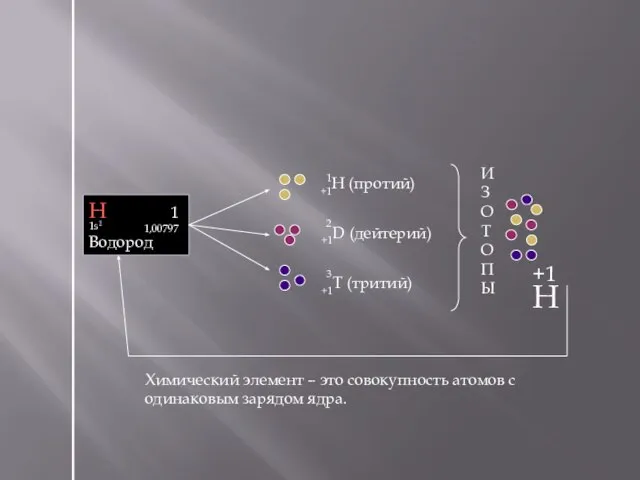
- 27. +1H (протий) +1D (дейтерий) +1T (тритий) Химический элемент – это совокупность атомов с одинаковым зарядом ядра.
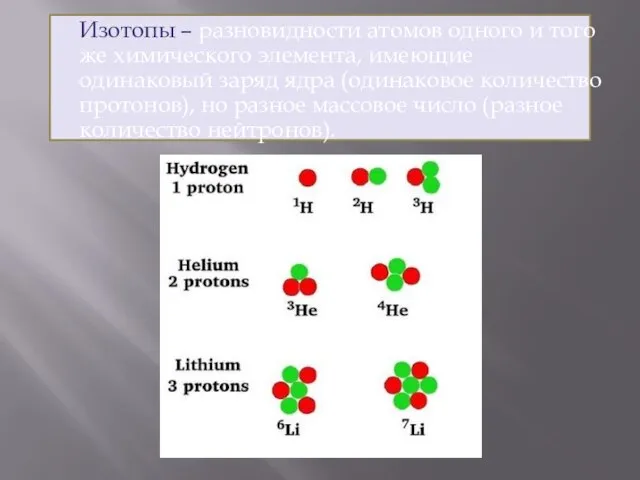
- 28. Изотопы – разновидности атомов одного и того же химического элемента, имеющие одинаковый заряд ядра (одинаковое количество
- 32. Скачать презентацию




















 Всероссийская электронная музыкальная библиотека LibMusicЗадачи первого этапа разработки
Всероссийская электронная музыкальная библиотека LibMusicЗадачи первого этапа разработки История создания клуба
История создания клуба Классификация спортивных соревнований
Классификация спортивных соревнований Галактики. Многообразие галактик
Галактики. Многообразие галактик Авторское право
Авторское право Презентация на тему Профессия парикмахер
Презентация на тему Профессия парикмахер Наш продукт – Азотные коктейли
Наш продукт – Азотные коктейли Marketing channels. Retailing and wholesaling
Marketing channels. Retailing and wholesaling NORMATIVE MATERIALS
NORMATIVE MATERIALS Производственный участок Красноуфимск-Уральский, Горьковской дирекции по ремонту тягового подвижного состава
Производственный участок Красноуфимск-Уральский, Горьковской дирекции по ремонту тягового подвижного состава Правописание безударных окончаний имён существительных
Правописание безударных окончаний имён существительных Перевод вторичного рынка ОФЗ в ЗАО «ФБ ММВБ»
Перевод вторичного рынка ОФЗ в ЗАО «ФБ ММВБ» Права ребенка в нашей стране
Права ребенка в нашей стране Н.А.Некрасов Крестьянские дети
Н.А.Некрасов Крестьянские дети Показ части фильма “Чемпионы 2”
Показ части фильма “Чемпионы 2” Дистанционное обучение. ГУО Средняя школа д. Черни
Дистанционное обучение. ГУО Средняя школа д. Черни Проект SLIMELAB
Проект SLIMELAB Республика Крым
Республика Крым Внутренняя среда ОАО Цвет
Внутренняя среда ОАО Цвет IntelSVO. Оптимизация судебной работы
IntelSVO. Оптимизация судебной работы Проводы зимы
Проводы зимы Разработка ТЭО строительство автомобильной обходной дороги г. Ош
Разработка ТЭО строительство автомобильной обходной дороги г. Ош Презентация на тему Культура Западной Европы в раннее средневековье
Презентация на тему Культура Западной Европы в раннее средневековье  История лампочки
История лампочки КОНЦЕССИИ КАК ОСНОВНОЙ ИНСТРУМЕНТ ГОСУДАРСТВЕННО-ЧАСТНОГО ПАРТНЕРСТВА В УКРАИНЕ: ВОЗМОЖНОСТИ И ПОТЕНЦИАЛЬНЫЕ РИСКИ ПРОЕКТОВ АВТ
КОНЦЕССИИ КАК ОСНОВНОЙ ИНСТРУМЕНТ ГОСУДАРСТВЕННО-ЧАСТНОГО ПАРТНЕРСТВА В УКРАИНЕ: ВОЗМОЖНОСТИ И ПОТЕНЦИАЛЬНЫЕ РИСКИ ПРОЕКТОВ АВТ Врожденный гипотиреоз
Врожденный гипотиреоз Презентация на тему: Писатель Красноярского края
Презентация на тему: Писатель Красноярского края Пассажирские и товарные вагоны
Пассажирские и товарные вагоны