Содержание
- 2. Но наука никогда не стоит на месте: В середине XIX века было известно уже 63 химических
- 3. Классификация химических элементов на: металлы и неметаллы Якоб Йен Берцеллиус Общие свойства металлов: Пластичность – способность
- 4. Какими признаками обладают указанные вещества? Графит - углерод Кремний Йод Некоторые неметаллы обладают металлическими признаками Вывод:
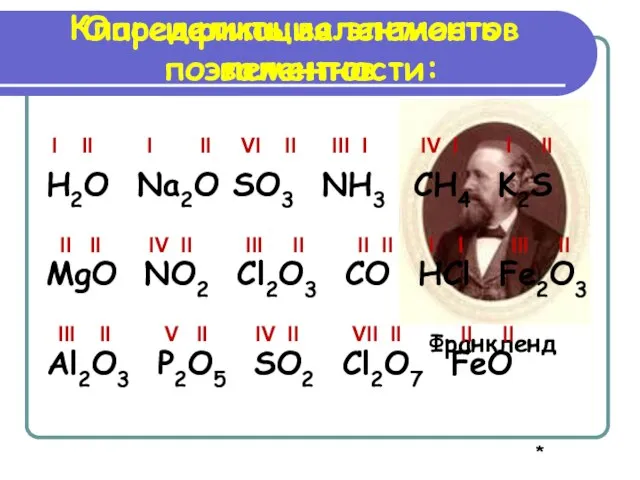
- 5. Классификация элементов по валентности: Франкленд I II I II VI II III I IV I I
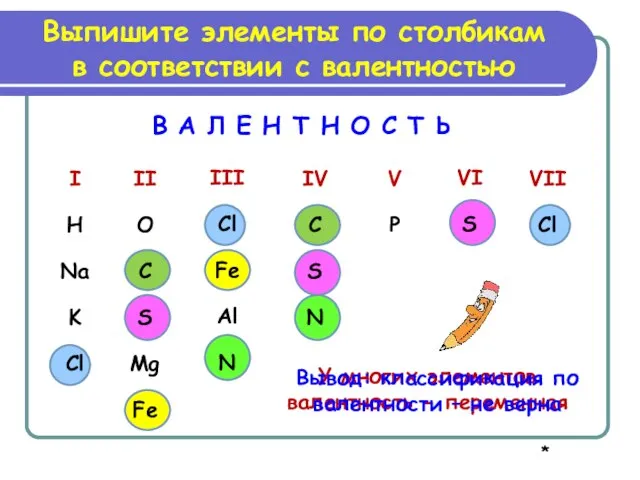
- 6. Выпишите элементы по столбикам в соответствии с валентностью В А Л Е Н Т Н О
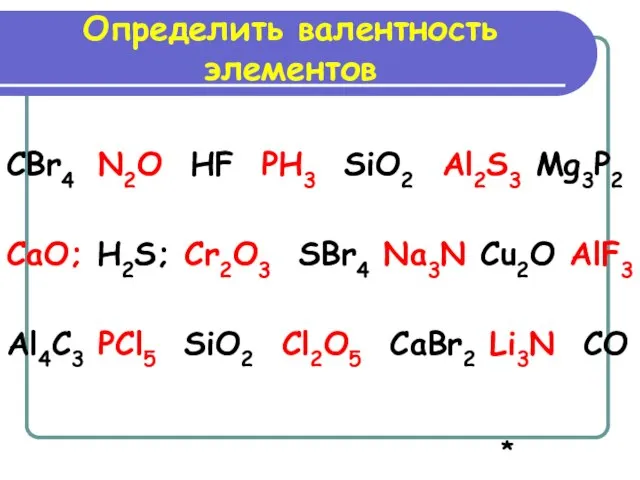
- 7. CBr4 N2O HF PH3 SiO2 Al2S3 Mg3P2 CaO; H2S; Cr2O3 SBr4 Na3N Cu2O AlF3 Al4C3 PCl5
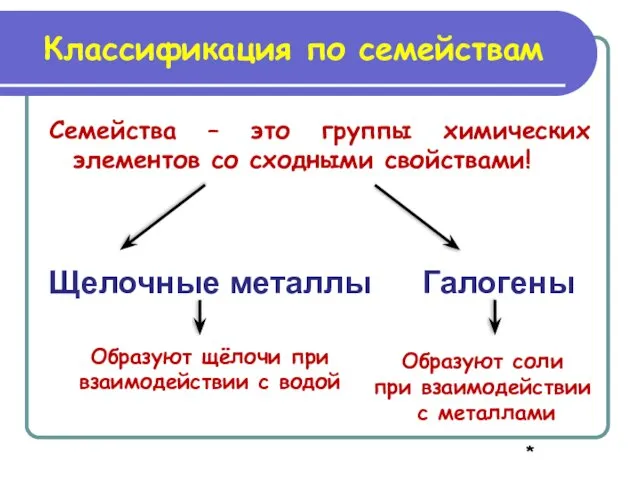
- 8. Классификация по семействам Семейства – это группы химических элементов со сходными свойствами! Щелочные металлы Галогены Образуют
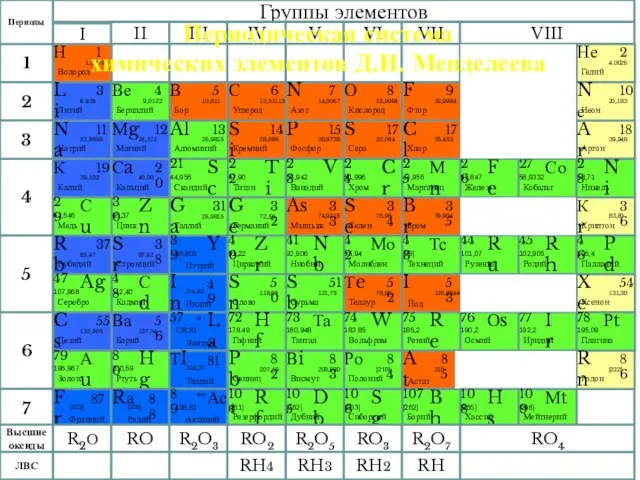
- 9. Периодическая система химических элементов Д.И. Менделеева
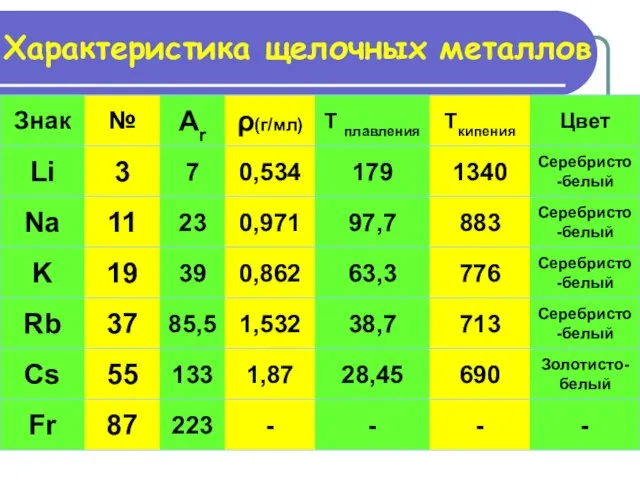
- 10. Характеристика щелочных металлов
- 11. Щелочные металлы – простые вещества литий натрий калий рубидий цезий *
- 12. Na + H2O → NaOH + H2↑ 2 2 2 I I Взаимодействие щелочных металлов с
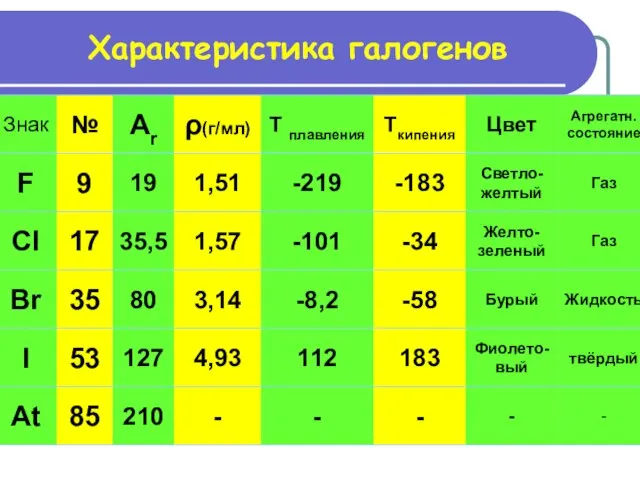
- 13. Характеристика галогенов
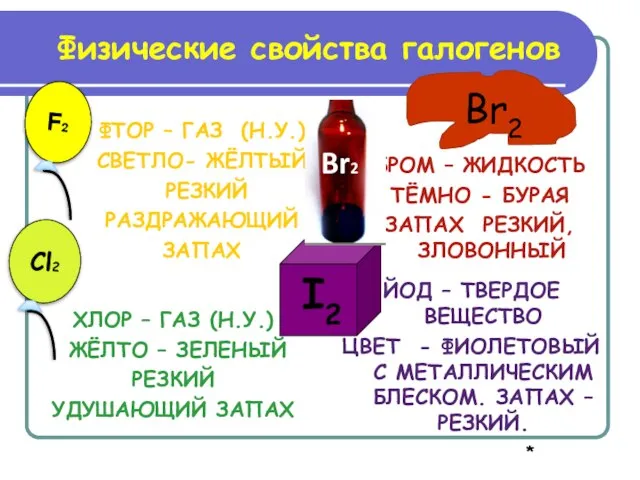
- 14. ФТОР – ГАЗ (Н.У.) СВЕТЛО- ЖЁЛТЫЙ РЕЗКИЙ РАЗДРАЖАЮЩИЙ ЗАПАХ БРОМ – ЖИДКОСТЬ ТЁМНО - БУРАЯ ЗАПАХ
- 15. Возгонка йода Возгонка – это переход вещества из твердого агрегатного состояния в газообразное, минуя жидкое.
- 16. Повторение: 1. Расставьте коэффициенты в следующих уравнениях реакций. Определите типы реакций: СаСО3 → СаО + CO2
- 18. Скачать презентацию







 Системный блок. Внутри ПК
Системный блок. Внутри ПК Субъекты международного права
Субъекты международного права Звери наших лесов
Звери наших лесов Нескучные прогулки по Перми
Нескучные прогулки по Перми Возможности человеческой памяти
Возможности человеческой памяти Логотип Morozov Stile
Логотип Morozov Stile Презентация_по_Компенсам_для_рассылки
Презентация_по_Компенсам_для_рассылки Позиционирование специальных видов бумаг
Позиционирование специальных видов бумаг Презентация на тему Украинская кухня
Презентация на тему Украинская кухня Name of presentation
Name of presentation Герб Удмуртской Республики
Герб Удмуртской Республики Презентация на тему Экономическое устройство России
Презентация на тему Экономическое устройство России Презентация на тему АНТОНИМЫ
Презентация на тему АНТОНИМЫ  Леонид Пантелеев
Леонид Пантелеев Кредит на возобновление деятельности Перезагрузка, банк ПСБ
Кредит на возобновление деятельности Перезагрузка, банк ПСБ Экономия и несостоявшиеся торги
Экономия и несостоявшиеся торги Технология развития субъекта физкультурной деятельности
Технология развития субъекта физкультурной деятельности История новогодней игрушки
История новогодней игрушки Введение в социологию
Введение в социологию Системы Интернет коммерции и их значение
Системы Интернет коммерции и их значение Поделка из бумаги и картона в технике оригами
Поделка из бумаги и картона в технике оригами Аид и его подземное царство
Аид и его подземное царство ©
© Подбор сувенирной продукции окончательно
Подбор сувенирной продукции окончательно Отец русского театра - Фёдор Волков
Отец русского театра - Фёдор Волков Профилактика взаимоотношений в семье «Лучший способ воспитать хороших детей – это сделать их счастливыми». Оскар Уайльд
Профилактика взаимоотношений в семье «Лучший способ воспитать хороших детей – это сделать их счастливыми». Оскар Уайльд Исәнмесез! Хәерле көн! Көнегез уңышлы үтсен!
Исәнмесез! Хәерле көн! Көнегез уңышлы үтсен! Социально - досуговая спортивно-оздоровительная программа Автослёт «Пятое колесо»
Социально - досуговая спортивно-оздоровительная программа Автослёт «Пятое колесо»