Содержание
- 2. «Повсюду, где мы встречаем жизнь, мы находим, что она связана с каким-либо белковым телом, и повсюду,
- 3. Пребиотический (абиогенный) синтез аминокислот * CH4, NH3, H2, H2O, HCN, H2S, CH2O; * УФ-излучение, электрический разряд,
- 4. “Натура тем паче всего удивительна, что в простоте своей многохитростна и от малого числа причин производит
- 5. 20 аминокислот могут дать примерно 100000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000 белков, состоящих из 150 остатков аминокислот. Это астрономическое число –
- 6. Первая по популярности поисковая система (79,65 %)
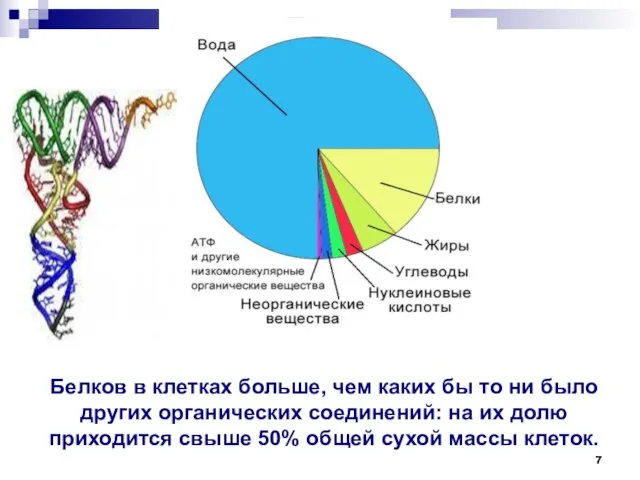
- 7. Белков в клетках больше, чем каких бы то ни было других органических соединений: на их долю
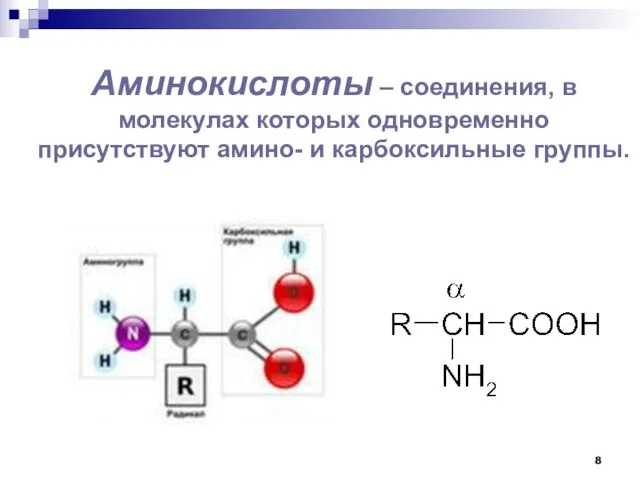
- 8. Аминокислоты – соединения, в молекулах которых одновременно присутствуют амино- и карбоксильные группы.
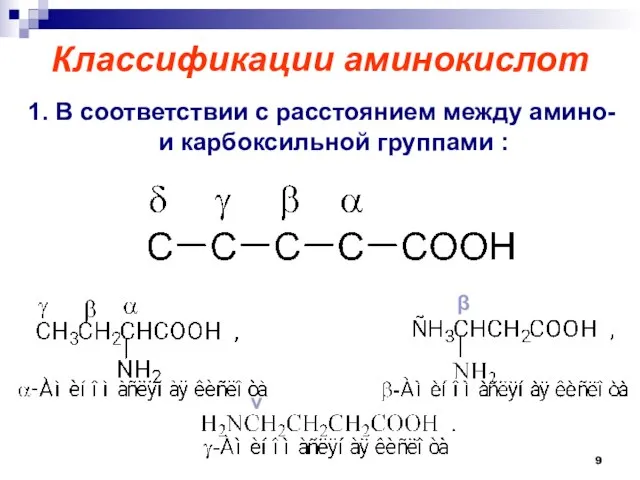
- 9. Классификации аминокислот 1. В соответствии с расстоянием между амино- и карбоксильной группами : β ν
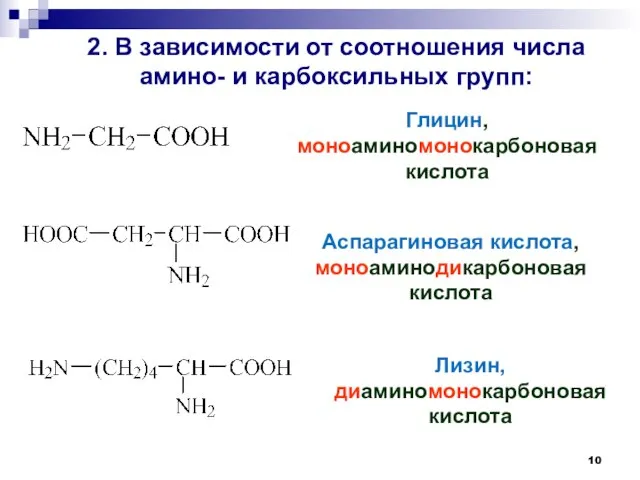
- 10. Глицин, моноаминомонокарбоновая кислота Аспарагиновая кислота, моноаминодикарбоновая кислота Лизин, диаминомонокарбоновая кислота 2. В зависимости от соотношения числа
- 11. В зависимости от того, могут ли аминокислоты синтезироваться в организме или обязательно должны поступать в составе
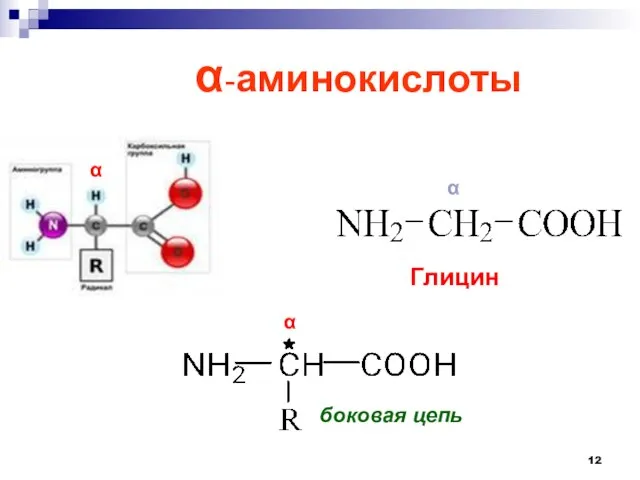
- 12. -аминокислоты α α Глицин боковая цепь α
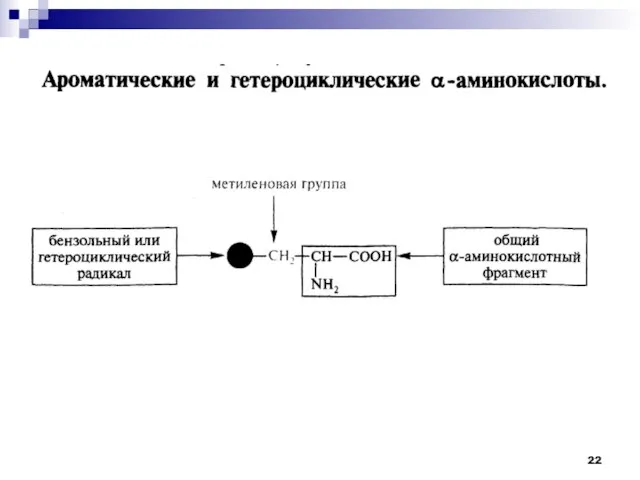
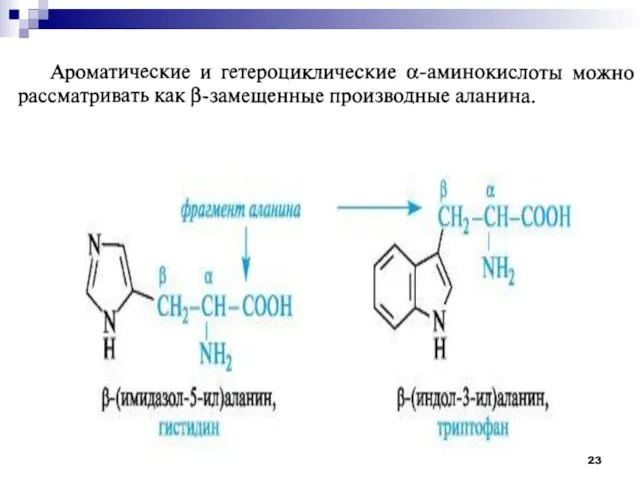
- 13. В соответствии с природой остатка R (боковой цепью) -аминокислоты подразделяют на группы:
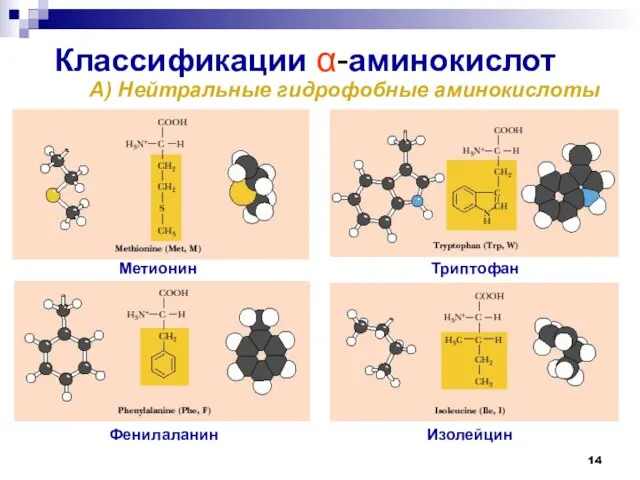
- 14. Классификации -аминокислот А) Нейтральные гидрофобные аминокислоты Изолейцин Фенилаланин Метионин Триптофан
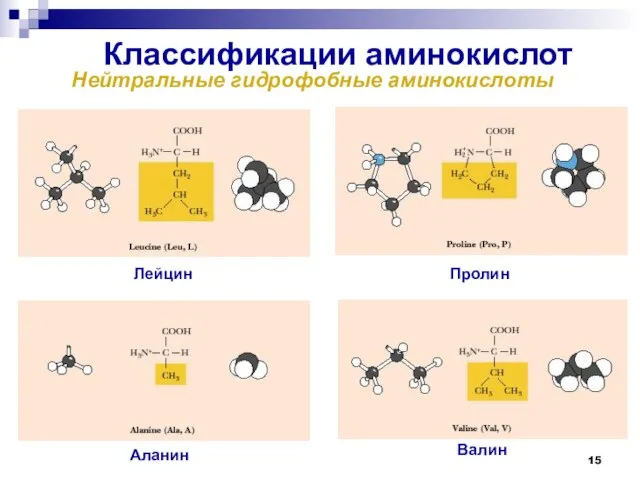
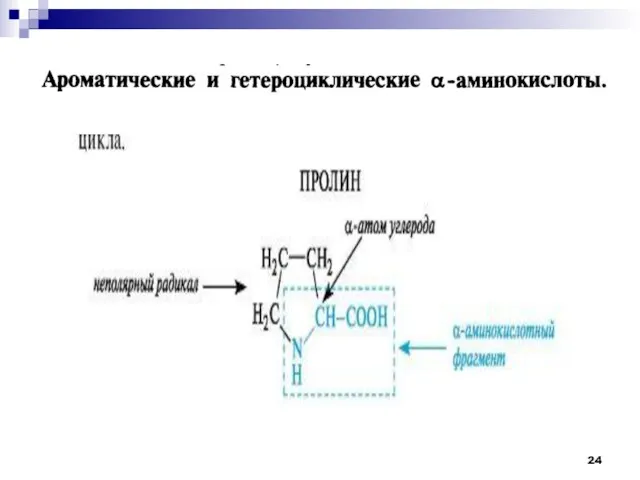
- 15. Классификации аминокислот Нейтральные гидрофобные аминокислоты Аланин Валин Лейцин Пролин
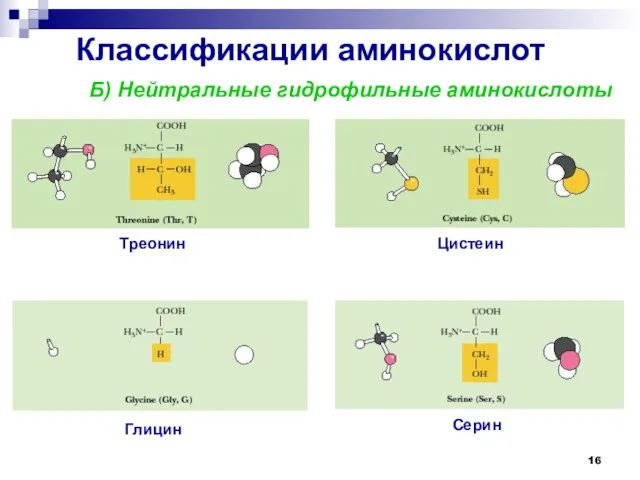
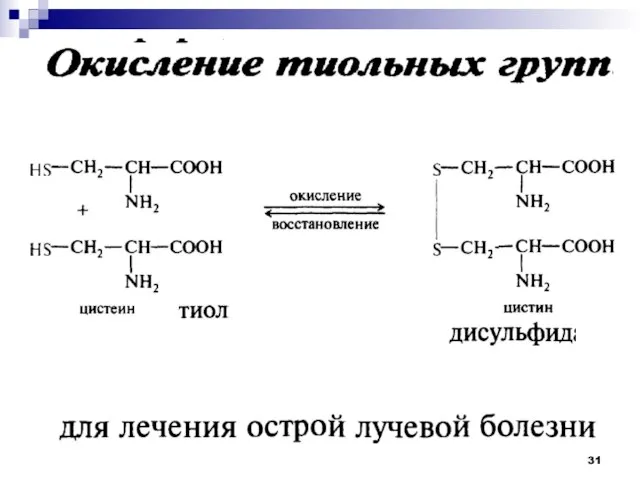
- 16. Классификации аминокислот Б) Нейтральные гидрофильные аминокислоты Глицин Серин Треонин Цистеин
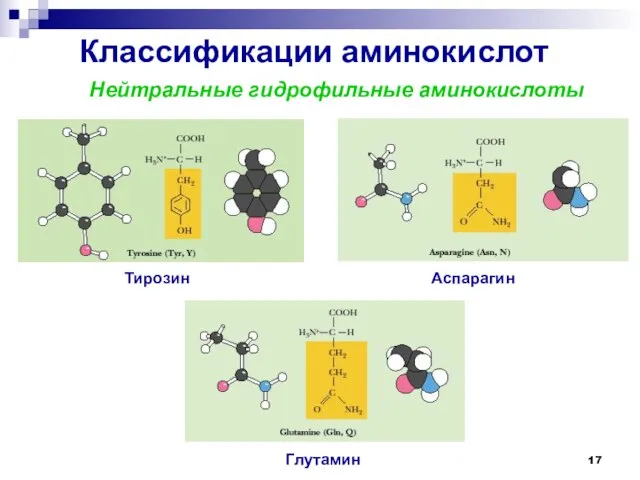
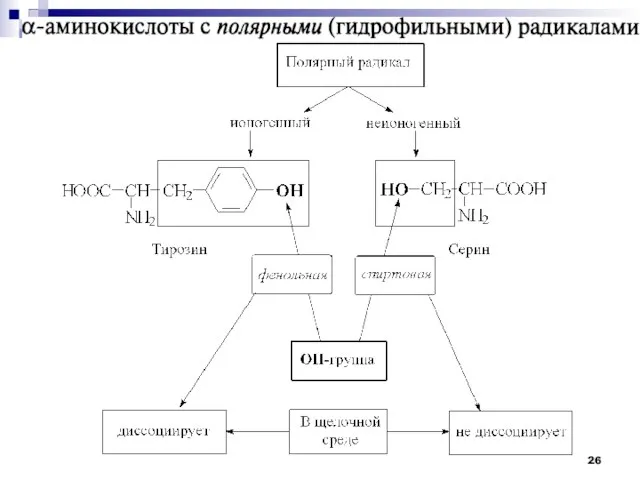
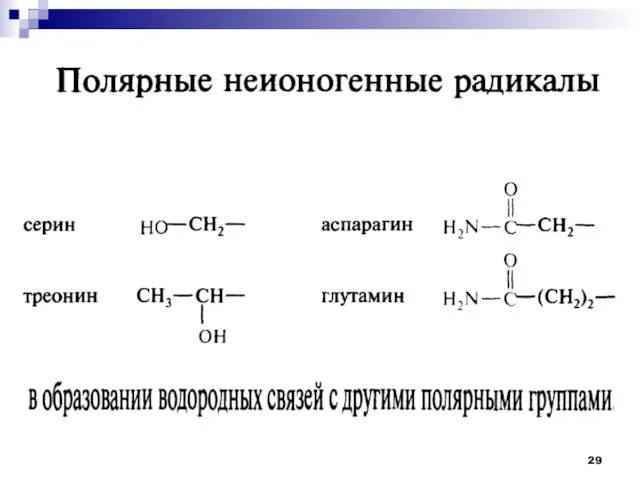
- 17. Классификации аминокислот Нейтральные гидрофильные аминокислоты Тирозин Аспарагин Глутамин
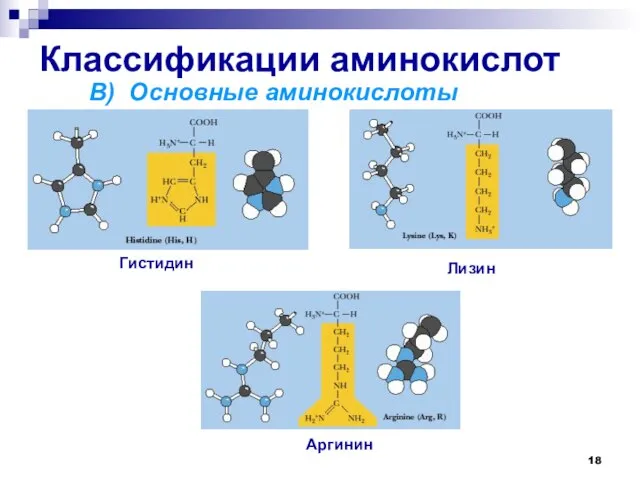
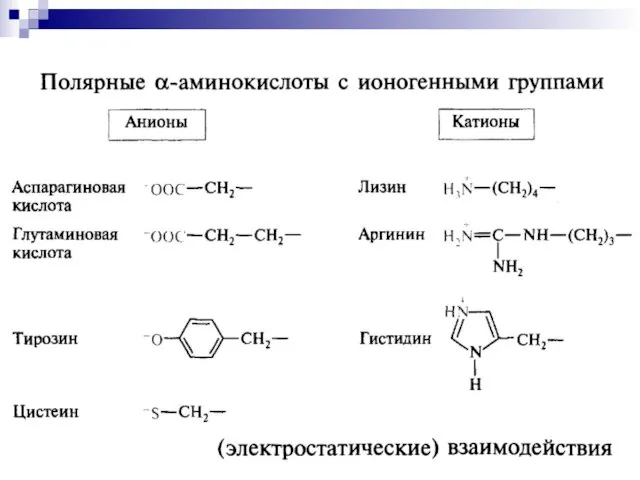
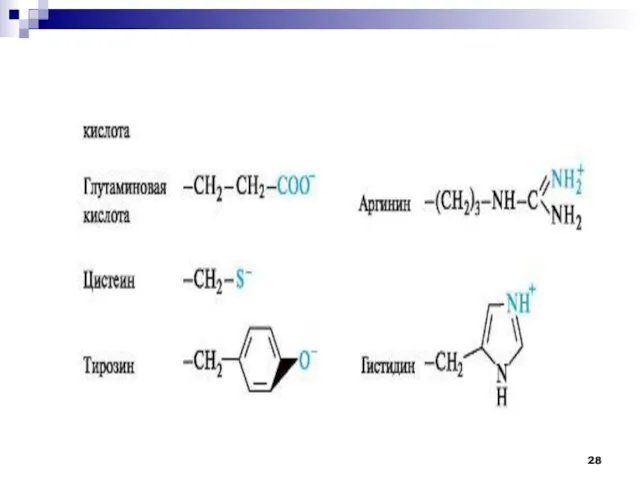
- 18. Классификации аминокислот В) Основные аминокислоты Лизин Аргинин Гистидин
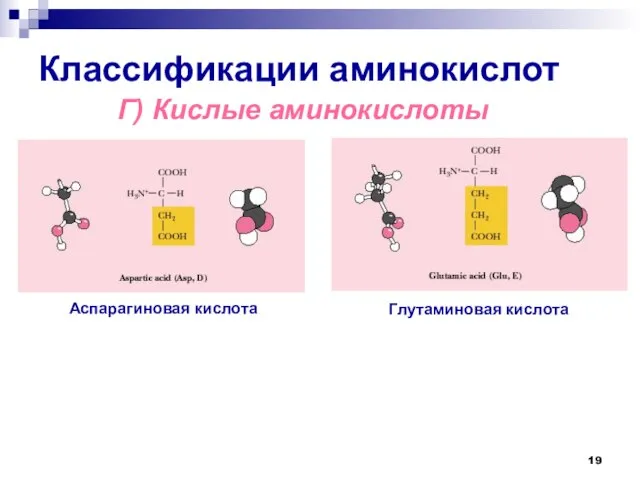
- 19. Классификации аминокислот Г) Кислые аминокислоты Глутаминовая кислота Аспарагиновая кислота
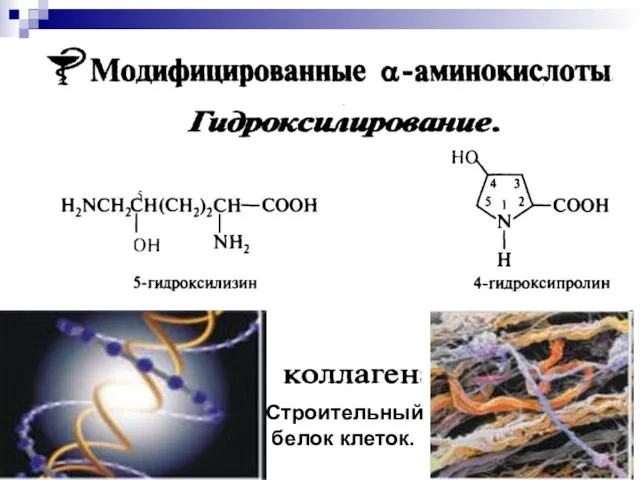
- 30. Строительный белок клеток.
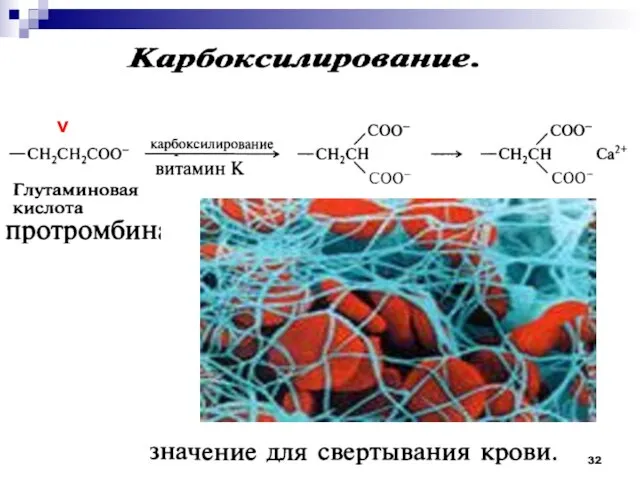
- 32. ν
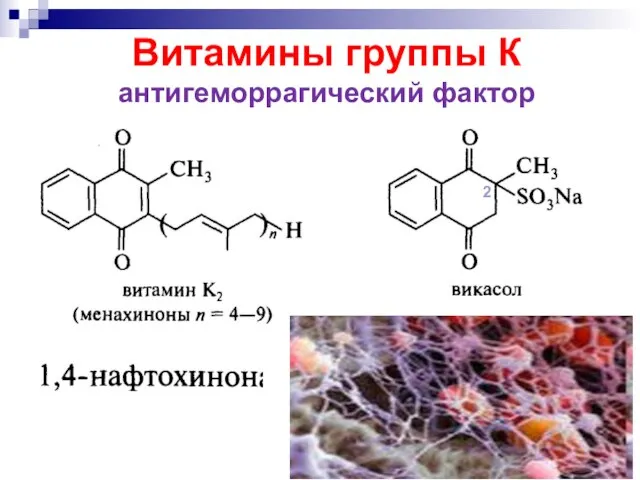
- 33. Витамины группы К антигеморрагический фактор 2
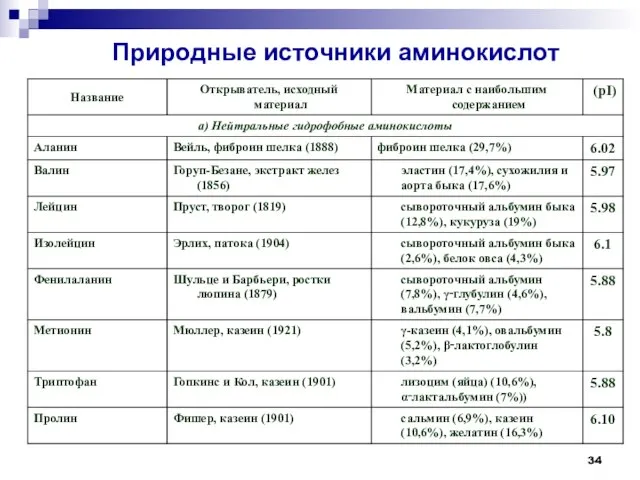
- 34. Природные источники аминокислот
- 35. Природные источники аминокислот
- 36. Природные источники аминокислот
- 37. Тривиальные названия α-аминокислот Серин входит в состав фиброина шелка (от лат. serieus - шелковистый); Тирозин впервые
- 38. Номенклатура Тривиальная номенклатура в основном используется для широко распространённых -- аминокислот. Рациональная IUPAC -амино- -гидроксипропионовая кислота
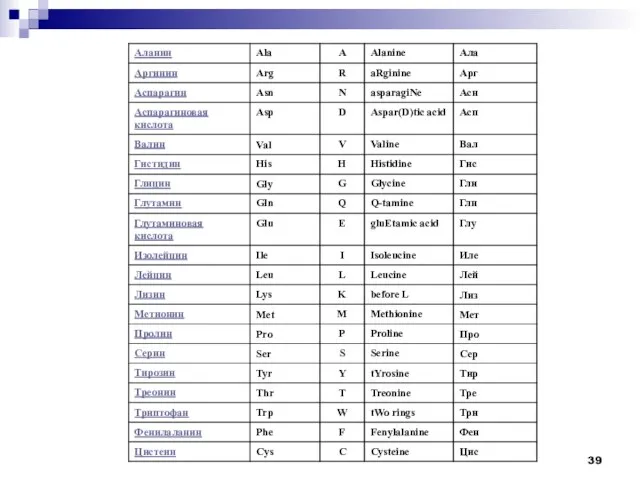
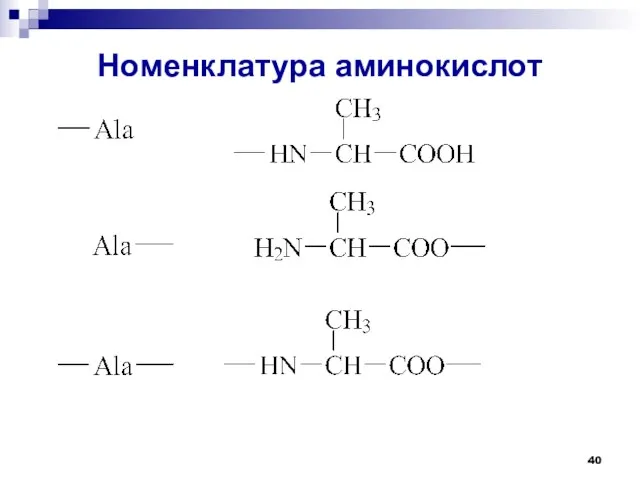
- 40. Номенклатура аминокислот
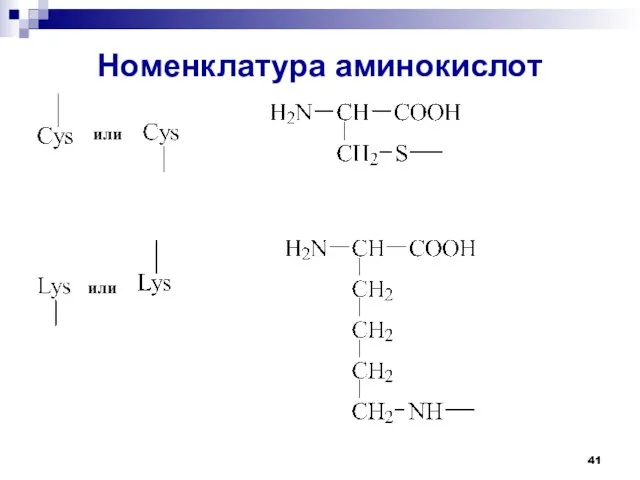
- 41. Номенклатура аминокислот или или
- 42. Нестандартные аминокислоты β-Аланин, 3-аминопропановая кислота, β-Ala H3N+CH2CH2COO– Карнозин (бета-аланил-L-гистидин) , βAlaHis антиоксидант , природный стимулятор мышечной
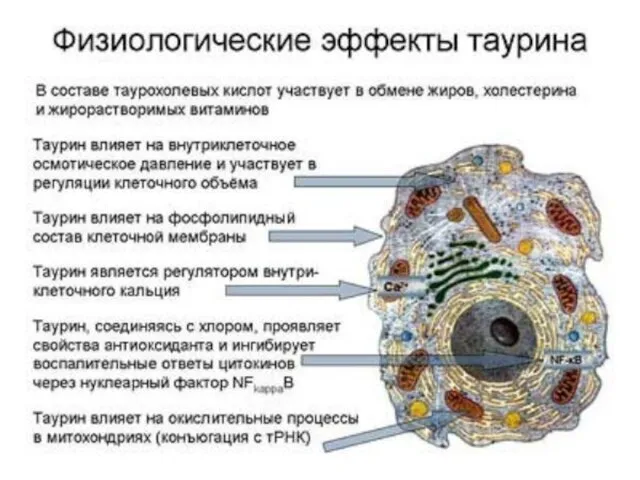
- 43. Таурин, 2-аминоэтансульфоновая кислота, природная серосодержащая аминокислота, выделенная из бычьей желчи в 1827 г. нейромедиаторная аминокислота в
- 45. Зеркало Венеры (1898), Sir Edward Burne-Jones / Museu Calouste Gulbenkian Lisbon /
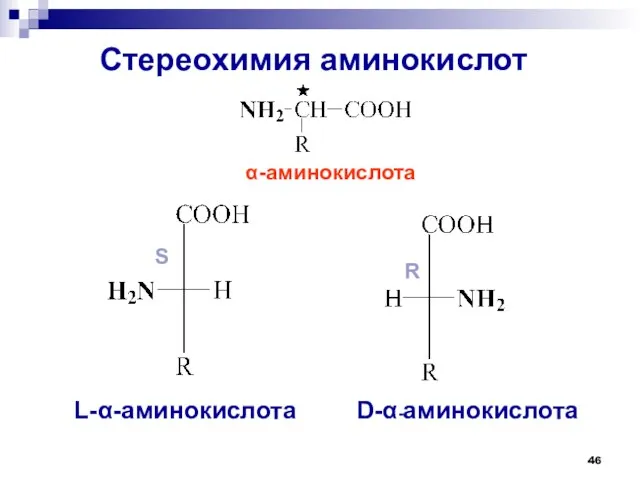
- 46. Стереохимия аминокислот -аминокислота L--аминокислота D--аминокислота S R
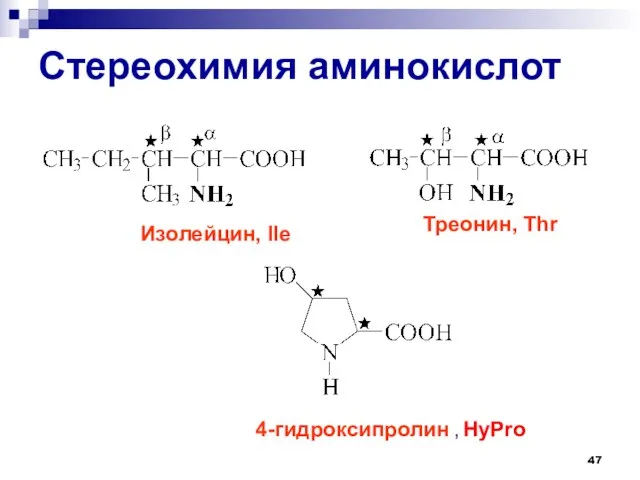
- 47. Стереохимия аминокислот Изолейцин, Ile Треонин, Thr 4-гидроксипролин , HyPro
- 48. D-аспарагиновая кислота и D-метионин предположительно являются нейромедиаторами у млекопитающих. D-метионин и D-аланин входят в состав опиоидных
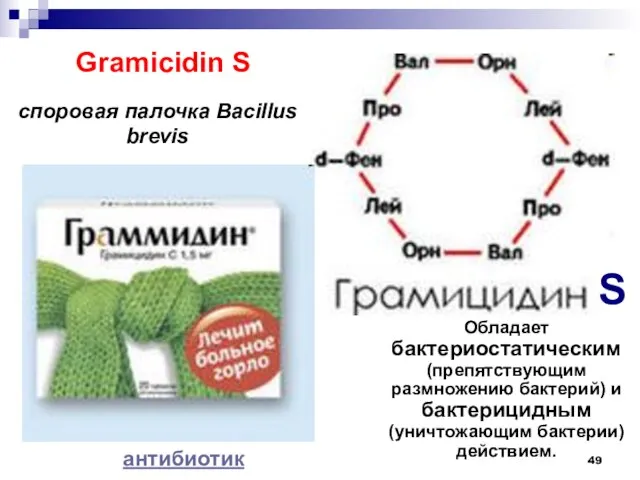
- 49. Gramicidin S S споровая палочка Bacillus brevis Обладает бактериостатическим (препятствующим размножению бактерий) и бактерицидным (уничтожающим бактерии)
- 50. Аспартам метиловый эфир L-Аспартил-L-Фенилаланина Большое количество токсикологических и клинических исследований аспартама подтверждают его безвредность, если дневная
- 51. Несуществующая в природе форма Биполярный ион (цвиттер-ион), внутренняя соль Физические и химические свойства Как в водных
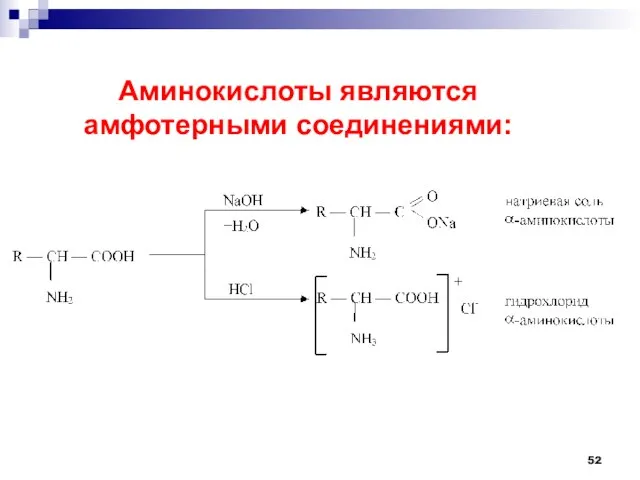
- 52. Аминокислоты являются амфотерными соединениями:
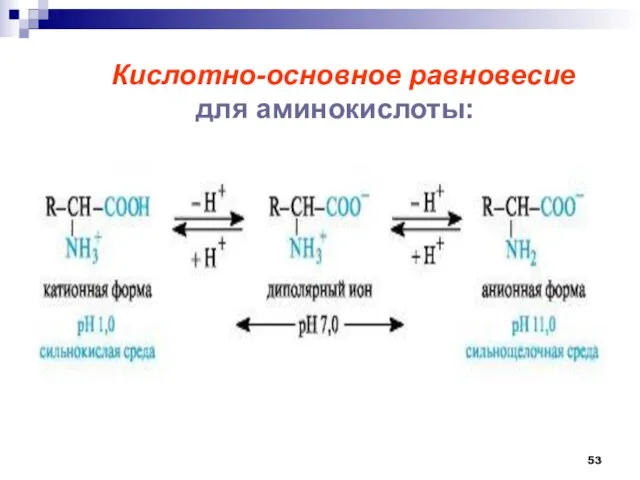
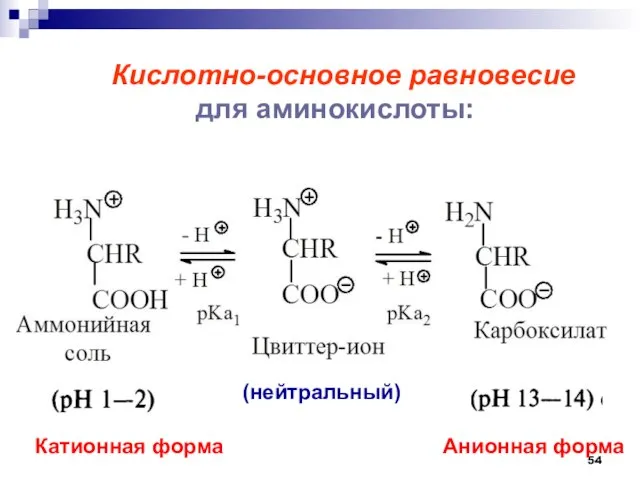
- 53. Кислотно-основное равновесие для аминокислоты:
- 54. Кислотно-основное равновесие для аминокислоты: Катионная форма Анионная форма (нейтральный)
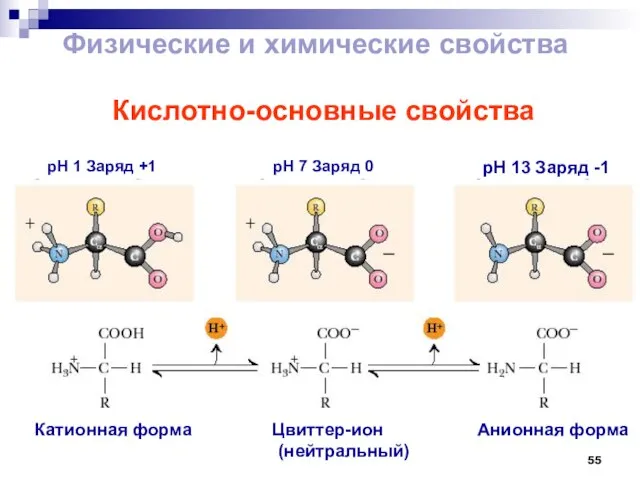
- 55. Кислотно-основные свойства pH 1 Заряд +1 pH 7 Заряд 0 pH 13 Заряд -1 Цвиттер-ион (нейтральный)
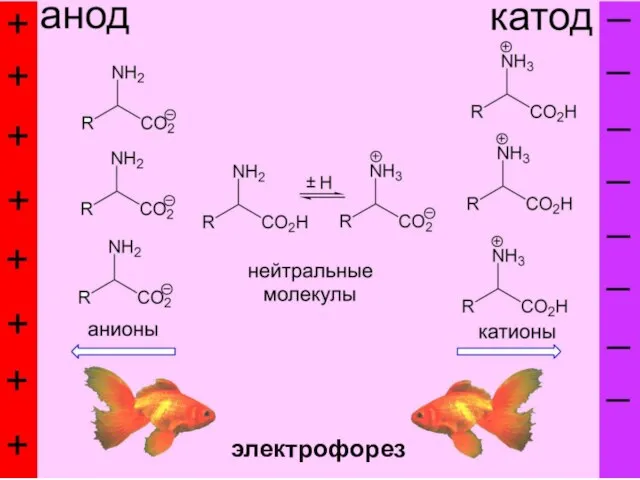
- 56. электрофорез
- 57. Изоэлектрическая точка
- 58. Изоэлектрическая точка
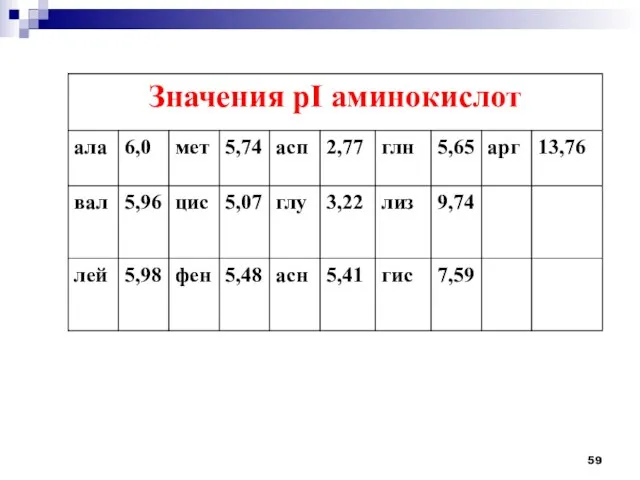
- 60. Для моноаминомонокарбоновых кислот pI ≈ 5-6 pI моноаминодикарбоновых кислот (Asp, Glu) ≈ 3 pI диаминомонокарбоновых кислот
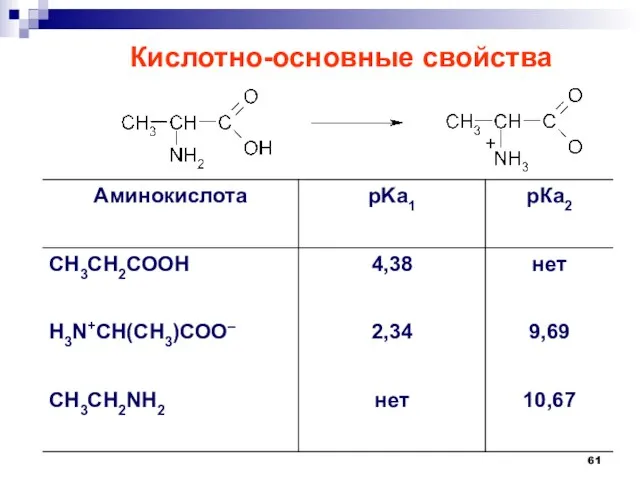
- 61. Кислотно-основные свойства
- 62. Получение аминокислот 1. Выделение из белков и пептидов Белки гидролизуют - 6 М HCl, при нагревании
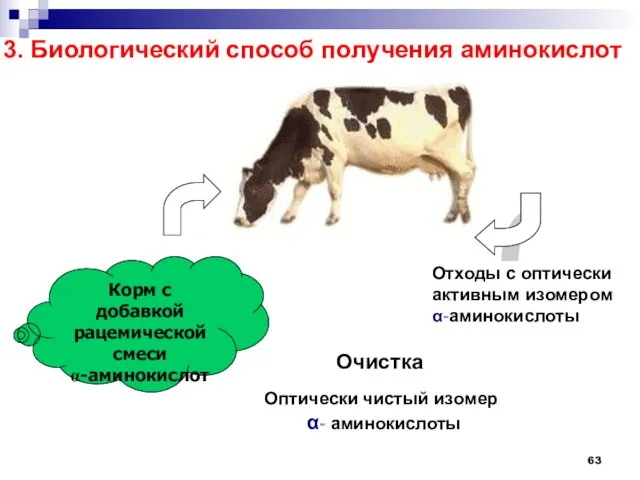
- 63. 3. Биологический способ получения аминокислот Корм с добавкой рацемической смеси a-аминокислот Отходы с оптически активным изомером
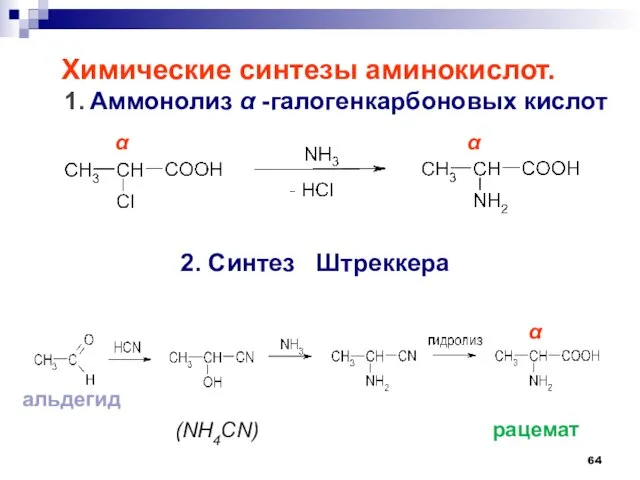
- 64. Химические синтезы аминокислот. 1. Аммонолиз -галогенкарбоновых кислот 2. Синтез Штреккера (NH4CN) рацемат альдегид
- 65. Реакции с участием только аминогруппы 1. Алкилирование саркозин - N-метилглицин биполярный ион (CH3I) CH3N+H2CH2COO- промежуточное соединение
- 66. Простейший бетаин - производное глицина - был впервые обнаружен в соке столовой свеклы Beta vulgaris биполярный
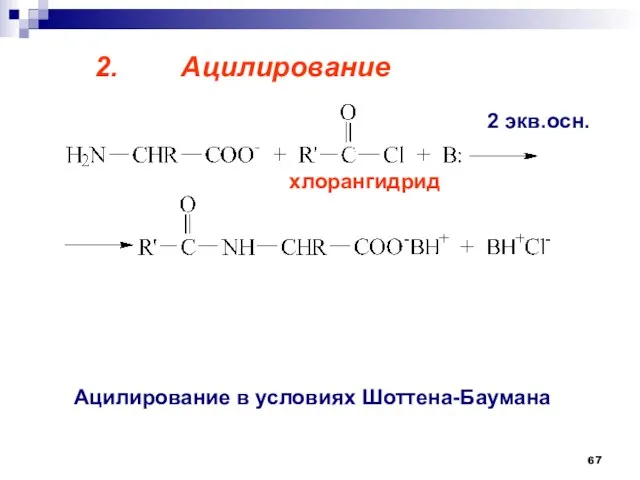
- 67. 2. Ацилирование Ацилирование в условиях Шоттена-Баумана хлорангидрид 2 экв.осн.
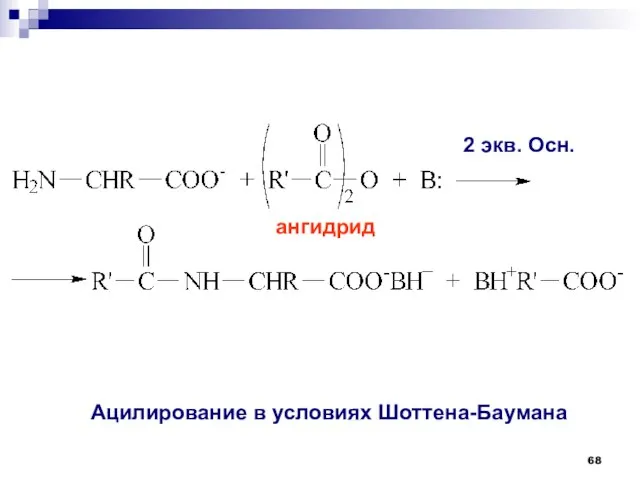
- 68. 2 экв. Осн. ангидрид Ацилирование в условиях Шоттена-Баумана
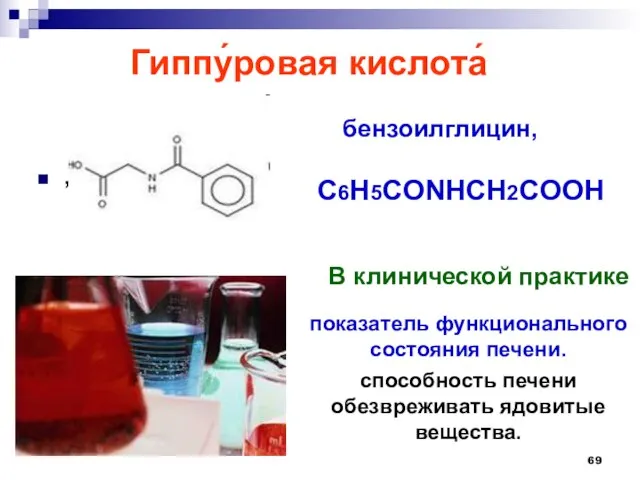
- 69. Гиппу́ровая кислота́ , В клинической практике бензоилглицин, C6H5CONHCH2COOH показатель функционального состояния печени. способность печени обезвреживать ядовитые
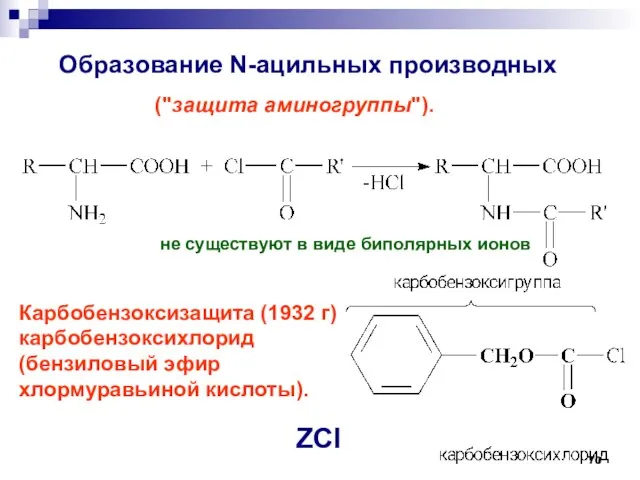
- 70. Образование N-ацильных производных Карбобензоксизащита (1932 г) карбобензоксихлорид (бензиловый эфир хлормуравьиной кислоты). ZCl ("защита аминогруппы"). не существуют
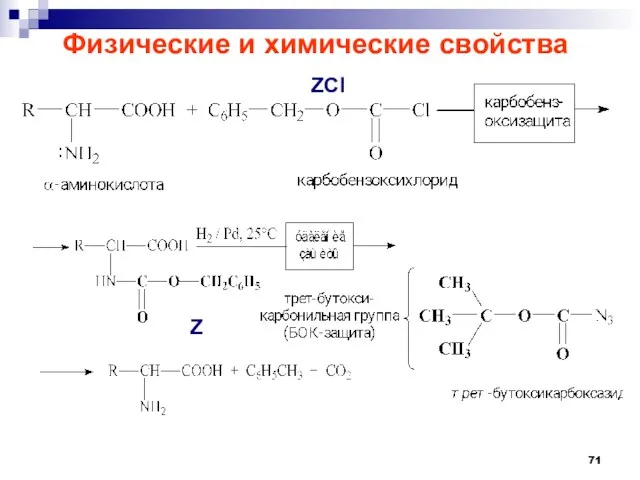
- 71. Физические и химические свойства Z ZCl
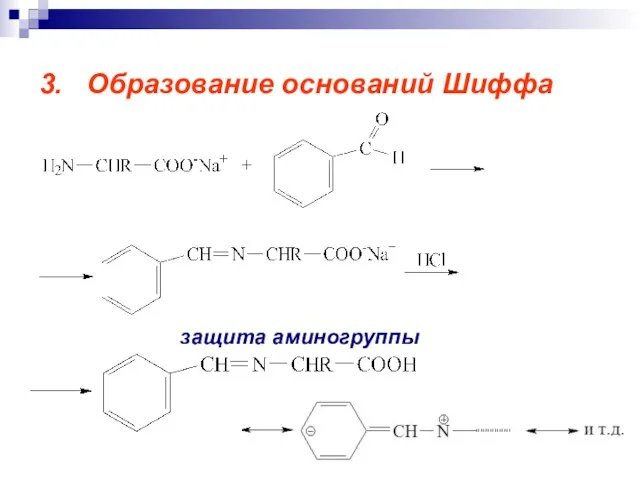
- 72. 3. Образование оснований Шиффа защита аминогруппы
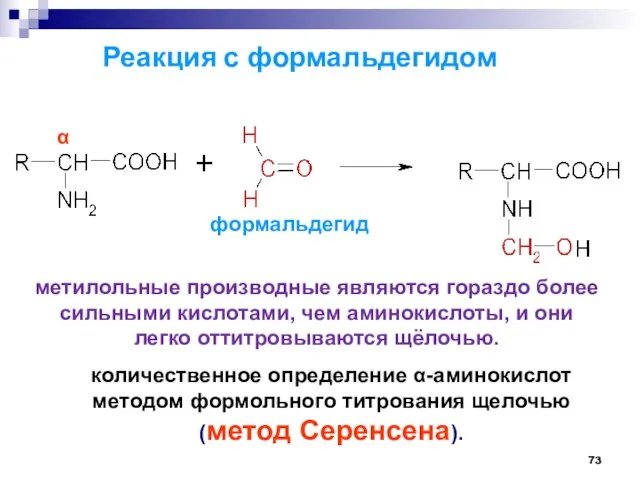
- 73. Реакция с формальдегидом количественное определение -аминокислот методом формольного титрования щелочью (метод Серенсена). формальдегид метилольные производные
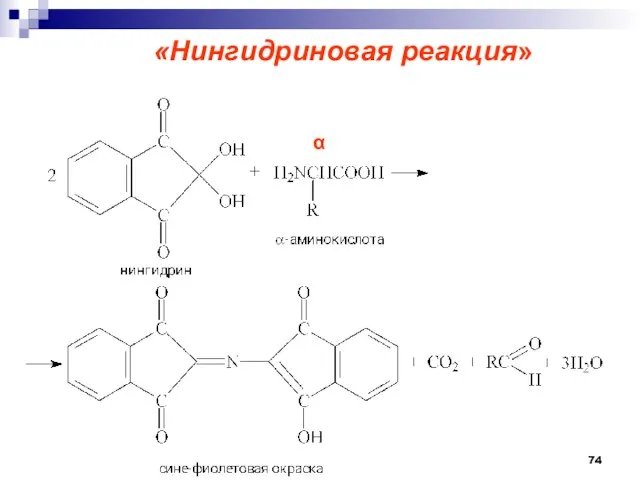
- 74. «Нингидриновая реакция»
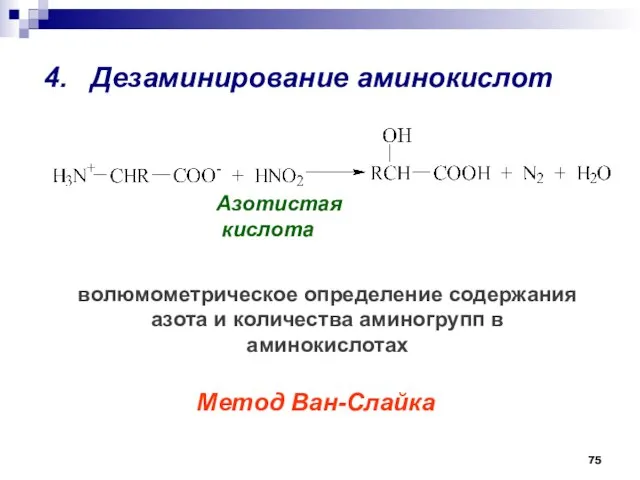
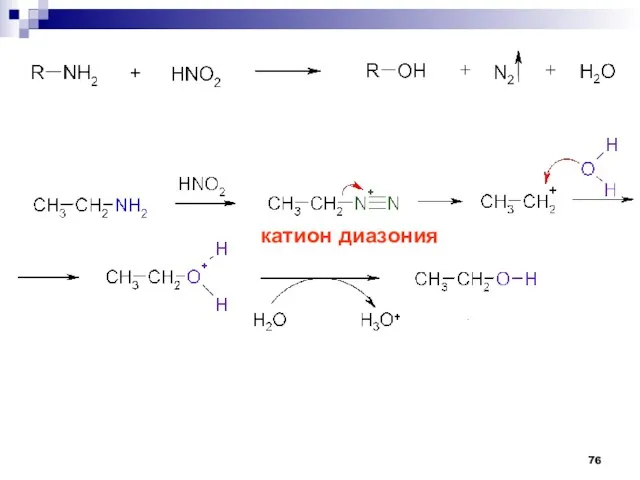
- 75. волюмометрическое определение содержания азота и количества аминогрупп в аминокислотах 4. Дезаминирование аминокислот Метод Ван-Слайка Азотистая кислота
- 76. катион диазония
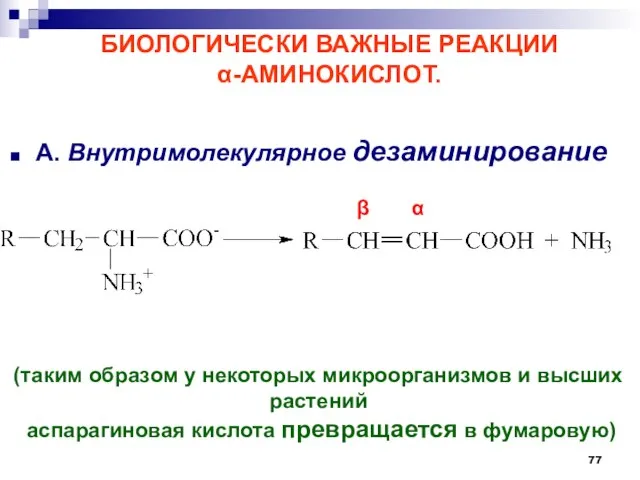
- 77. БИОЛОГИЧЕСКИ ВАЖНЫЕ РЕАКЦИИ -АМИНОКИСЛОТ. А. Внутримолекулярное дезаминирование (таким образом у некоторых микроорганизмов и высших растений аспарагиновая
- 78. Б. Восстановительное дезаминирование (у некоторых микроорганизмов ) В. Гидролитическое дезаминирование (тип дезаминирования, характерный для микроорганизмов)
- 79. Г. Дегидратазное дезаминирование (этот тип дезаминирования характерен для аминокислот серин, треонин, цистеин)
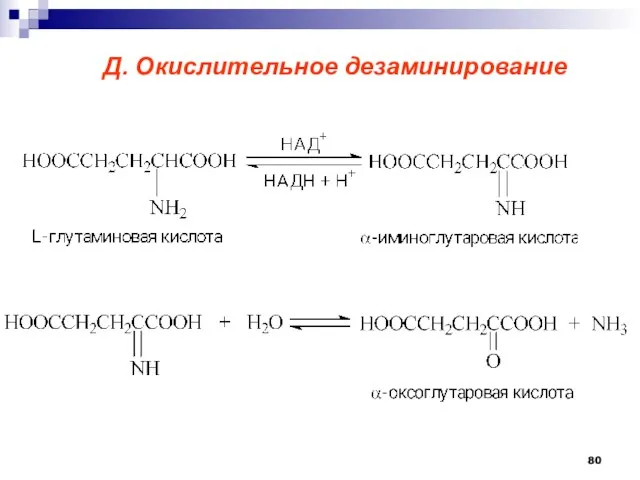
- 80. Д. Окислительное дезаминирование
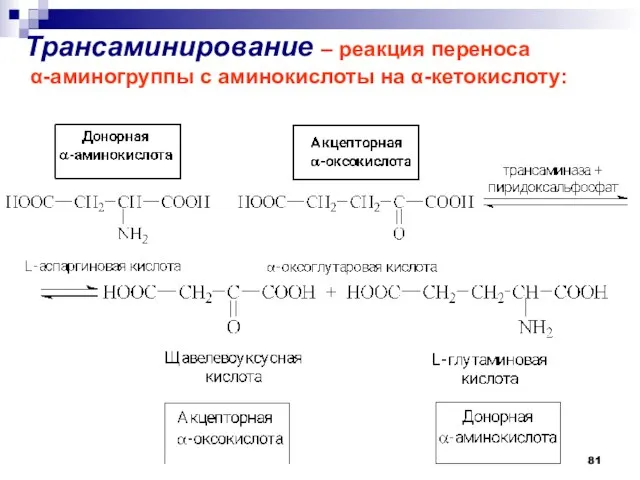
- 81. Трансаминирование – реакция переноса α-аминогруппы с аминокислоты на α-кетокислоту:
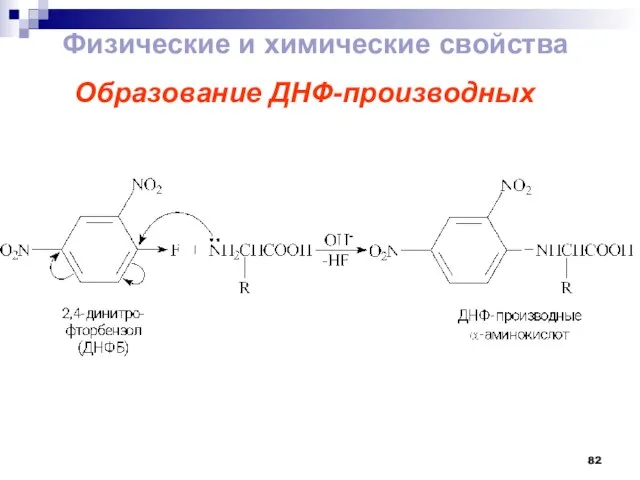
- 82. Образование ДНФ-производных Физические и химические свойства
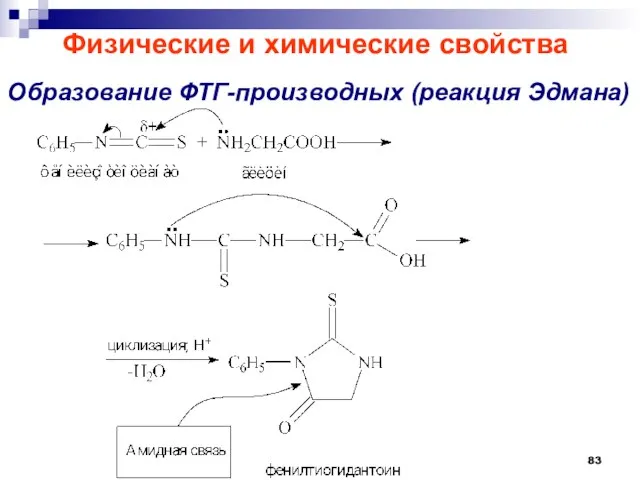
- 83. Образование ФТГ-производных (реакция Эдмана) Физические и химические свойства
- 84. 1.Образование эфиров глицин — кристаллическое вещество с Тпл=292°С метиловый эфир глицина — жидкость с Ткип=130°С. Реакции,
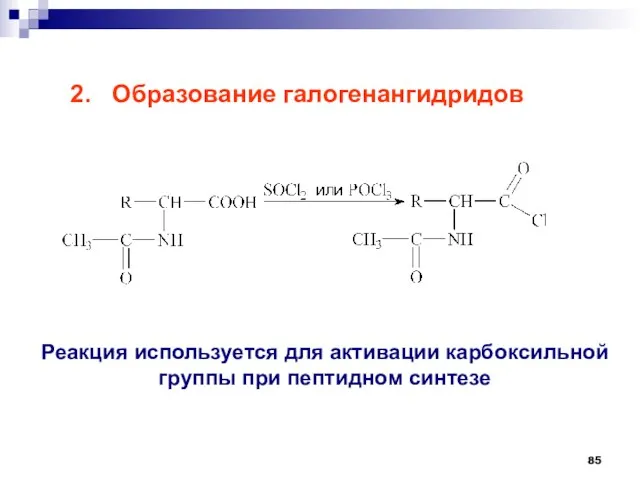
- 85. 2. Образование галогенангидридов Реакция используется для активации карбоксильной группы при пептидном синтезе
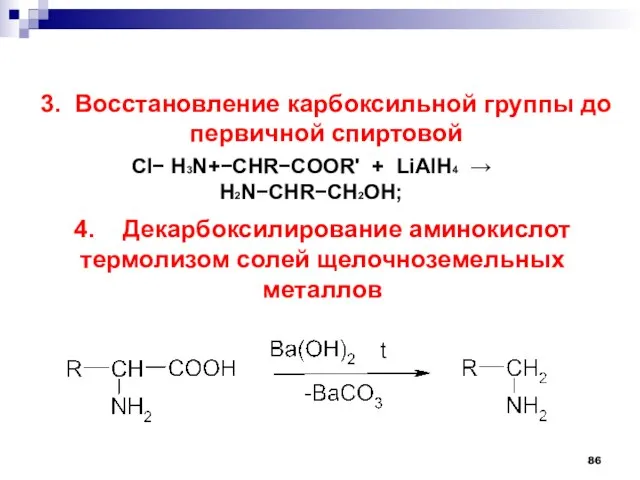
- 86. 3. Восстановление карбоксильной группы до первичной спиртовой Cl H3N+CHRCOOR' + LiAlH4 H2NCHRCH2OH; 4. Декарбоксилирование аминокислот
- 87. Процесс декарбоксилирования -аминокислот в организме ведет к образованию биогенных аминов
- 88. Путресцин- 1,4-диаминобутан, образующийся в толстой кишке при ферментативном декарбоксилировании орнитина; при цистинурии обнаруживается в моче. Кадаверин-(лат.
- 89. Ферментативное гидроксилирование При генетически обусловленном отсутствии в организме фермента, катализирующего этот процесс, развивается тяжелое заболевание —
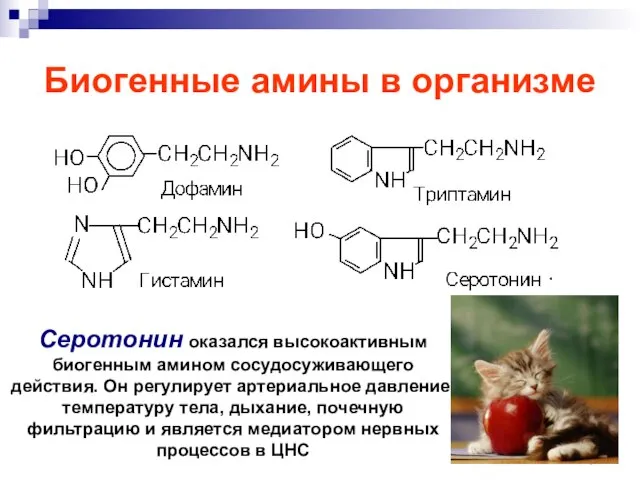
- 90. Биогенные амины в организме Серотонин оказался высокоактивным биогенным амином сосудосуживающего действия. Он регулирует артериальное давление, температуру
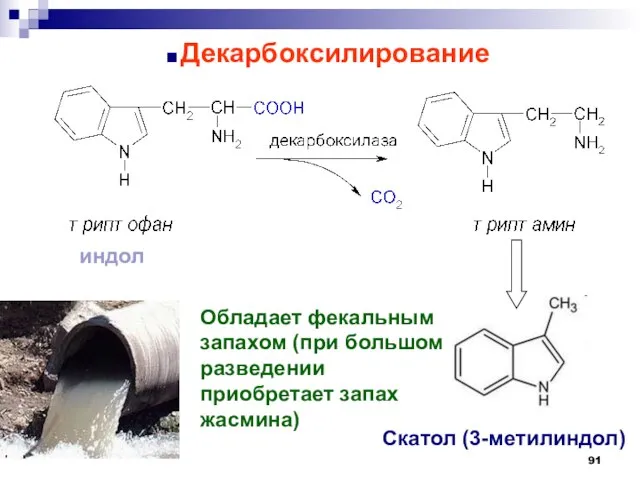
- 91. Декарбоксилирование Обладает фекальным запахом (при большом разведении приобретает запах жасмина) Скатол (3-метилиндол) индол
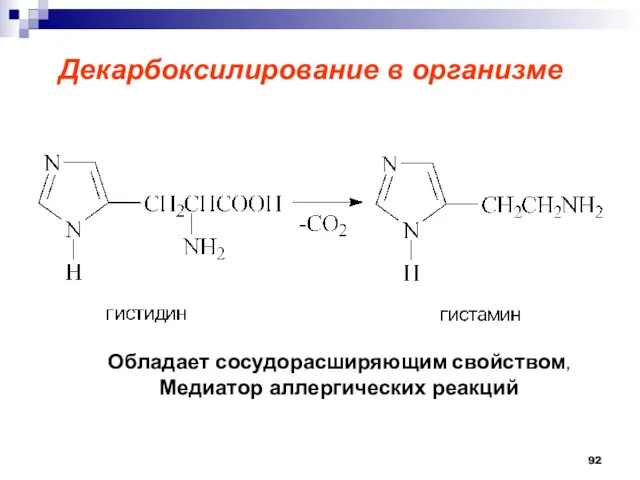
- 92. Декарбоксилирование в организме Обладает сосудорасширяющим свойством, Медиатор аллергических реакций
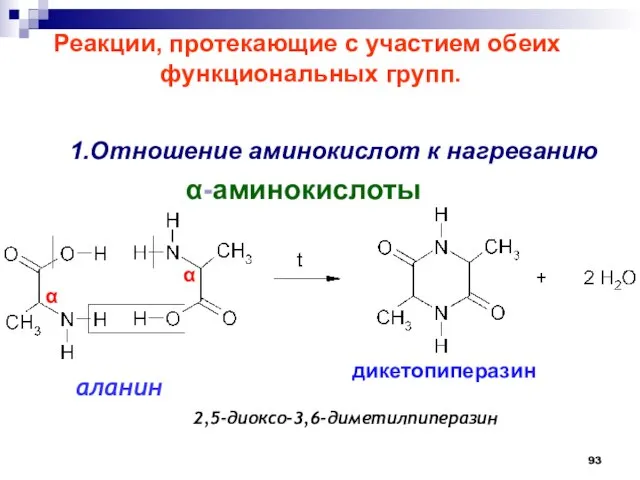
- 93. 1.Отношение аминокислот к нагреванию -аминокислоты Реакции, протекающие с участием обеих функциональных групп. 2,5-диоксо-3,6-диметилпиперазин дикетопиперазин аланин α
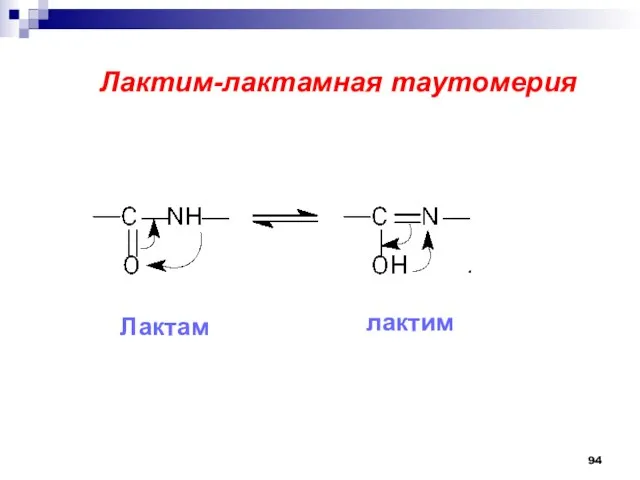
- 94. Лактим-лактамная таутомерия Лактам лактим
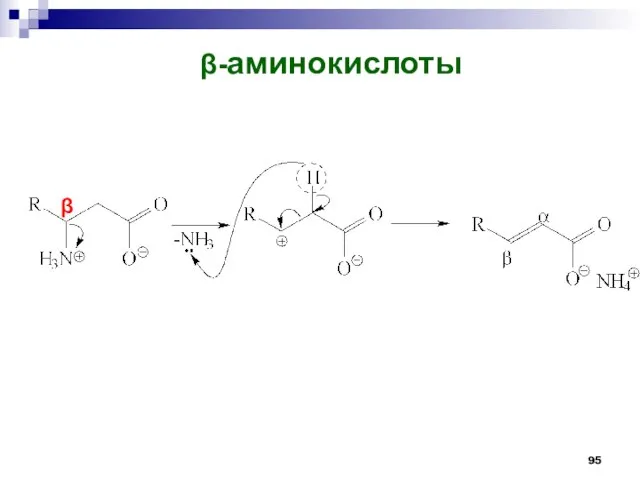
- 95. -аминокислоты
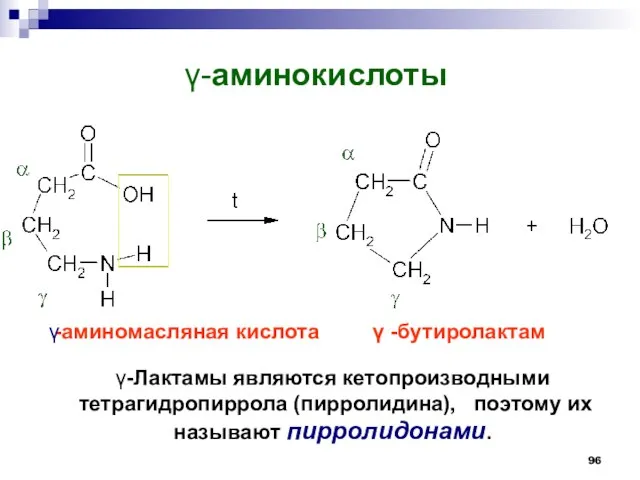
- 96. -аминокислоты -Лактамы являются кетопроизводными тетрагидропиррола (пирролидина), поэтому их называют пирролидонами. -аминомасляная кислота -бутиролактам
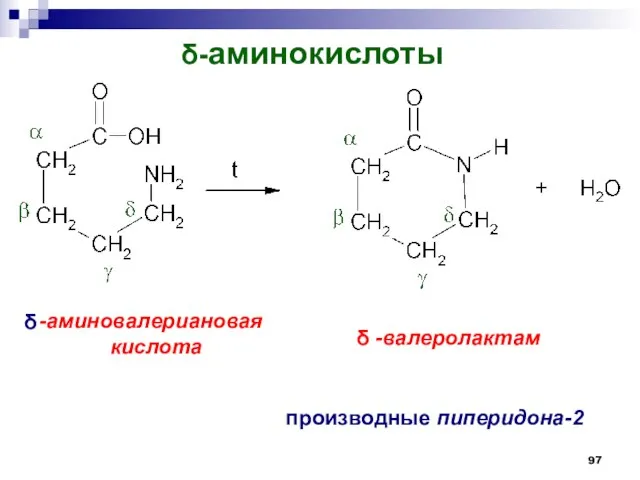
- 97. -аминокислоты производные пиперидона-2 -аминовалериановая кислота -валеролактам
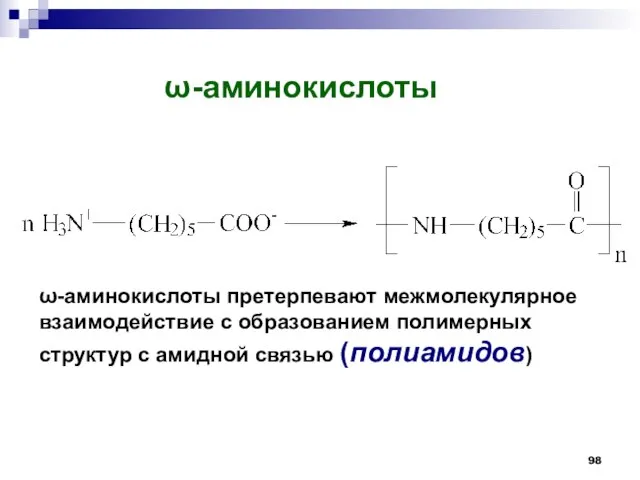
- 98. -аминокислоты -аминокислоты претерпевают межмолекулярное взаимодействие с образованием полимерных структур с амидной связью (полиамидов)
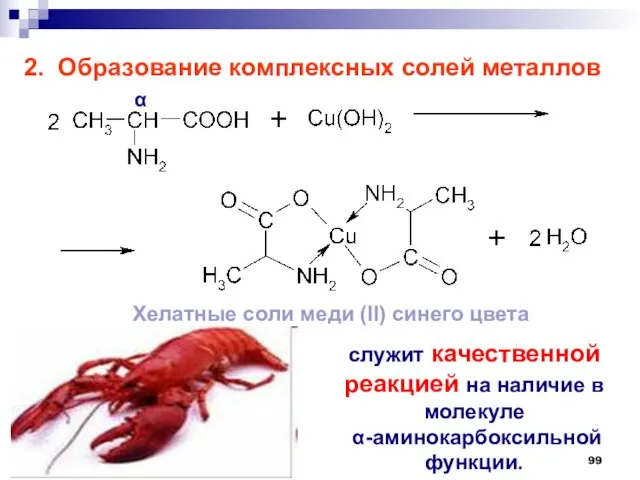
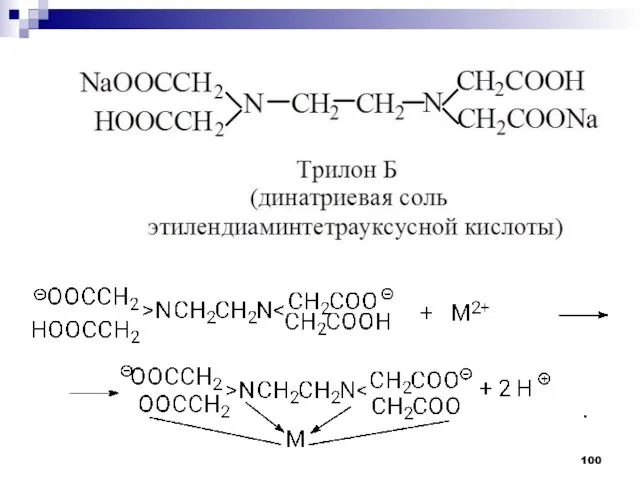
- 99. 2. Образование комплексных солей металлов служит качественной реакцией на наличие в молекуле -аминокарбоксильной функции. Хелатные
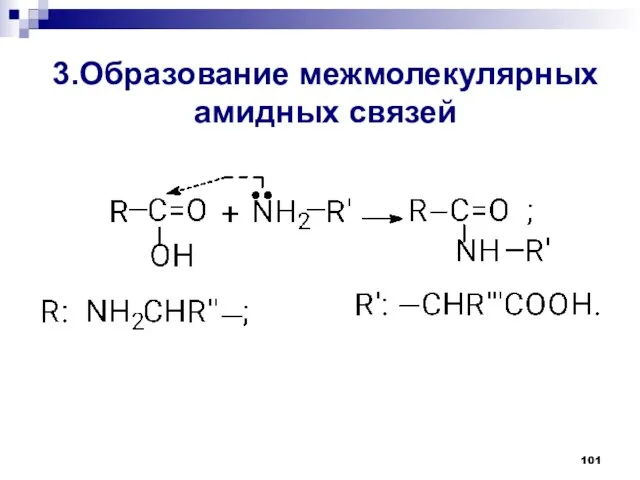
- 101. 3.Образование межмолекулярных амидных связей
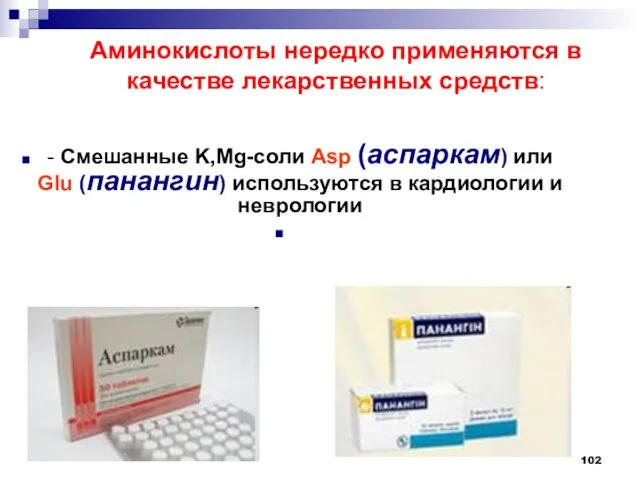
- 102. Аминокислоты нередко применяются в качестве лекарственных средств: - Смешанные K,Mg-соли Asp (аспаркам) или Glu (панангин) используются
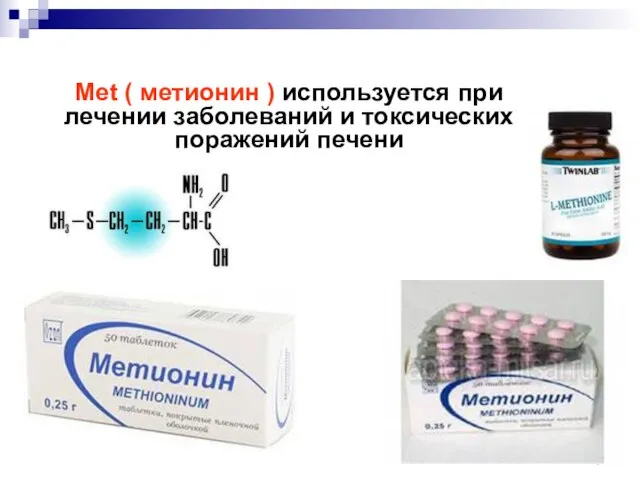
- 103. Met ( метионин ) используется при лечении заболеваний и токсических поражений печени
- 104. Cys (цистеин) участвуя в обмене веществ хрусталика глаза, полезен для профилактики и задержки развития некоторых типов
- 105. うま味 Умами - “мясной вкус” Глутаминовая кислота (E620) и её соли: (глутамат натрия Е621, глутамат калия
- 106. Глутаминовая кислота и её соли безопасны! Глутамат натрия разрешено добавлять к продуктам питания в количестве 1,5
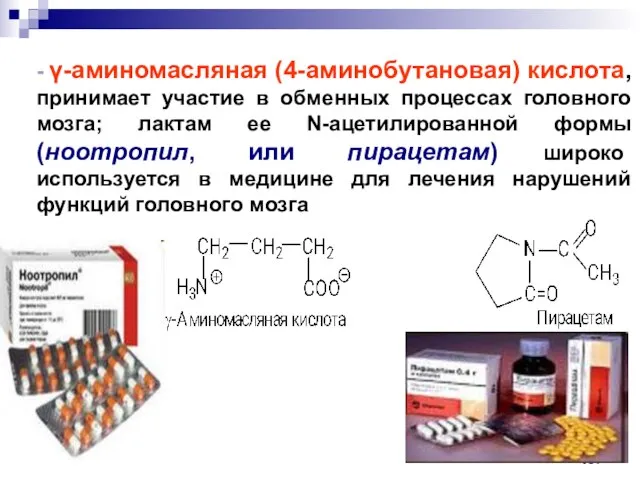
- 107. - -аминомасляная (4-аминобутановая) кислота, принимает участие в обменных процессах головного мозга; лактам ее N-ацетилированной формы (ноотропил,
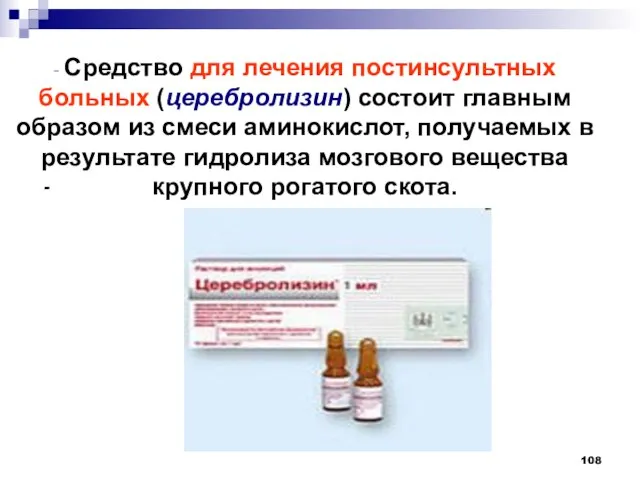
- 108. - Средство для лечения постинсультных больных (церебролизин) состоит главным образом из смеси аминокислот, получаемых в результате
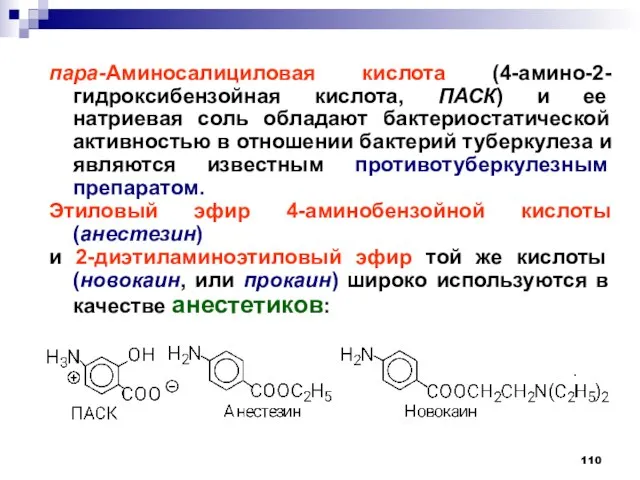
- 110. пара-Аминосалициловая кислота (4-амино-2-гидроксибензойная кислота, ПАСК) и ее натриевая соль обладают бактериостатической активностью в отношении бактерий туберкулеза
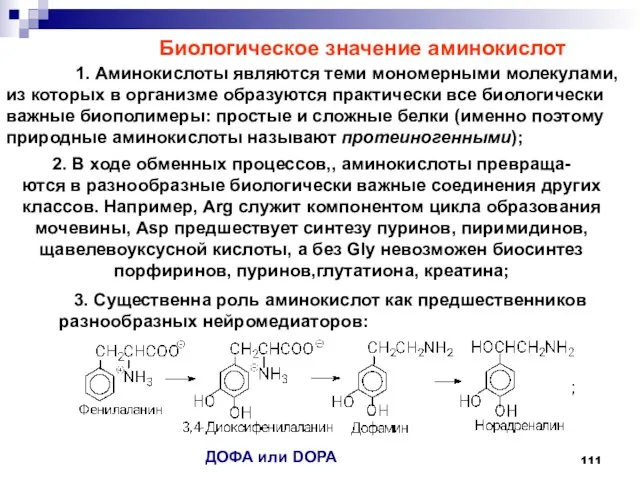
- 111. Биологическое значение аминокислот 1. Аминокислоты являются теми мономерными молекулами, из которых в организме образуются практически все
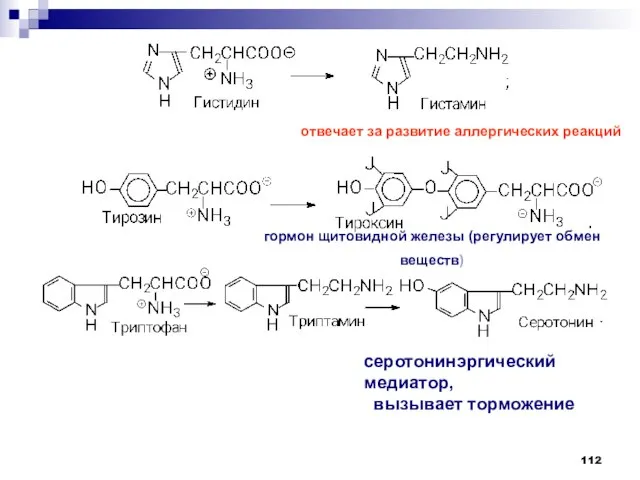
- 112. отвечает за развитие аллергических реакций гормон щитовидной железы (регулирует обмен веществ) серотонинэргический медиатор, вызывает торможение
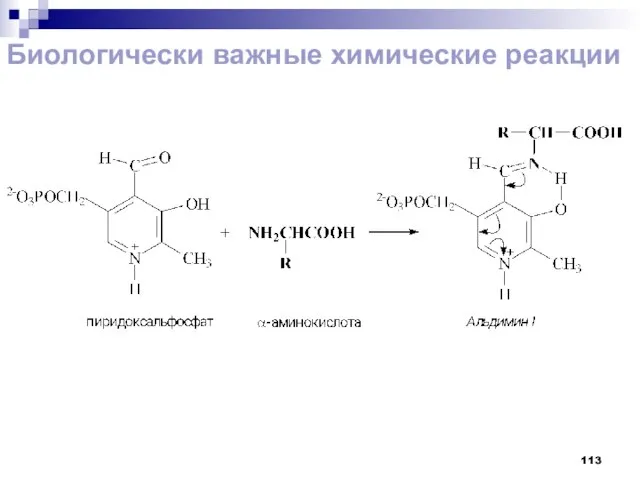
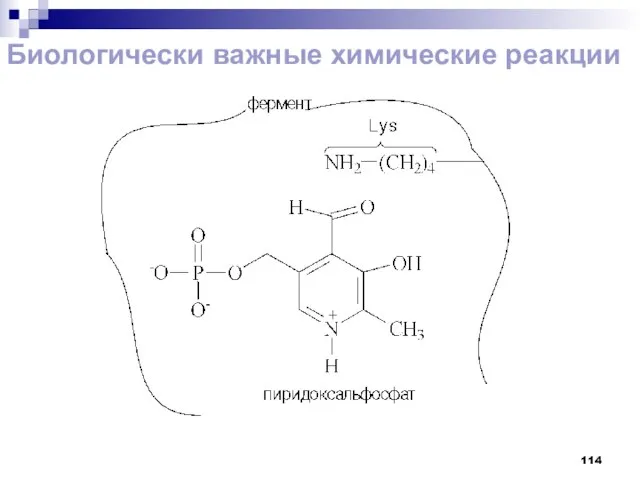
- 113. Биологически важные химические реакции
- 114. Биологически важные химические реакции
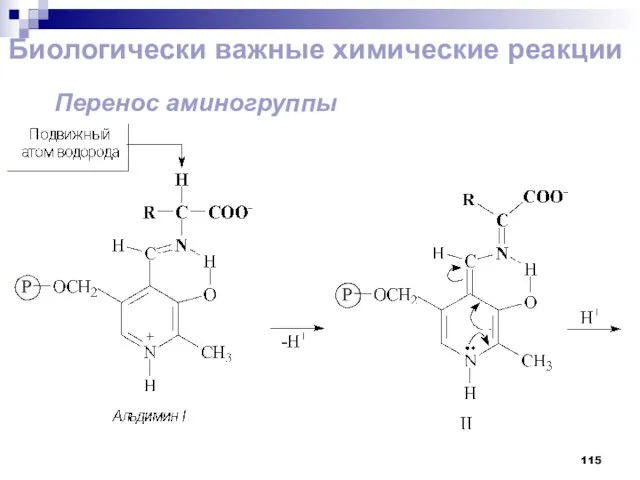
- 115. Биологически важные химические реакции Перенос аминогруппы
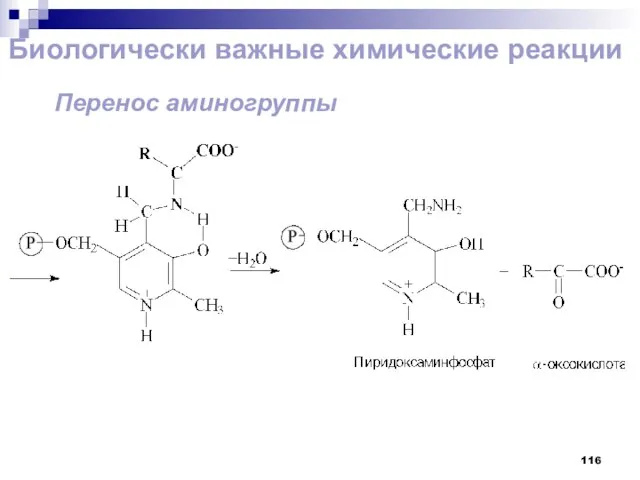
- 116. Биологически важные химические реакции Перенос аминогруппы
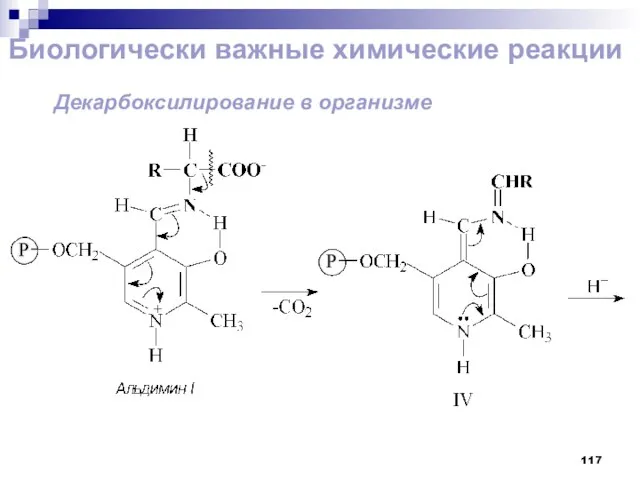
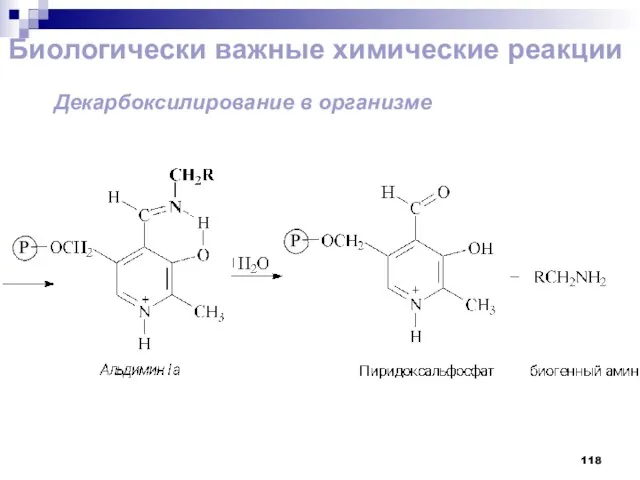
- 117. Биологически важные химические реакции Декарбоксилирование в организме
- 118. Биологически важные химические реакции Декарбоксилирование в организме
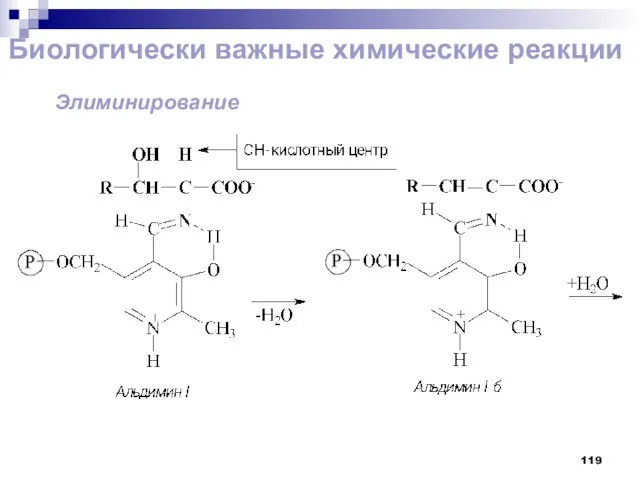
- 119. Биологически важные химические реакции Элиминирование
- 121. Скачать презентацию




































 Курсовая работа по дисциплине “Математические методы” на тему “Игры с природой”
Курсовая работа по дисциплине “Математические методы” на тему “Игры с природой” Terex RS446 Регенератор / Стабилизатор
Terex RS446 Регенератор / Стабилизатор Определи падеж.
Определи падеж. Определение количества информации
Определение количества информации ОЗК и противогазы. Назначение, устройство и принцип действия
ОЗК и противогазы. Назначение, устройство и принцип действия Русский терем
Русский терем Пижамные брюки. Обработка верхнего среза пижамных брюк притачным поясом
Пижамные брюки. Обработка верхнего среза пижамных брюк притачным поясом Муниципальное дошкольное образовательное учреждение «Детский сад № 47» Рожкова Галина Ивановна Попеляева Галина Константиновна
Муниципальное дошкольное образовательное учреждение «Детский сад № 47» Рожкова Галина Ивановна Попеляева Галина Константиновна Исследование прибрежных преобразователей энергии волн
Исследование прибрежных преобразователей энергии волн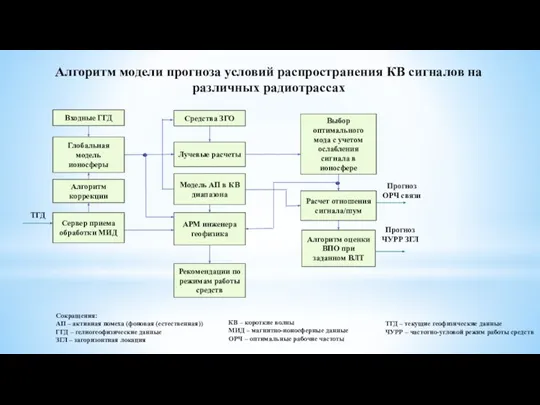 Алгоритм модели прогноза условий распространения КВ сигналов на различных радиотрассах
Алгоритм модели прогноза условий распространения КВ сигналов на различных радиотрассах История Владимирского края
История Владимирского края Педагогический анализ работы МОУ «Казначеевская СОШ» за 2007-2008 учебный год.
Педагогический анализ работы МОУ «Казначеевская СОШ» за 2007-2008 учебный год. Делимость чисел
Делимость чисел Сетевые ОС
Сетевые ОС ПРИМЕНЕНИЕ ОНТОЛОГИЙ ПРИ ПОСТРОЕНИИ ТЕСТОВ ДЛЯ ПРОВЕРКИ УРОВНЯ ПОДГОТОВКИ ОБУЧАЕМЫХ
ПРИМЕНЕНИЕ ОНТОЛОГИЙ ПРИ ПОСТРОЕНИИ ТЕСТОВ ДЛЯ ПРОВЕРКИ УРОВНЯ ПОДГОТОВКИ ОБУЧАЕМЫХ Тема:«Бросание мяча под определёнными углами к горизонту для попадания в площадную цель»
Тема:«Бросание мяча под определёнными углами к горизонту для попадания в площадную цель» Компания ТОО GFcom. Оптово-розничная компания, входящая в список лидеров по продаже автокомпонентов на территории Казахстана
Компания ТОО GFcom. Оптово-розничная компания, входящая в список лидеров по продаже автокомпонентов на территории Казахстана Цветовые наименования в творчестве
Цветовые наименования в творчестве Риск и промышленная безопасность
Риск и промышленная безопасность  ЛЮДИ
ЛЮДИ Приобретение гражданства в России1
Приобретение гражданства в России1 AOUT/May01 Влияние качества смазочных материалов на агрегаты гидросистем.
AOUT/May01 Влияние качества смазочных материалов на агрегаты гидросистем. Выполнение болевых приёмов при подходе к правонарушителю спереди
Выполнение болевых приёмов при подходе к правонарушителю спереди ?
? Природные достопримечательности Румынии
Природные достопримечательности Румынии  Мировой посредник
Мировой посредник Автоматизация звука Р в 2-3х сложных словах
Автоматизация звука Р в 2-3х сложных словах Почвогрунты для улучшения качества почвы
Почвогрунты для улучшения качества почвы