Содержание
- 2. Тема урока. Микропараметры вещества 1. Молекулярная физика 1.1. Основы МКТ План урока 2. Размеры молекул. 3.
- 3. СОЗДАТЕЛИ АТОМНОЙ ТЕОРИИ Джон Дмитрий Дальтон Менделеев Амедео Эрнест Авогадро Резерфорд
- 4. Микропараметры вещества характеризуют каждую частицу вещества в отдельности, в отличие от макропараметров, характеризующих вещество в целом.
- 5. Основные положения МКТ • Все тела состоят из малых частиц, между которыми есть промежутки. • Частицы
- 6. ПЕРВОЕ ПОЛОЖЕНИЕ 1. Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц –
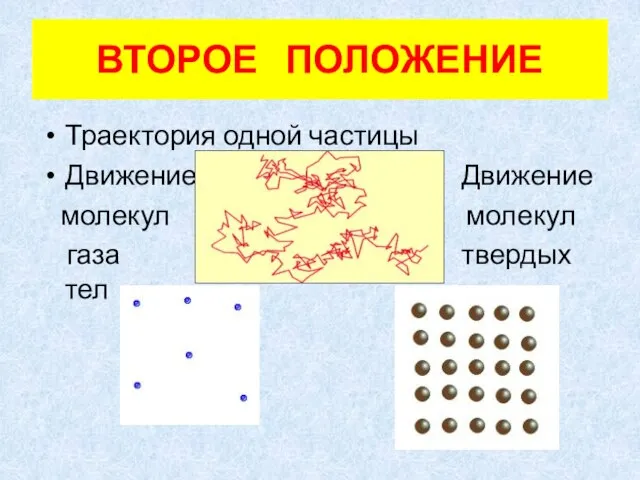
- 7. ВТОРОЕ ПОЛОЖЕНИЕ Траектория одной частицы Движение Движение молекул молекул газа твердых тел
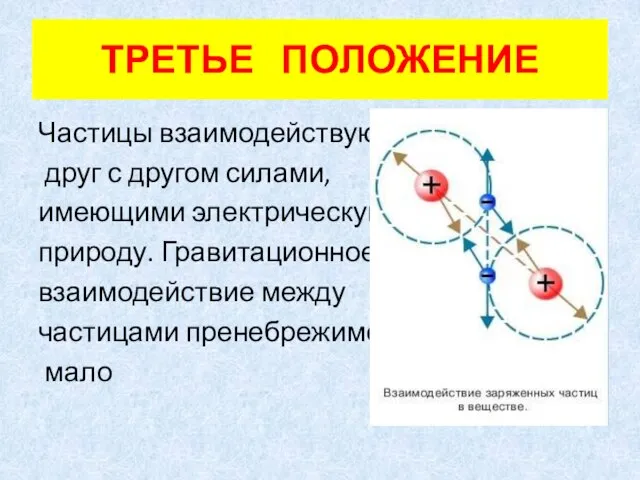
- 8. ТРЕТЬЕ ПОЛОЖЕНИЕ Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо
- 9. ОПЫТНЫЕ ПОДТВЕРЖДЕНИЯ I положение 1. Дробление вещества 2. Испарение жидкостей 3. Расширение тел при нагревании
- 10. II положение 1. Диффузия – перемешивание молекул разных веществ 2.Броуновское движение – движение взвешенных в жидкости
- 11. III положение Силы упругости Прилипание свинцовых цилиндров Смачивание Поверхностное натяжение ОПЫТНЫЕ ПОДТВЕРЖДЕНИЯ
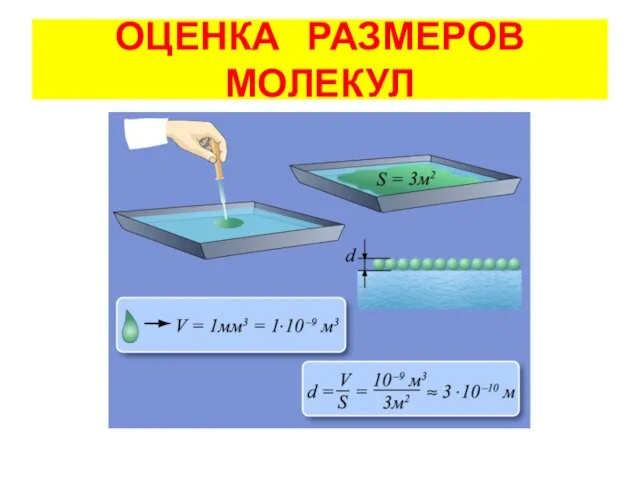
- 12. ОЦЕНКА РАЗМЕРОВ МОЛЕКУЛ
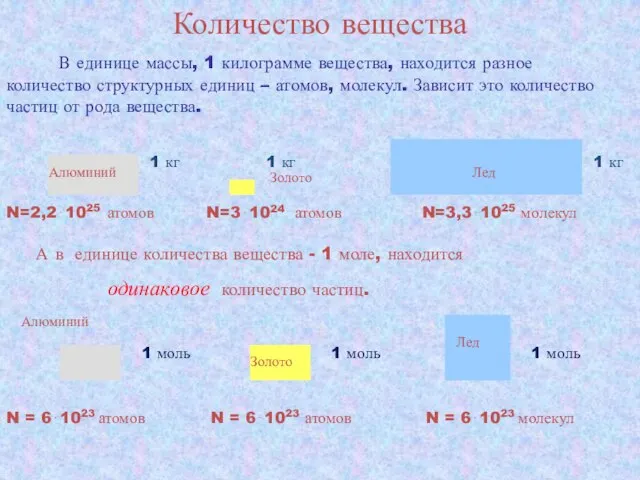
- 13. Количество вещества В единице массы, 1 килограмме вещества, находится разное количество структурных единиц – атомов, молекул.
- 14. КОЛИЧЕСТВО ВЕЩЕСТВА В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу частиц. Единица количества вещества называется
- 15. ФОРМУЛЫ
- 16. В одном моле любого вещества содержится одно и то же число частиц (молекул). Это число называется
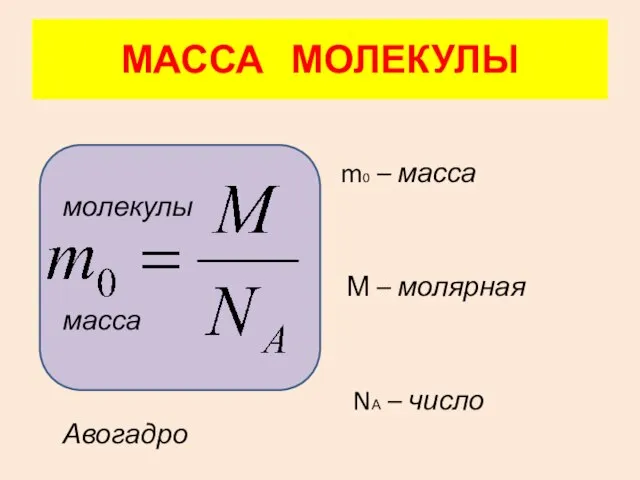
- 17. МАССА МОЛЕКУЛЫ m0 – масса молекулы М – молярная масса NА – число Авогадро
- 18. ЗАДАЧИ 1. Рассчитать массу молекулы Н2SО4. М(Н2SО4) = 2·1 + 32 + 16·4 = 98 г/моль
- 19. 2. Сколько молекул содержится в 50г Аℓ? М(Аℓ) = 27г/моль N = νNA ν = m/M
- 21. Скачать презентацию













 1. Доходы
1. Доходы AMANAT INVEST GROUP High Tech Logistic» Ответственное хранение грузов Ответственное хранение грузов Весь спектор операций на складе Весь спектор о
AMANAT INVEST GROUP High Tech Logistic» Ответственное хранение грузов Ответственное хранение грузов Весь спектор операций на складе Весь спектор о Native american boarding schools
Native american boarding schools Цель: выяснить отношение жителей г. Канска к проблеме лесных пожаров Красноярского края.
Цель: выяснить отношение жителей г. Канска к проблеме лесных пожаров Красноярского края. Презентация на тему Азбука города
Презентация на тему Азбука города Язык Рефлекс – диалект Си для программирования ПЛК
Язык Рефлекс – диалект Си для программирования ПЛК Туристический потенциал Балахнинского района
Туристический потенциал Балахнинского района О создании многофункциональных центров предоставления государственных и муниципальных услуг в 2008 году
О создании многофункциональных центров предоставления государственных и муниципальных услуг в 2008 году Дошкольный, школьный и подростковый возраст. Градация детского возраста на группы в СК Планета Фитнес
Дошкольный, школьный и подростковый возраст. Градация детского возраста на группы в СК Планета Фитнес Я и полиция
Я и полиция Различай С - З
Различай С - З Класс Земноводные или Амфибии 7 класс
Класс Земноводные или Амфибии 7 класс Проект Народные инициативы в 2018 году в городе Шелехове
Проект Народные инициативы в 2018 году в городе Шелехове Понятие судебных доказательств
Понятие судебных доказательств Универсальный лазерный гравировальный станок для неметаллов. Wattsan 2030FLAT BED
Универсальный лазерный гравировальный станок для неметаллов. Wattsan 2030FLAT BED Спортивная динейка. Подведение итогов
Спортивная динейка. Подведение итогов МОУ "Аликовская СОШ им. И.Я. Яковлева" Аликовского района Чувашской Республики
МОУ "Аликовская СОШ им. И.Я. Яковлева" Аликовского района Чувашской Республики Пусть меня научат - презентация для начальной школы_
Пусть меня научат - презентация для начальной школы_ Обучение технике ударов по мячу в футболе
Обучение технике ударов по мячу в футболе Понятие и виды деловой карьеры
Понятие и виды деловой карьеры Презентация на тему Славянская мифология
Презентация на тему Славянская мифология  Nanotechnologies: potential benefits or a great danger?
Nanotechnologies: potential benefits or a great danger? Обычно землетрясения происходят вблизи границ литосферных плит. Эти плиты находятся в постоянном движении. Плиты движутся по гори
Обычно землетрясения происходят вблизи границ литосферных плит. Эти плиты находятся в постоянном движении. Плиты движутся по гори Неповторимые, эксклюзивные коллекции ограниченной серии. De Luxe
Неповторимые, эксклюзивные коллекции ограниченной серии. De Luxe Организационная структура страховой компании. Понятие
Организационная структура страховой компании. Понятие СОЧЕТАННЫЕ (СИМУЛЬТАННЫЕ) ОПЕРАЦИИ В ЛАПАРОСКОПИЧЕСКОЙ ХИРУРГИИ
СОЧЕТАННЫЕ (СИМУЛЬТАННЫЕ) ОПЕРАЦИИ В ЛАПАРОСКОПИЧЕСКОЙ ХИРУРГИИ NUMUNE ALIMI ve TRANSFERi
NUMUNE ALIMI ve TRANSFERi Общие положения по монтажу внутренних газопроводов и газоиспользующего оборудования
Общие положения по монтажу внутренних газопроводов и газоиспользующего оборудования