Слайд 2Цель:
Изучение строения атомов щелочноземельных металлов, физических и химических свойств.

Слайд 3Положение в периодической таблице
Be Mg Ca Sr Ba Ra
Восстановительные свойства усиливаются

Слайд 4Строение атома
+4 ) )
+12 ) ) )
+20 ) ) )

)
+38 ) ) ) ) )
+56 ) ) ) ) ) )
Ве
Mg
Ca
Sr
Ba
2
2
2
2
2
Слайд 5Распишите электронные формулы всех элементов
6
3S
Ве
Mg

Слайд 6Физические свойства щелочноземельных металлов.
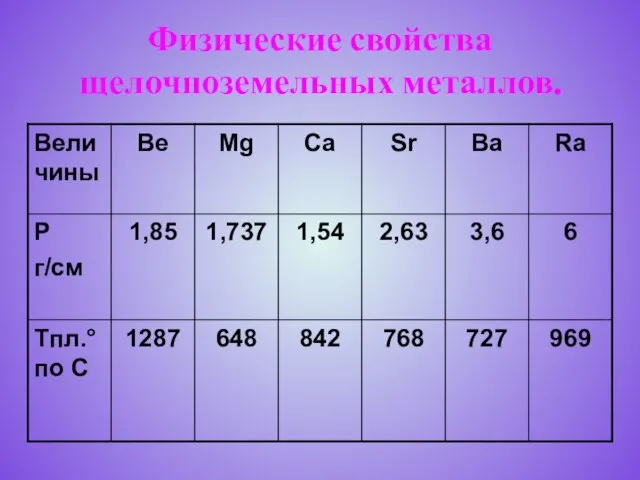
Слайд 7Химические свойства
1.Взаимодйествие с простыми веществами:
А) с кислородом
2Са+ О2= 2СаО
Б) с галогенами
Са +Сl2=

CaCl2
В) с водородом
Са +Н2 = СаН2
Г) с азотом
3Са + N2 = Ca3N2
Слайд 8Химические свойства
2. Взаимодействие со сложными веществами.
а) с водой
Са + 2Н2О = Са(ОН)2

+ Н2
б) с солями менее активных металлов
Mg +CuSO4 =Cu +MgSO4
в) с оксидами металлов
FeO + Mg = MgO +Fe
Его используют для получения чистых металлов из оксидов. Этот способ получил название магниотермия.
Слайд 9Mg +2HCl = MgCl2 +H2
Са с разбавленными кислотами не реагирует
Взаимодействие с кислотами

Слайд 10Соединения щелочноземельных металлов

Слайд 11Выполните следующее задание:
Решить задачу №1после §12
Осуществить превращения:
Ca → CaO→ CaCl2→ Ca(OH)2 →
CaCO3

→CaO










 Круглый стол для потенциальных участников закупки работ по СМР для АО НК Конданефть
Круглый стол для потенциальных участников закупки работ по СМР для АО НК Конданефть Что такое Пассивный доход
Что такое Пассивный доход Презентация на тему Садоводство и виноградарство
Презентация на тему Садоводство и виноградарство  Зачем региональной компании перестраховщик
Зачем региональной компании перестраховщик Магазин IT- услуг
Магазин IT- услуг Презентация на тему Осторожно - электроприборы!
Презентация на тему Осторожно - электроприборы! Процедуры и функции. Модули
Процедуры и функции. Модули Дарите нужные подарки!
Дарите нужные подарки! Организм человека
Организм человека 1.3.2. Определение количества информации.
1.3.2. Определение количества информации. СОТРУДНИЧЕСТВО С КНР ОПЫТ ВТБ МАРТ 2011
СОТРУДНИЧЕСТВО С КНР ОПЫТ ВТБ МАРТ 2011 Бурый медведь 2 класс
Бурый медведь 2 класс Презентация на тему Учим словарь со смешариками 1 класс
Презентация на тему Учим словарь со смешариками 1 класс Приемы умножения единицы и нуля.
Приемы умножения единицы и нуля. Учебный курс. Технологии и средства разработки корпоративных систем. Основные возможности корпоративных приложений
Учебный курс. Технологии и средства разработки корпоративных систем. Основные возможности корпоративных приложений Занятие по развитию речи «Каникулы»
Занятие по развитию речи «Каникулы» МОРФОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА СЛОВА
МОРФОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА СЛОВА Проблемы криптопреступности и способы их решения
Проблемы криптопреступности и способы их решения Новогодняя настольная лампа "Ночь перед Рождеством"
Новогодняя настольная лампа "Ночь перед Рождеством" Development Leadership Skills
Development Leadership Skills Monash Road, Loganlea
Monash Road, Loganlea Социальная структура общества
Социальная структура общества  ПЕРСПЕКТИВЫ МЕДИЦИНСКОГО ОБРАЗОВАНИЯ В РОССИИ: НОВЫЕ ОБРАЗОВАТЕЛЬНЫЕ СТАНДАРТЫ.
ПЕРСПЕКТИВЫ МЕДИЦИНСКОГО ОБРАЗОВАНИЯ В РОССИИ: НОВЫЕ ОБРАЗОВАТЕЛЬНЫЕ СТАНДАРТЫ. Комикс «Самая скорая помощь» Переохлаждение в воде
Комикс «Самая скорая помощь» Переохлаждение в воде Как стать сказочником?
Как стать сказочником? Технологии и продукты Microsoft в обеспечении ИБ
Технологии и продукты Microsoft в обеспечении ИБ Вышивка тамбурным швом
Вышивка тамбурным швом Книжная полка
Книжная полка