Содержание
- 2. Самое необыкновенное вещество в мире
- 3. H2O
- 4. 1H — протий (Н) 2H — дейтерий (D) 3H — тритий(T)
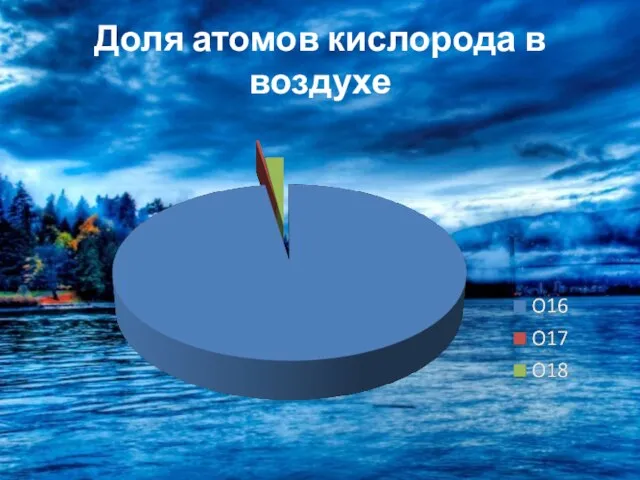
- 5. Доля атомов кислорода в воздухе
- 6. Лёгкая вода 1H2016
- 7. Тяжёлая вода́ (также оксид дейтерия) — обычно этот термин применяется для обозначения тяжёловодородной воды. Тяжёловодородная вода
- 8. Радиоактивная вода Тритиевая вода (сверхтяжелая вода) — вода, в молекулах которой атомы водорода замещены атомами трития.
- 9. 1 литр воды= =100 кг. угля
- 10. 1H — протий (Н)1,007825 2H — дейтерий (D) 2,014102 3H — тритий(T)3,016049
- 11. Ядерная Реакция между атомами дейтерия(тяжелого водорода) D2+D2=>H1+T3
- 12. 2*2.014102-1.007825-3.016049=0.004330а.е.м.
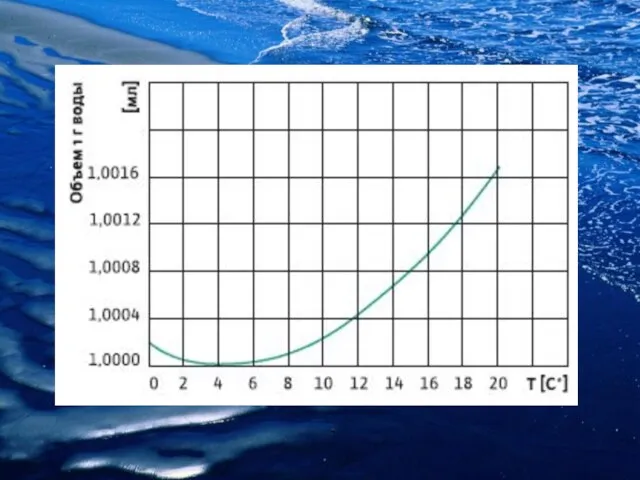
- 13. Аномалия воды Все природные материалы расширяются при нагревании и сжимаются при охлаждении. Единственным исключением из этого
- 15. При плавлении льда образуются крупные сложные молекулы воды. Они сохраняют остатки кристаллической структуры льда и растворены
- 17. Скачать презентацию












 Наблюдения за семьёй серых ворон в гнездовой период
Наблюдения за семьёй серых ворон в гнездовой период Застосування рідких кристалів
Застосування рідких кристалів Презентация на тему Пять мифов о лидерстве
Презентация на тему Пять мифов о лидерстве Православные храмы
Православные храмы МАГНЕТРОННЫЕ РАСПЫЛИТЕЛЬНЫЕ СИСТЕМЫ
МАГНЕТРОННЫЕ РАСПЫЛИТЕЛЬНЫЕ СИСТЕМЫ День Святой Троицы
День Святой Троицы Презентация на тему Конкуренция. Конкуренты
Презентация на тему Конкуренция. Конкуренты ВЕЛИКИЕ ГЕОГРАФИЧЕСКИЕ ОТКРЫТИЯ XV – XVII ВЕКОВ УРОК – ИГРА «КЛУБ ЗНАТОКОВ»
ВЕЛИКИЕ ГЕОГРАФИЧЕСКИЕ ОТКРЫТИЯ XV – XVII ВЕКОВ УРОК – ИГРА «КЛУБ ЗНАТОКОВ» Псалом 31. Блажен оставивший беззаконие
Псалом 31. Блажен оставивший беззаконие ОПЫТ И НАПРАВЛЕНИЯ ВЗАИМОДЕЙСТВИЯ ВЕНДОРОВ И УЧЕБНО-МЕТОДИЧЕСКИХ ОБЪЕДИНИЙ ВУЗОВ В СФЕРЕ ИКТ
ОПЫТ И НАПРАВЛЕНИЯ ВЗАИМОДЕЙСТВИЯ ВЕНДОРОВ И УЧЕБНО-МЕТОДИЧЕСКИХ ОБЪЕДИНИЙ ВУЗОВ В СФЕРЕ ИКТ History of Philip Morris Company
History of Philip Morris Company Возможности и перспективы реализации профессиональных интересов молодых педагогов
Возможности и перспективы реализации профессиональных интересов молодых педагогов Доступный тайм-менеджмент и целедостижение в профессиональной деятельности педагога для профилактики эмоционального выгорания
Доступный тайм-менеджмент и целедостижение в профессиональной деятельности педагога для профилактики эмоционального выгорания Презентация на тему Война 1812 года
Презентация на тему Война 1812 года  УЧАСТИЕ ГРАЖДАН В ПОЛИТИЧЕСКОЙ ЖИЗНИ СТРАНЫ
УЧАСТИЕ ГРАЖДАН В ПОЛИТИЧЕСКОЙ ЖИЗНИ СТРАНЫ Москва, 2010
Москва, 2010 Жизнь и творчество И.С.Тургенева 1818 -1883
Жизнь и творчество И.С.Тургенева 1818 -1883 Marketion – сервис для ваших массовых рассылок
Marketion – сервис для ваших массовых рассылок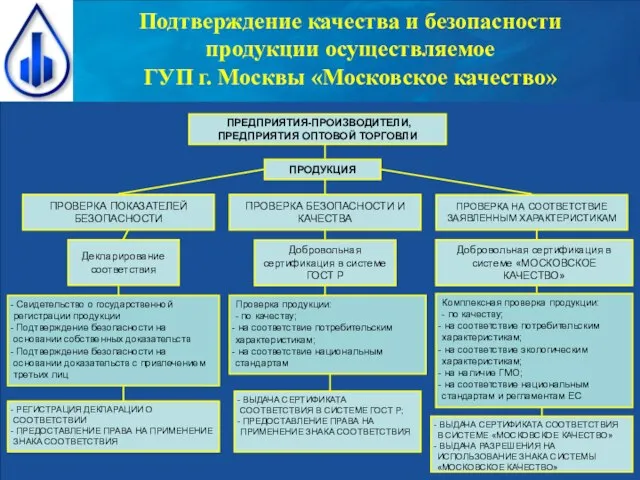 Подтверждение качества и безопасности продукции осуществляемое ГУП г. Москвы «Московское качество»
Подтверждение качества и безопасности продукции осуществляемое ГУП г. Москвы «Московское качество» Папка классного руководителяПолещук Татьяны Васильевныучителя первой квалификационной категории
Папка классного руководителяПолещук Татьяны Васильевныучителя первой квалификационной категории Презентация на тему Экосистемы арктических пустынь и тундры
Презентация на тему Экосистемы арктических пустынь и тундры  Планируемые результаты освоения обучающимися основной образовательной программы НОО
Планируемые результаты освоения обучающимися основной образовательной программы НОО Театр Древней Греции
Театр Древней Греции Приделы и неопредилености Бураковсая
Приделы и неопредилености Бураковсая Рекламное бюро. Создание бюро
Рекламное бюро. Создание бюро SDL Trados Studio 2009 SP3 SDL Trados Team SDL MultiTerm Team
SDL Trados Studio 2009 SP3 SDL Trados Team SDL MultiTerm Team Ономатопоэтика в манге
Ономатопоэтика в манге Хостинг, домен, работа через FileZilla
Хостинг, домен, работа через FileZilla