Содержание
- 2. Типы химических реакций По числу вступивших в реакцию веществ По тепловому эффекту По обратимости По изменению
- 3. По числу вступивших в реакцию веществ
- 4. По тепловому эффекту Экзотермические Идут с выделение теплоты S + O2 = SO2 + Q Эндотермические
- 5. По обратимости Необратимые Идут только в одном направлении Условия: образование осадка или слабого электролита (Н2О), выделение
- 6. По изменению степени окисления Идут без изменения степени окисления элементов CaCO3 = CaO + CO2 Окислительно
- 7. По механизму Ионные NaOH + HCl = NaCl + H2O Na+ + OH- + H+ +Cl-
- 9. Скачать презентацию






 Таблица умножения
Таблица умножения Ультразвук
Ультразвук Freestyle сессия «Инвестиционно-банковские услуги для фарммедсектора»
Freestyle сессия «Инвестиционно-банковские услуги для фарммедсектора» Комната девочек
Комната девочек Масалович Андрей Игоревич
Масалович Андрей Игоревич  Подготовка публичного выступления шаг за шагом
Подготовка публичного выступления шаг за шагом Программа курса Семейная фотография
Программа курса Семейная фотография Условия перехода в думающую компанию
Условия перехода в думающую компанию Олимпиада
Олимпиада Cалон «Золотой локон»Строение волоса. Дисперсные системы.
Cалон «Золотой локон»Строение волоса. Дисперсные системы. Введение в Data Mining
Введение в Data Mining Техники рисования по сырому,лессировка
Техники рисования по сырому,лессировка "Златоустовская гравюра" для детей 6-7 лет
"Златоустовская гравюра" для детей 6-7 лет Презентация на тему Образ святого Александра Невского в культуре и литературе
Презентация на тему Образ святого Александра Невского в культуре и литературе  Ко дню собора казанских святых. Удивительные факты единства православных святых земли Казанской, связанной с Пермской землей
Ко дню собора казанских святых. Удивительные факты единства православных святых земли Казанской, связанной с Пермской землей Киянка
Киянка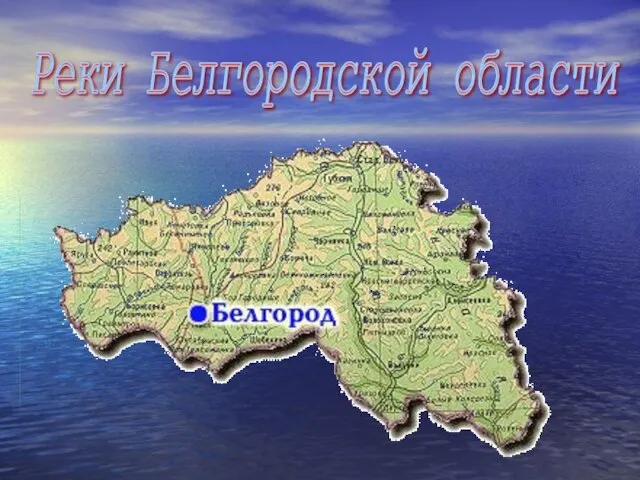 Реки Белгородской области
Реки Белгородской области Почему коробочная CMS лучше собственной
Почему коробочная CMS лучше собственной Введение ФГОС
Введение ФГОС Анализ стоимости монтажа на основе оборудования Meibes и Handmade.
Анализ стоимости монтажа на основе оборудования Meibes и Handmade. Викторина Знатоки прав
Викторина Знатоки прав Медок и его коммунальные АОС на примере ассортимента МАВТ
Медок и его коммунальные АОС на примере ассортимента МАВТ Модели атомов. Опыт Резерфорда
Модели атомов. Опыт Резерфорда Презентация на тему Турецкая республика
Презентация на тему Турецкая республика  Ключевые условия Договора Генерального Подряда
Ключевые условия Договора Генерального Подряда Презентация на тему Шаблоны для презентаций
Презентация на тему Шаблоны для презентаций  Турагенство Pegas. Обучающий семинар
Турагенство Pegas. Обучающий семинар ЗАО Балтийская Промышленная Компания
ЗАО Балтийская Промышленная Компания