Содержание
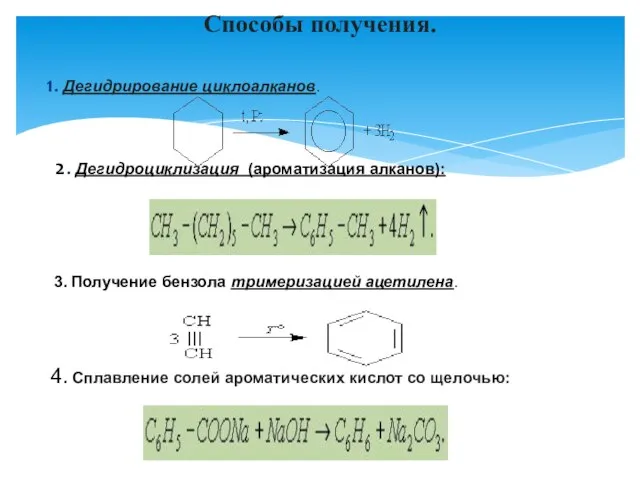
- 2. 1. Дегидрирование циклоалканов. 2. Дегидроциклизация (ароматизация алканов): 3. Получение бензола тримеризацией ацетилена. 4. Сплавление солей ароматических
- 3. Обладая подвижной шестеркой p -электронов, ароматическое ядро является удобным объектом для атаки электрофильными реагентами. Этому способствует
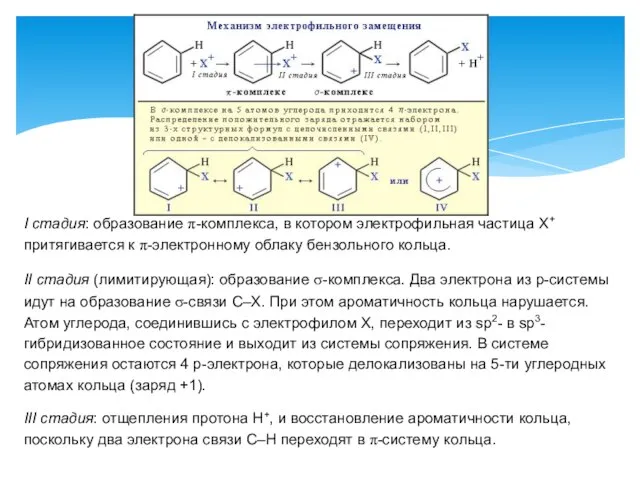
- 4. I стадия: образование π-комплекса, в котором электрофильная частица Х+ притягивается к π-электронному облаку бензольного кольца. II
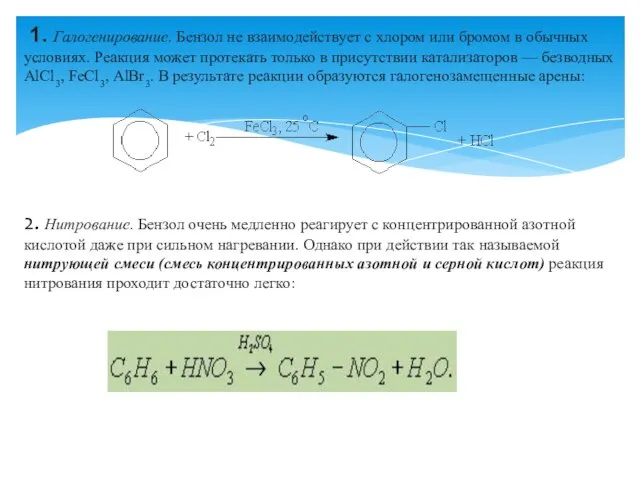
- 5. 1. Галогенирование. Бензол не взаимодействует с хлором или бромом в обычных условиях. Реакция может протекать только
- 6. 3. Алкилирование по Фриделю—Крафтсу. В результате реакции происходит введение в бензольное ядро алкильной группы с получением
- 7. 4.Алкилирование алкенами. Эти реакции широко используются в промышленности для получения этилбензола и изопропилбензола (кумола). Алкилирование проводят
- 8. Важнейшим фактором, определяющим химические свойства молекулы, является распределение в ней электронной плотности. Характер распределения зависит от
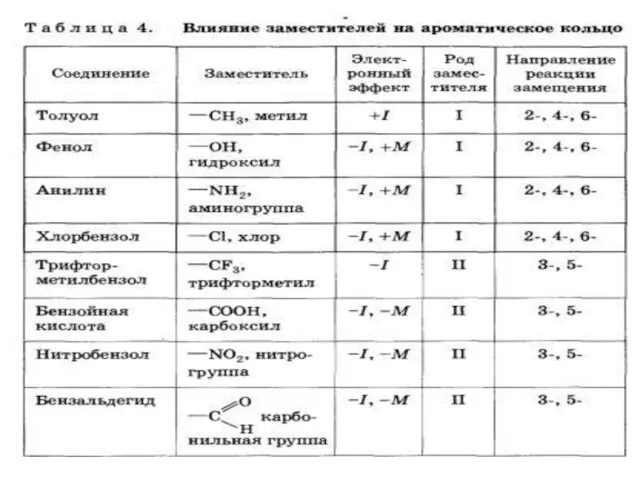
- 9. Заместители подразделяют на две группы в зависимости от проявляемого ими эффекта (мезомерного или индуктивного): 1.электронодонорные 2.электроноакцепторные.
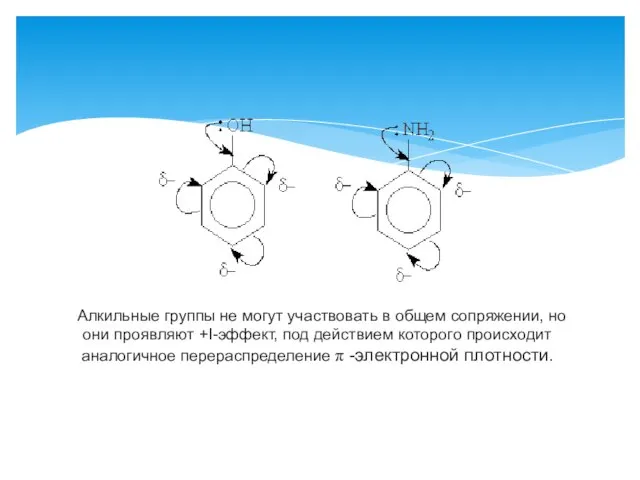
- 10. Алкильные группы не могут участвовать в общем сопряжении, но они проявляют +I-эффект, под действием которого происходит
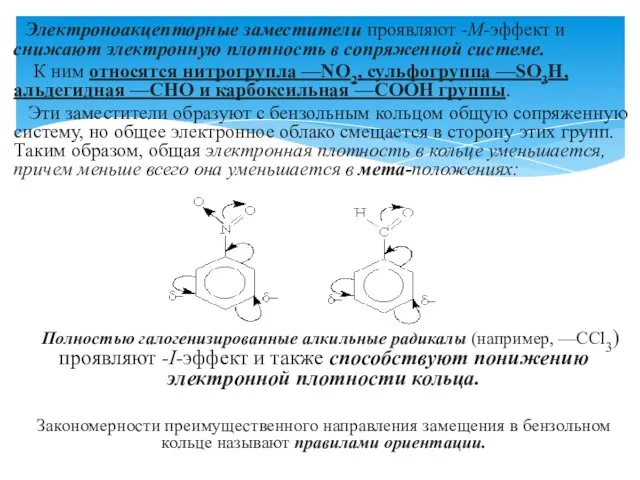
- 11. Электроноакцепторные заместители проявляют -М-эффект и снижают электронную плотность в сопряженной системе. К ним относятся нитрогрупла —NO2,
- 12. Заместители, обладающие +I-эффектом или +М-эффектом, способствуют электрофильному замещению в орто- и пара-положениях бензольного кольца и называются
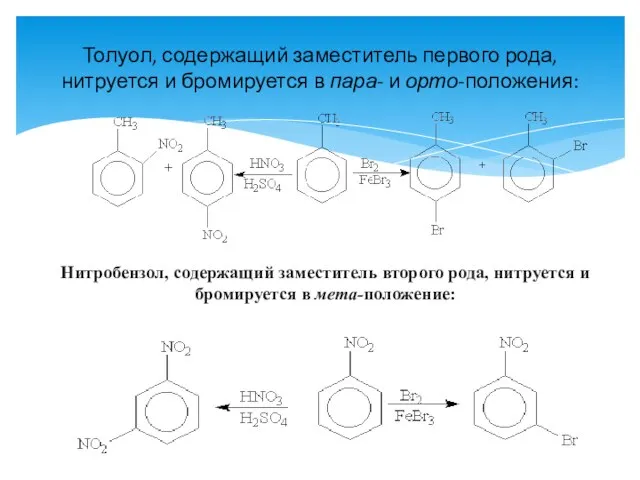
- 13. Толуол, содержащий заместитель первого рода, нитруется и бромируется в пара- и орто-положения: Нитробензол, содержащий заместитель второго
- 15. 1. Гидрирование. Реакция присоединения водорода к аренам идет при нагревании и высоком давлении в присутствии металлических
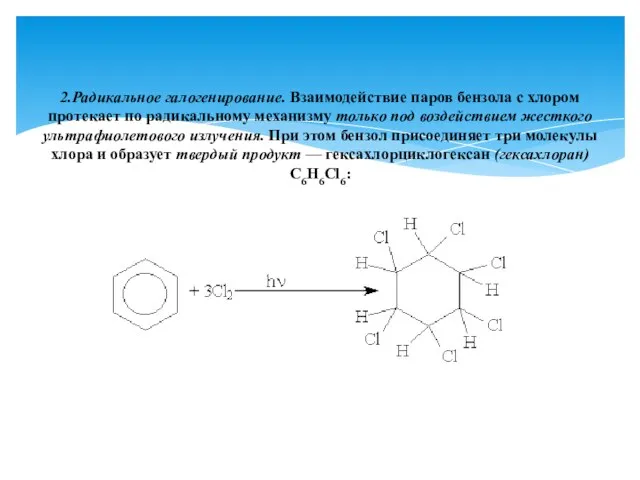
- 16. 2.Радикальное галогенирование. Взаимодействие паров бензола с хлором протекает по радикальному механизму только под воздействием жесткого ультрафиолетового
- 17. Метильная группа проявляет положительный индуктивный эффект по отношению к бензольному кольцу. Соответственно бензольное кольцо обладает отрицательным
- 19. Скачать презентацию








 Синтаксические свойства инфинитива
Синтаксические свойства инфинитива Презентация 1
Презентация 1 Die BRD (1949 -1990)
Die BRD (1949 -1990) Родными тропами
Родными тропами SPb_GBOU_SPO_Akusherskiy_kolledzh_Yana_Skolova_402 (1)
SPb_GBOU_SPO_Akusherskiy_kolledzh_Yana_Skolova_402 (1) Реставрация картины Г. Угрюмова Испытание силы Яна Усмаря
Реставрация картины Г. Угрюмова Испытание силы Яна Усмаря «Пётр Великий русской литературы» (В.Г.Белинский)
«Пётр Великий русской литературы» (В.Г.Белинский) История и перспективы производства видеопродукции нового формата в России и за рубежом
История и перспективы производства видеопродукции нового формата в России и за рубежом Создание единого китайского государства
Создание единого китайского государства Экологические проблемы мира
Экологические проблемы мира Национальная посуда народов мира
Национальная посуда народов мира Персидская империя.
Персидская империя. Программное обеспечение для поддержки информационной бизнес-аналитики
Программное обеспечение для поддержки информационной бизнес-аналитики Презентация на тему Классификация профессий Профессия и специальность Способы классификации
Презентация на тему Классификация профессий Профессия и специальность Способы классификации Сжатие информации. Алгоритм Хаффмана
Сжатие информации. Алгоритм Хаффмана LIEBHERR LTM 1160-5.1Самоходный кран большой грузоподъемности (160 тонн)
LIEBHERR LTM 1160-5.1Самоходный кран большой грузоподъемности (160 тонн) Презентация на тему Кайнозойская эра
Презентация на тему Кайнозойская эра Презентация на тему Трудовая дисциплина и ответственность за её нарушение
Презентация на тему Трудовая дисциплина и ответственность за её нарушение  Poker face
Poker face Волейбол – виды подач
Волейбол – виды подач Эволюция интернет-трейдинга
Эволюция интернет-трейдинга ГЕНЕРАТОРЫ ИМПУЛЬСНЫХ НАПРЯЖЕНИЙ СУБНАНОСЕКУНДНОЙ ДЛИТЕЛЬНОСТИразработки ЗАО «НПАО ФИД-технология»
ГЕНЕРАТОРЫ ИМПУЛЬСНЫХ НАПРЯЖЕНИЙ СУБНАНОСЕКУНДНОЙ ДЛИТЕЛЬНОСТИразработки ЗАО «НПАО ФИД-технология» Название проекта
Название проекта Новый Год
Новый Год Немеркнущая красота России или Сквозь эпохи и поколения
Немеркнущая красота России или Сквозь эпохи и поколения Основные понятия «Теории вероятностей»
Основные понятия «Теории вероятностей» Овощи и их вредители
Овощи и их вредители География сельского хозяйства мира
География сельского хозяйства мира