Содержание
- 2. Загадка Очень древний я металл, Счёт столетьям потерял. Был нескромным я не в меру, Тысячи лет
- 3. «Третий лишний». Задание: Решите анаграммы и исключите лишнее. леруогд иксолодр ддрооов золеже углерод кислород водород железо
- 4. Охарактеризуйте Fe как химический элемент, составив предложения со словами и словосочетаниями: Порядковый номер, номер периода ,
- 5. Задание Закончите электронно - буквенную формулу и нарисуйте графическую формулу строения атома железа: Железо(№ 131835)
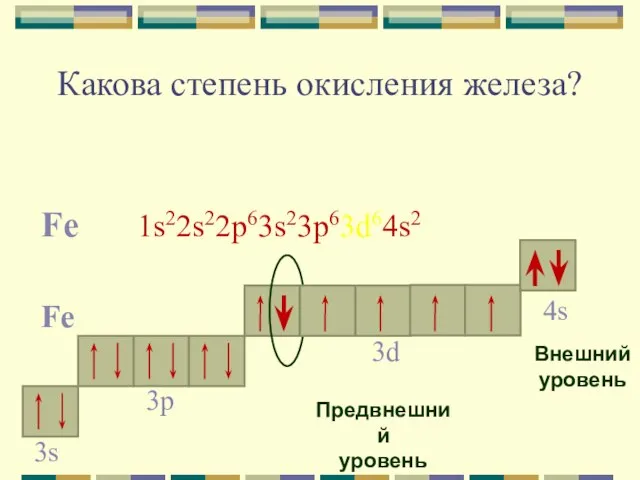
- 6. Какова степень окисления железа? Fe 1s22s22p63s23p63d64s2 Fe 4s Внешний уровень 3d Предвнешний уровень 3p 3s
- 7. Для железа характерны две основные степени окисления: +2, +3. Fe0 - 2e- = Fe+2 Fe0 -
- 8. Задание: Рассмотрите образец металла (№ 131836). Опишите физические свойства металла (№ 131797).. Используя текст учебник, заполните
- 9. Выберите и запишите цифры только тех свойств, которые не относятся к физическим свойствам железа: Серебристо-белый металл
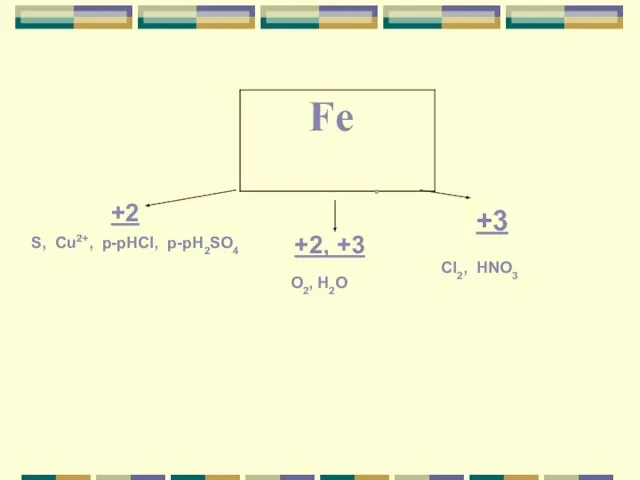
- 10. +2 +2, +3 +3 S, Cu2+, p-рHCI, p-рH2SO4 O2, H2O CI2, HNO3
- 11. Химические свойства железа Взаимодействие железа с хлором Видеофрагмент (№ 54490): 2Fe + 3Cl2 = 2FeCl3
- 12. Химические свойства железа Взаимодействие железа сВзаимодействие железа с Взаимодействие железа с кислородом: Видеофрагмент (№ 131824) Fe
- 13. : Какие из реакций соответствуют схеме Fe+2 → Fe+3 FeCI2 + CI2 = FeCI3 FeCI3 +
- 14. Задание: Расставить коэффициенты в уравнениях 1 и 3 методом электронного баланса, определить окислитель и восстановитель в
- 15. Нахождение в природе В земной коре 5,1% железа, 4 место после кислорода, кремния и алюминия. По
- 16. Нахождение в природе Метеоритное железо(№ 131727) Запишите не менее 4 -х формул соединений железа, встречающихся в
- 17. Природные соединения железа Fe FeS Пирит (железный или серный колчедан) FeCO3 Сидерит Fe2O3*3H2O Лимонит (бурый железняк)
- 18. Генетические связи Fe - ОТ ЖЕЛЕЗА ДО ОКСИДА ЖЕЛЕЗА (- ОТ ЖЕЛЕЗА ДО ОКСИДА ЖЕЛЕЗА (II-
- 19. ПРИМЕНЕНИЕ(№ 207382) Чистое железо способно быстро намагничиваться и размагничиваться, поэтому его применяют для изготовления трансформаторов, электромоторов
- 20. Домашнее задание § 14, с. 76 -78 № 5 с. 82 - всем № 6 с.
- 21. Используемая литература: 1. Горковенко М. Ю. Химия. 9 класс. Поурочные разработки к учебнику О. С. Габриеляна
- 23. Скачать презентацию

















 Презентация на тему Эдуард Мане
Презентация на тему Эдуард Мане 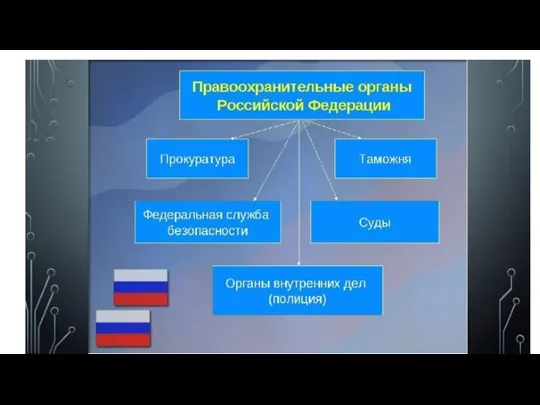 Правоохранительные органы Российской Федерации
Правоохранительные органы Российской Федерации Организация сопровождаемого проживания граждан с нарушениями
Организация сопровождаемого проживания граждан с нарушениями 学校
学校 Типы сварных швов
Типы сварных швов Отчет о размещении вакансий
Отчет о размещении вакансий СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ
СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ Сравнительный анализ развития лыжероллеров
Сравнительный анализ развития лыжероллеров Прыжки в длину
Прыжки в длину Презентация на тему Механические колебания 11 класс
Презентация на тему Механические колебания 11 класс  Понятия частей речи
Понятия частей речи Презентация Нагрузки и воздействия
Презентация Нагрузки и воздействия Презентация на тему Разнообразие животных
Презентация на тему Разнообразие животных  English theater
English theater  Класс Однодольные, характерные признаки растений семейства злаковых
Класс Однодольные, характерные признаки растений семейства злаковых Еңбек нормасы. Өнім нормасы
Еңбек нормасы. Өнім нормасы Формы и методы профессиональной ориентации
Формы и методы профессиональной ориентации e70f443261a743aba5fb4ba5defd798a
e70f443261a743aba5fb4ba5defd798a Функциональные стили речи
Функциональные стили речи Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100"
Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100" Презентация на тему Вельможи Древнего ЕГИПТА
Презентация на тему Вельможи Древнего ЕГИПТА  Маршалы Великой Отечественной войны
Маршалы Великой Отечественной войны Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона
Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона Природный газ
Природный газ Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы
Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы Оркестр. Инструменты симфонического оркестра
Оркестр. Инструменты симфонического оркестра МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА
МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА  Богиня Молва (Фама, Осса)
Богиня Молва (Фама, Осса)