Содержание
- 2. Классификация минеральных удобрений - по агрохимическому назначению: прямые – содержат питательные элементы; косвенные – для улучшения
- 3. – по агрегатному состоянию: 1. твердые; 2. жидкие (NH3 · H2O, суспензии, водные растворы). – по
- 4. Азотные удобрения нитратные – KNO3; амидные – СО(NH2)2; аммонийные – (NH4)2SO4, NH3·H2O, NH4NO3 – 35% N.
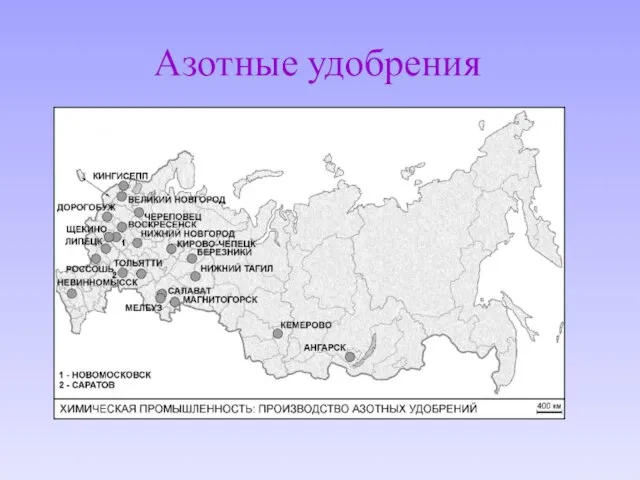
- 5. Азотные удобрения
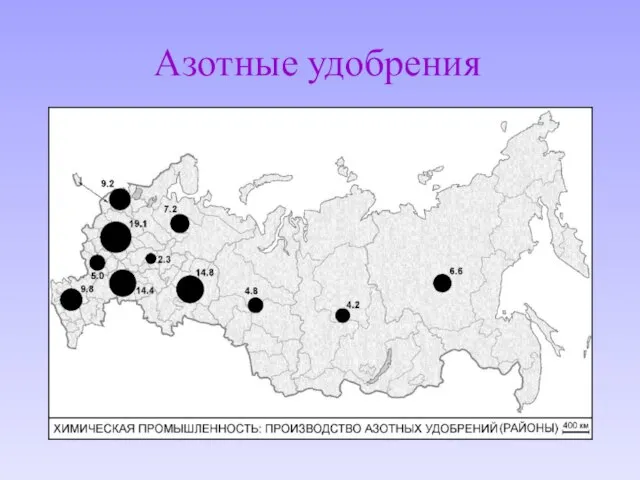
- 6. Азотные удобрения
- 7. Производство NH4NO3 Достоинства: высокое содержание азота – 35%; растворимость в воде Недостаток: гигроскопичность, слёживаемость, поэтому –
- 8. Производство NH4NO3 NH3 + HNO3 → NH4NO3 ΔH = -144,9 кДж/моль Лимитирующая стадия – диффузия аммиака
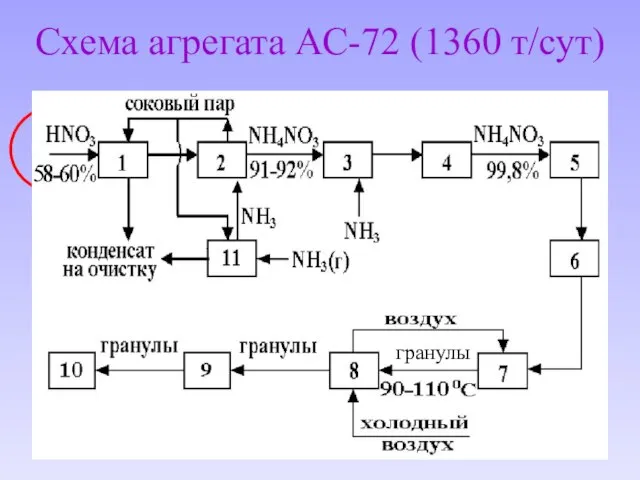
- 9. Схема агрегата АС-72 (1360 т/сут) 5 гранулы
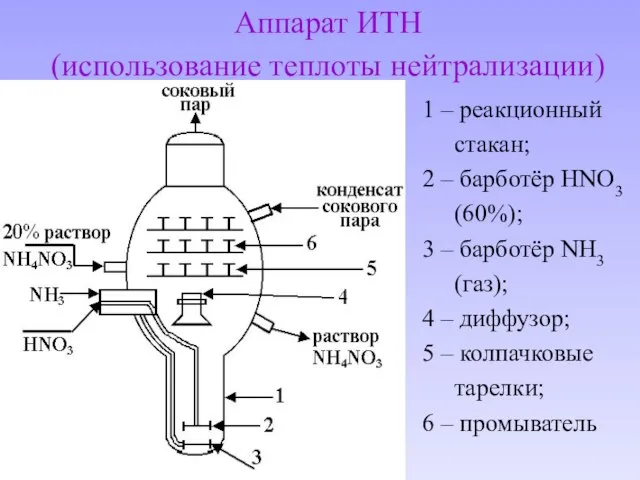
- 10. Аппарат ИТН (использование теплоты нейтрализации) 1 – реакционный стакан; 2 – барботёр HNO3 (60%); 3 –
- 11. 1 – подогреватель HNO3 до 70 – 800 С соковым паром из 2; 2 – два
- 12. Производство карбамида (мочевины) - CO(NH2)2
- 13. Мочевина открыта в 1773 г в моче И.Руэлем, идентифицирована У.Праутом в 1818 г, синтезирована Ф.Вёлером (1828)
- 14. Использование мочевины (106 млн.т/год – 1984; 15,9 - 1995 г. все азотные) удобрение; кормовые добавки; синтез
- 15. Достоинства карбамида: высокое содержание азота - 46,6%, негигроскопичность, небольшие потери за счёт вымывания из почвы Получение
- 16. Условия : 1 стадия: Р>15-20 МПа (реакция идёт с уменьшением объёма), t = 150-190о С (для
- 17. Условия : Итак: t = 180-230oC, P = 12-25 МПа, но превращение не полное, смесь содержит
- 18. Открытая схема: отделение карбамида, а не прореагировавшие NH3 и CO2 – на синтез NH4NO3. Для этого
- 19. Рецикл жидкой фазы - стриппинг -процесс (отдувка) - разложение карбамата при высоком давлении вследствие продувки сжатым
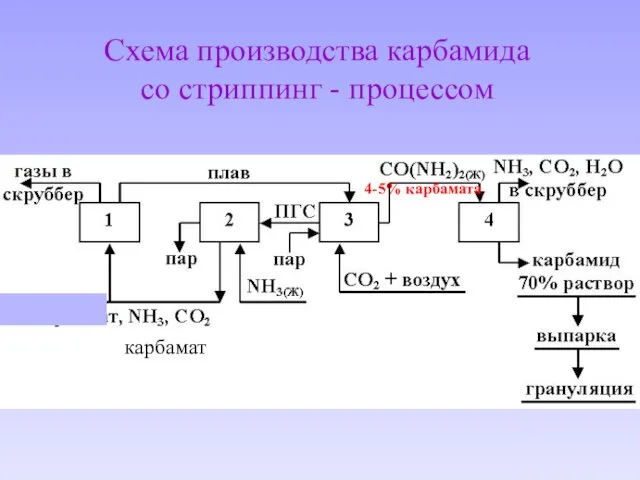
- 20. Схема производства карбамида со стриппинг - процессом
- 21. 1 – колонна синтеза карбамида (2-я стадия), 170 – 190 0С, 13 – 15 МПа, NH3
- 22. Очистка сточных вод Биологическая очистка после разбавления сточных вод до концентрации карбамид аммиак
- 23. ПРОИЗВОДСТВО ФОСФОРНЫХ УДОБРЕНИЙ
- 24. Сырьё для производства – природные фосфаты () Название апатиты происходит от греч. «апатао» – обманываю, поскольку
- 25. Цвет апатитов: бледно–зелёный, голубой, желто–зелёный, розовый
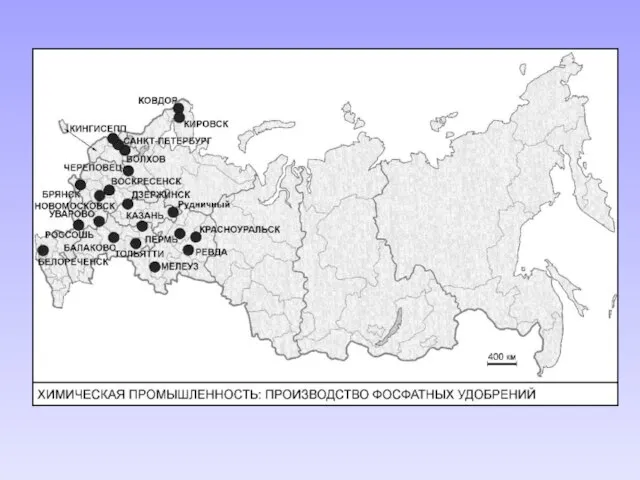
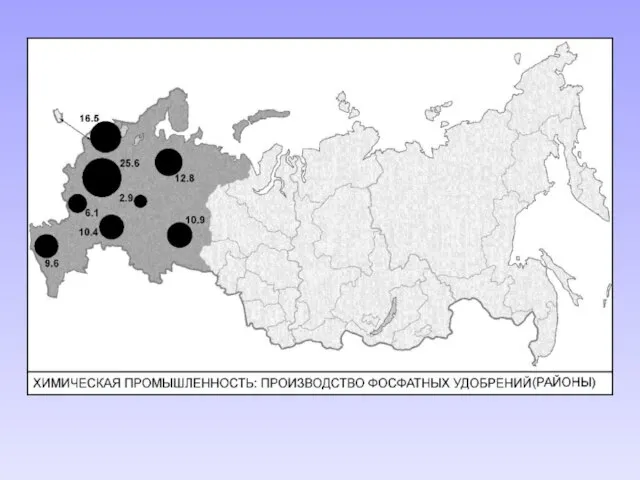
- 26. Месторождения: Хибинское (1925 г.) на Кольском полуострове – крупнейшее в мире (несколько километров, глубина 100–200 метров):
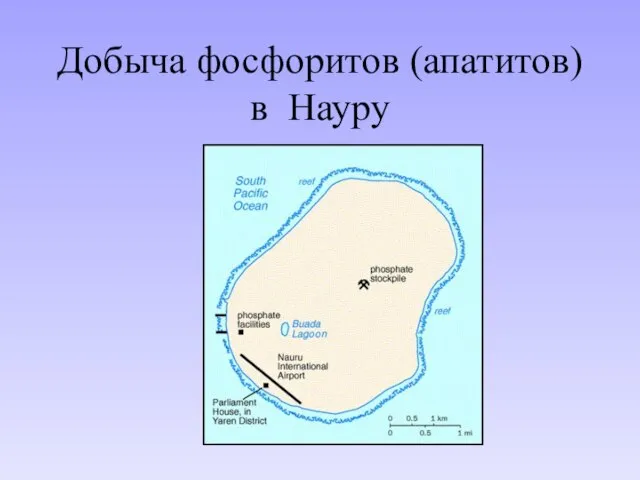
- 27. Науру – территория 21 кв. км, население - 10,7 тыс. чел. (1998 г.)
- 28. Добыча фосфоритов (апатитов) в Науру
- 31. Методы переработки апатитов (1990 г. – 3,85 млн.т; 1995 г.– 2,17 млн.т) механические (фосфоритная мука); термические;
- 32. Методы переработки апатитов Химические: при обработке минеральными кислотами получают простой суперфосфат и ортофосфорную кислоту, из которых
- 33. Производство простого суперфосфата Суммарная реакция: 2Ca5F(PO4)3 + 7H2SO4 + 6,5H2O → → 3[Ca(H2PO4)2 · H2O] +
- 34. Производство простого суперфосфата II стадия (медленно, 5 – 20 суток на складе): после расходования H2SO4 апатит
- 35. Условия: избыток H2SO4 (1,07 ÷ 1,14), концентрация H2SO4 68,5 – 69,5 % – оптимальная для кристаллизации
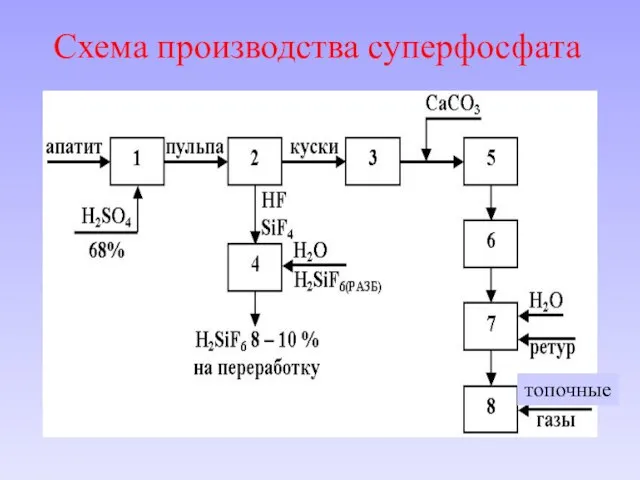
- 36. Схема производства суперфосфата
- 37. 1 – смеситель (t =110 – 115 0C); 2 – суперфосфатная камера; 3 – склад (дозревание)
- 38. Простой суперфосфат Недостатки: низкое содержание фосфора - 19 – 21% P2O5; высокая доля балласта - CaSO4
- 39. Двойной суперфосфат Достоинства: высокое содержание фосфора - 42 – 50 % P2O5; высокая доля водорастворимого фосфора
- 40. Методы получения H3PO4
- 41. термический – получение белого фосфора и его дальнейшее окисление: электротермическое восстановление апатитов Ca5F(PO4)3 + 6SiO2 +
- 42. конденсация паров фосфора – (t≥500 C), под водой окисление фосфора P4 + 5О2 → 2Р2О5 Р2О5
- 43. гидролиз фосфора – перспективный метод P4 + 10Н2О → 2Р2О5 + 10Н2 t = 600 -
- 44. Применение H3PO4 производство удобрений; неорганических солей (фосфаты); органический синтез; получение активированного угля; антикоррозийные покрытия; в производстве
- 45. Методы получения двойного суперфосфата камерный (малоэффективный); поточный (непрерывный). Ca5F(PO4)3 + 7H3РO4 + 5H2O → 5[Ca(H2PO4)2 ·
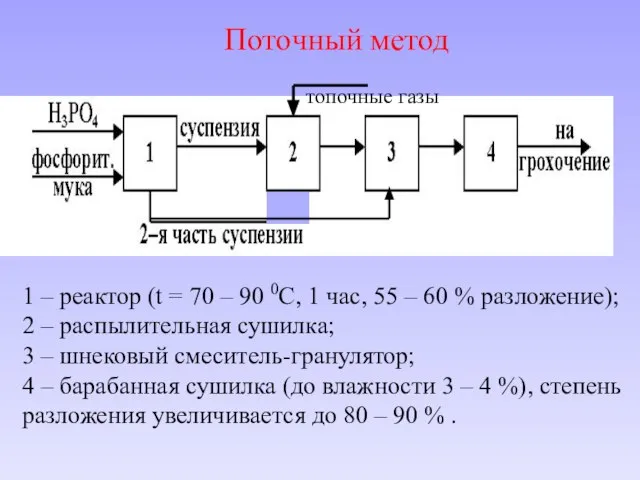
- 46. Поточный метод 1 – реактор (t = 70 – 90 0C, 1 час, 55 – 60
- 48. Скачать презентацию



































 О распределении и реализации дотации на поддержку мер по обеспечению сбалансированности местных бюджетов в 2011-2012 годах в Киров
О распределении и реализации дотации на поддержку мер по обеспечению сбалансированности местных бюджетов в 2011-2012 годах в Киров Деньги. Откуда они берутся и кто их контролирует
Деньги. Откуда они берутся и кто их контролирует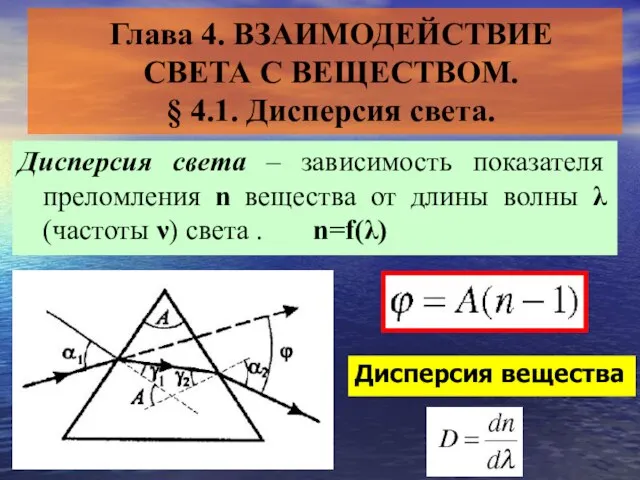 Презентация на тему Взаимодействие света с веществом Дисперсия света
Презентация на тему Взаимодействие света с веществом Дисперсия света
 МЕЖДУНАРОДНАЯ ПЕРЕДАЧА ТЕХНОЛОГИЙ
МЕЖДУНАРОДНАЯ ПЕРЕДАЧА ТЕХНОЛОГИЙ Поворот
Поворот Скетчинг
Скетчинг Социальная политика России в контексте сравнительной социальной политики
Социальная политика России в контексте сравнительной социальной политики Построение чертежа основы плечевого изделия с цельнокроеным рукавом
Построение чертежа основы плечевого изделия с цельнокроеным рукавом Гипертоническая болезнь
Гипертоническая болезнь  Презентация на тему Александр Николаевич Островский
Презентация на тему Александр Николаевич Островский  Суша
Суша Управление документацией. Управление записями. Ведение рабочих журналов. Управление целостностью данных
Управление документацией. Управление записями. Ведение рабочих журналов. Управление целостностью данных Презентация на тему Гумилев
Презентация на тему Гумилев THE KAZAKHSTAN’S ARCHITECTURE of the Nineteenth century (THE FORMS SUMMATION) / «STYLES OF THE KAZAKHSTAN’S ARCHITECTURE» the Series of thematic lectures by Dr. K.I.Samoilov, 2016. – ppt-Presentation. – 38 p.
THE KAZAKHSTAN’S ARCHITECTURE of the Nineteenth century (THE FORMS SUMMATION) / «STYLES OF THE KAZAKHSTAN’S ARCHITECTURE» the Series of thematic lectures by Dr. K.I.Samoilov, 2016. – ppt-Presentation. – 38 p. Презентация на тему Интернет в жизни человека
Презентация на тему Интернет в жизни человека Электроника и информационно-измерительная техника. Допуск к экзамену
Электроника и информационно-измерительная техника. Допуск к экзамену Альтернативный взгляд на лидерствоШубенкова Татьянаконсалтинговая компания «Шубенкова и Партнёры»
Альтернативный взгляд на лидерствоШубенкова Татьянаконсалтинговая компания «Шубенкова и Партнёры» Шÿвыр ( волынка) - один из древнейших музыкальных инструментов мари
Шÿвыр ( волынка) - один из древнейших музыкальных инструментов мари Олимпийские игры. История, девиз, символика и ритуал
Олимпийские игры. История, девиз, символика и ритуал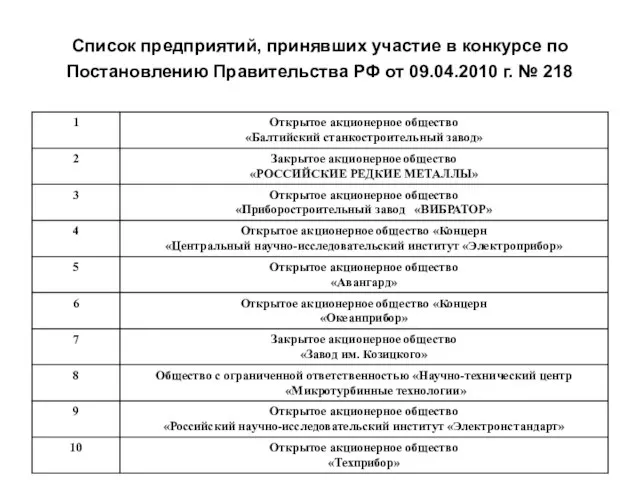 Список предприятий, принявших участие в конкурсе по Постановлению Правительства РФ от 09.04.2010 г. № 218
Список предприятий, принявших участие в конкурсе по Постановлению Правительства РФ от 09.04.2010 г. № 218 Невербальные средства общения. Ольфакторные
Невербальные средства общения. Ольфакторные Социальная структура группы
Социальная структура группы Маг. маг. д-р Йоханн М. ЗАКС Генеральный директор по внешнеэкономическим связям
Маг. маг. д-р Йоханн М. ЗАКС Генеральный директор по внешнеэкономическим связям Якутские национальные спортивные игры
Якутские национальные спортивные игры Применение компьютерных технологий при выполнении творческого проекта
Применение компьютерных технологий при выполнении творческого проекта praktika_po_zhkkh
praktika_po_zhkkh М.В.Ломоносов- человек энциклопедических знаний
М.В.Ломоносов- человек энциклопедических знаний Авторская школа ученого -исследователя
Авторская школа ученого -исследователя