Содержание
- 2. 5 г хлорида магния получено при обработке 6,5 г смеси оксида и бромида магния соляной кислотой.
- 3. Составим уравнения реакций: M(MgO)= 40 г/моль M(MgBr2)= 184 г/моль M(MgCl2)= 95 г/моль
- 4. Составим систему уравнений: х г – А г 40 г/моль – 95 г/моль (2) у г
- 5. Методы решения систем уравнений: Метод подстановки Метод сложения Графический метод
- 6. Способ сложения:
- 7. Способ подстановки:
- 9. Имеется раствор, содержащий одновременно соляную и азотную кислоты. Определить массу каждой из кислот, если при нейтрализации
- 10. Составим уравнения реакций: M(KOH)= 56 г/моль M(HNO3)= 63 г/моль M(HCl)= 36,5 г/моль
- 11. Составим систему уравнений: х г – А г 36,5 г/моль – 56 г/моль (2) у г
- 12. Систему уравнений решить самостоятельно. I вариант – методом подстановки; II вариант – графическим методом.
- 13. Метод подстановки:
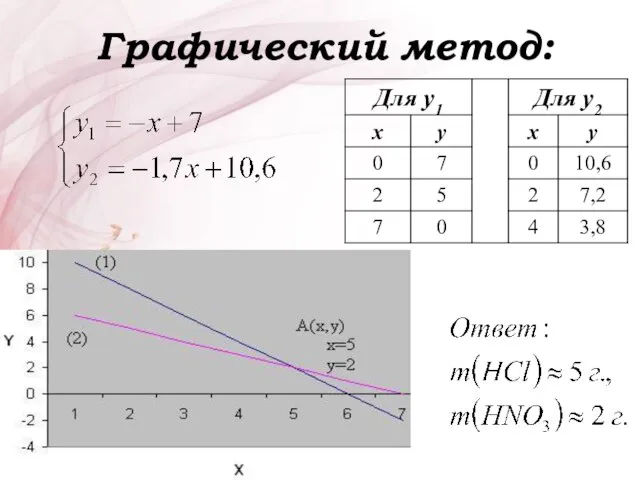
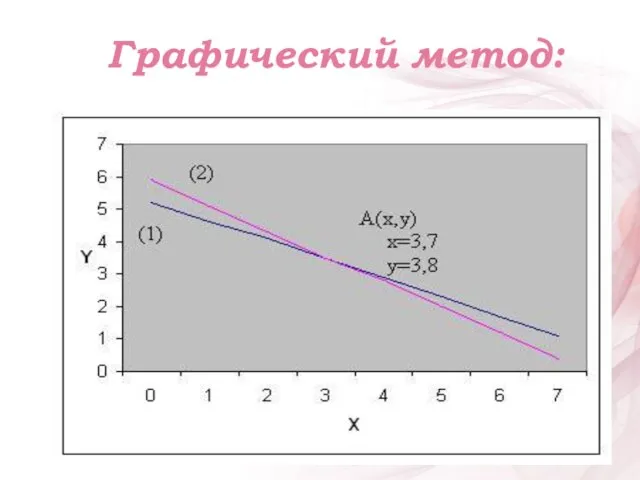
- 14. Графический метод:
- 15. 7,5 грамма смеси цинка и железа обработали соляной кислотой, при этом выделилось 2,78 л водорода. Определите
- 16. Уравнения реакций M(Zn)= 65 г/моль M(Fe)= 56 г/моль
- 17. Составим систему уравнений: х г/моль – А л 65 г/моль – 22,4 л (2) у г/моль
- 18. Метод подстановки Метод сложения
- 19. Графический метод:
- 23. Домашнее задание При взаимодействии нитрата серебра и 2,66 г смеси хлорида натрия и хлорида калия получено
- 24. Математические методы исполь-зуются при решении задач с практическим содержанием. Это могут быть задачи по физике, химии,
- 26. Скачать презентацию





















 Презентация на тему Семейство Зонтичные
Презентация на тему Семейство Зонтичные  Типология и характеристика недвижимого имущества как объектов оценки. Коммерческая недвижимость(склады)
Типология и характеристика недвижимого имущества как объектов оценки. Коммерческая недвижимость(склады) Презентация на тему Отряд хищные
Презентация на тему Отряд хищные  Источники права в Турции
Источники права в Турции Бритвы Braun Учебное пособие
Бритвы Braun Учебное пособие Основные положения конструирования элементов железобетонных конструкций
Основные положения конструирования элементов железобетонных конструкций Презентация на тему Свойства функции (9 класс)
Презентация на тему Свойства функции (9 класс) Основные свойства простейших геометрических фигур
Основные свойства простейших геометрических фигур Игрушки древних славян. Погремушки
Игрушки древних славян. Погремушки Эволюция человека. Первые современные люди - неоантропы
Эволюция человека. Первые современные люди - неоантропы Политические режимы
Политические режимы Игра Для детей 4-5 лет
Игра Для детей 4-5 лет Шындыққа келмейтіндерді жариялаудың проблемалары
Шындыққа келмейтіндерді жариялаудың проблемалары Презентация на тему История Древнего мира 5 класс
Презентация на тему История Древнего мира 5 класс  Царство Божье… и ты
Царство Божье… и ты Тема: как компьютер влияет на наше зрение?
Тема: как компьютер влияет на наше зрение? Принципы административной ответственности
Принципы административной ответственности Что означают наши имена
Что означают наши имена Некоторые подходы к построению автоматизированной системы проведения комплексного анализа результатов обучающихся
Некоторые подходы к построению автоматизированной системы проведения комплексного анализа результатов обучающихся Хрящевые и костные рыбы
Хрящевые и костные рыбы Financial Markets
Financial Markets Круговорот воды в природе (3 класс)
Круговорот воды в природе (3 класс) Классный час «Дороги, которые мы выбираем»
Классный час «Дороги, которые мы выбираем» Реализация государственной научно-технической и инновационной политики
Реализация государственной научно-технической и инновационной политики Гипертоническая болезнь Артериальные гипертензии
Гипертоническая болезнь Артериальные гипертензии Мастер-класс Точка роста
Мастер-класс Точка роста Обучение грамоте (письмо) 1 класс Тема «Прописная буква Ф.» Пропись 4 к «Русской азбуке» В.В. Горецкого Москва «Просвещение» 20
Обучение грамоте (письмо) 1 класс Тема «Прописная буква Ф.» Пропись 4 к «Русской азбуке» В.В. Горецкого Москва «Просвещение» 20 «Лен. Льняное волокно. Сравнительная характеристика растительных волокон и тканей из них»
«Лен. Льняное волокно. Сравнительная характеристика растительных волокон и тканей из них»