Содержание
- 2. Сера Сера – халькоген, довольно активный неметалл. Сущетсвует три аллотропных модификации серы: ромбическая S8 пластическая моноклинная
- 3. Характеристика серы Сера в ПСХЭ: положение (период, группа) строение атома свойства элемента по периоду / в
- 4. Получение При сливании растворов сероводородной и сернистой кислот: H2SO3 + 2H2S = 3S + 3H2O При
- 5. Химические свойства Не смачивается и не реагирует с водой. Как окислитель реагирует с: металлами (кроме золота)
- 6. Химические свойства Как восстановитель реагирует с: кислородом хлором фтором
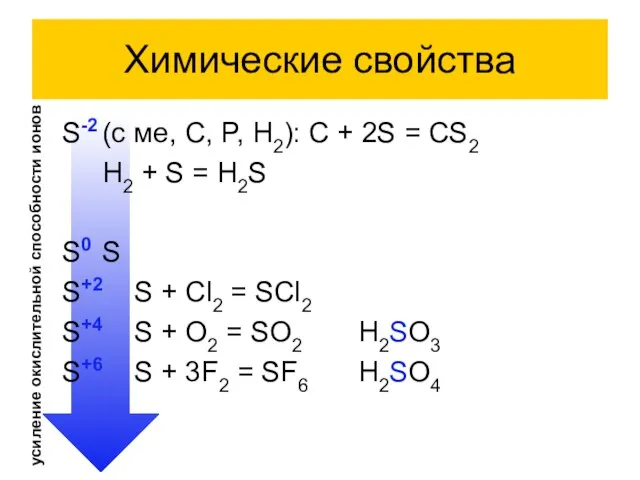
- 7. Химические свойства S-2 (с ме, C, P, H2): C + 2S = CS2 H2 + S
- 8. Сероводород H2S – сероводород. Его раствор в воде называется сероводородной кислотой. Кислота слабая двухосновная, поэтому диссоциирует
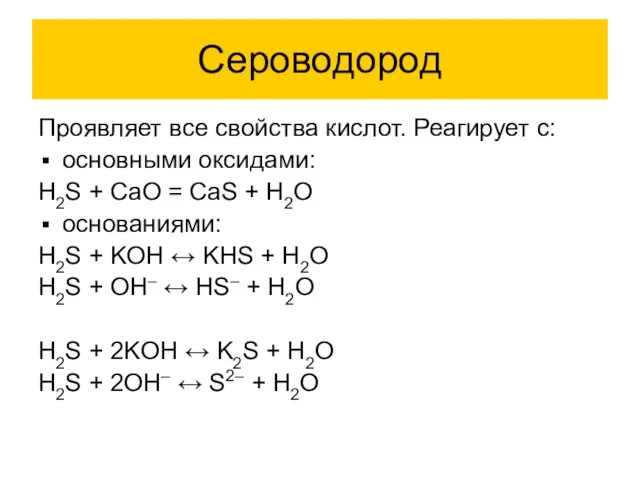
- 9. Сероводород Проявляет все свойства кислот. Реагирует с: основными оксидами: H2S + CaO = CaS + H2O
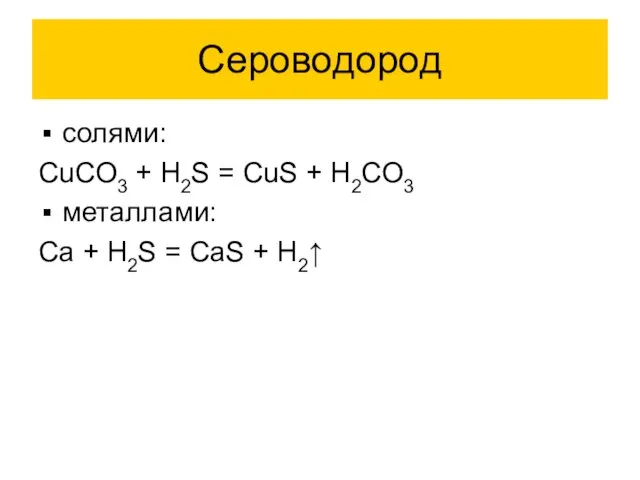
- 10. Сероводород солями: CuCO3 + H2S = CuS + H2CO3 металлами: Ca + H2S = CaS +
- 11. Свойства солей Кислые соли сероводородной кислоты – гидросульфиды (KHS, NaHS) хорошо растворимы в воде. Растворимыми также
- 12. Окисление сероводорода Сероводород легко окисляется кислородом (как при избытке O2 и недостатке?). Бромной водой Br2: H2S
- 13. Оксид серы (IV) SO2 – сернситый газ. Реагирует с водой с образование H2SO3. Типичный кислотный оксид.
- 14. Оксид серы (IV) Получают: горением серы обжигом пирита действием кислот на сульфиты взаимодействием конц. серной кислоты
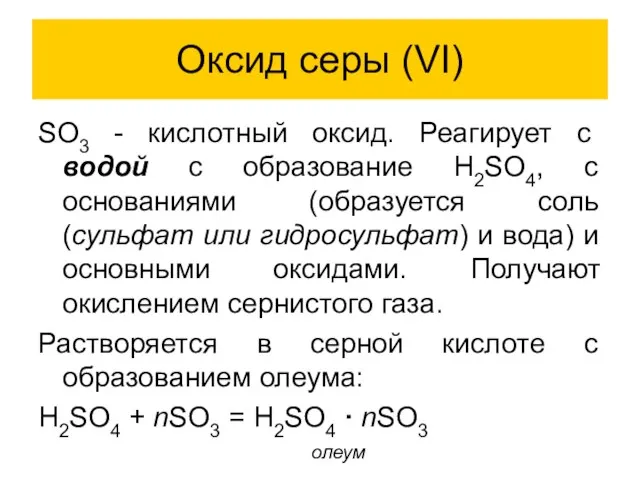
- 15. Оксид серы (VI) SO3 - кислотный оксид. Реагирует с водой с образование H2SO4, с основаниями (образуется
- 16. Серная кислота Серная кислота H2SO4 – тяжёлая маслянистая жидкость без запаха и цвета. При концентрации >
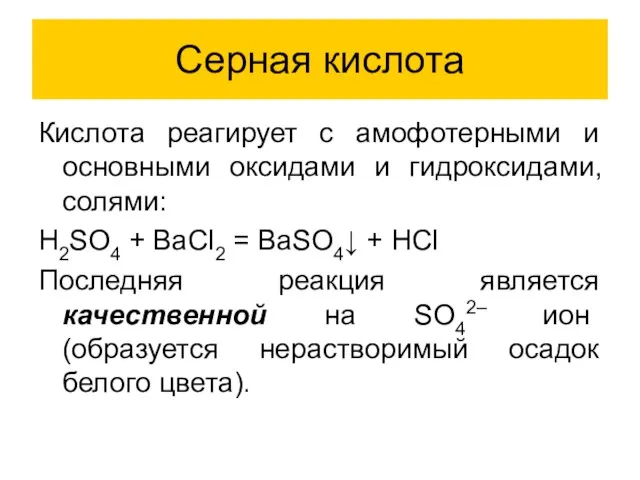
- 17. Серная кислота Кислота реагирует с амофотерными и основными оксидами и гидроксидами, солями: H2SO4 + BaCl2 =
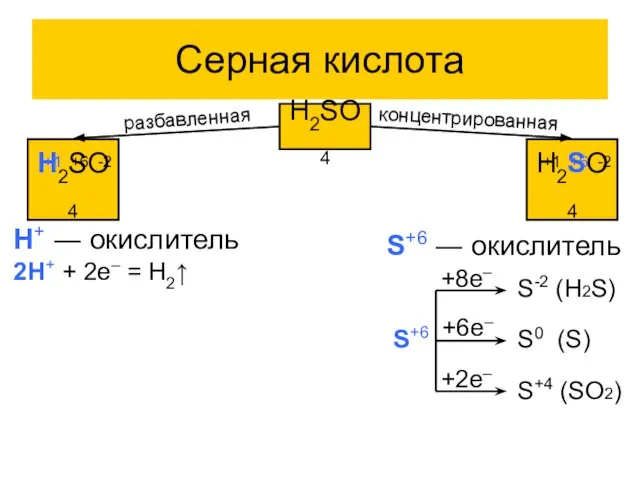
- 18. Серная кислота H2SO4 H2SO4 +1 +6 -2 H2SO4 +1 +6 -2 разбавленная концентрированная H+ ― окислитель
- 19. Серная кислота C разбавленной серной кислотой реагируют все металлы, стоящие в ряду активности до водорода. При
- 20. Концентрированная серная кислота Металлы, стоящие в ряду активности после водорода, взаимодействуют с концентрированной серной кислотой по
- 21. Концентрированная серная кислота Более активными ме серная кислота при определённых условиях может восстанавливаться до серы в
- 22. Получение серной кислоты получение SO2 (обычно обжигом пирита) окисление SO2 в SO3 в присутсвии катализатора –
- 23. Сульфаты Соли серной кислоты имеют все свойства солей. Особенным является их отношение к нагреванию: сульфаты активных
- 24. Вопросы в каких реакциях сера играет роль окислителя? восстановителя? какие степени она при этом проявляет? чем
- 26. Скачать презентацию

















 Импортозамещающая политика: основные понятия и Российская практика
Импортозамещающая политика: основные понятия и Российская практика  Презентация на тему Добровольная подготовка граждан к военной службе
Презентация на тему Добровольная подготовка граждан к военной службе  Фотографии людей
Фотографии людей Аудит компании USA Healthbeauty
Аудит компании USA Healthbeauty Презентация на тему Что такое эмоции и зачем они нужны
Презентация на тему Что такое эмоции и зачем они нужны Повышение эффективности деятельности Дистанции погрузочно-разгрузочных работ и коммерческих операций
Повышение эффективности деятельности Дистанции погрузочно-разгрузочных работ и коммерческих операций Природные и рукотворные формы в натюрморте
Природные и рукотворные формы в натюрморте Сладкое
Сладкое Представительство земли Бавария в Российской Федерации – с 1995 г. на службе баварской экономике
Представительство земли Бавария в Российской Федерации – с 1995 г. на службе баварской экономике Магистерская диссертация. Двухсекторная модель экономики с неоднородным трудом.
Магистерская диссертация. Двухсекторная модель экономики с неоднородным трудом. ЧЕТЫРЕ СВЕЧИ
ЧЕТЫРЕ СВЕЧИ Таможенные органы Челябинской области: Уровень эффективности работы и перспективные задачи
Таможенные органы Челябинской области: Уровень эффективности работы и перспективные задачи Елизаветинское барокко. Тест
Елизаветинское барокко. Тест Комплексные работы в начальной школе
Комплексные работы в начальной школе ИНТЕРНЕТ-ТЕХНОЛОГИИдля международного сотрудничества малых предприятий
ИНТЕРНЕТ-ТЕХНОЛОГИИдля международного сотрудничества малых предприятий Юридический институт
Юридический институт Площадки под мероприятия
Площадки под мероприятия Русь и Литва в XIII-XIV вв
Русь и Литва в XIII-XIV вв Финансовый контроль и его принципы. (Тема 21)
Финансовый контроль и его принципы. (Тема 21) Организация научных исследований в области дошкольного образования на уровне магистерской диссертации
Организация научных исследований в области дошкольного образования на уровне магистерской диссертации 1_WORD_ORDER_part_II
1_WORD_ORDER_part_II Психологическая уравновешенность в конфликтных ситуациях
Психологическая уравновешенность в конфликтных ситуациях Роль профессиональной компетентности учителя в формировании качества знаний учащихся классов специального образования (7 вида)
Роль профессиональной компетентности учителя в формировании качества знаний учащихся классов специального образования (7 вида) Дезинфицирующее средство СаБиДез - щит от вирусов, бактерий и микробов
Дезинфицирующее средство СаБиДез - щит от вирусов, бактерий и микробов Презентация на тему Красная книга «Окружающий мир» 2 класс
Презентация на тему Красная книга «Окружающий мир» 2 класс Одноклассники, сверстники, друзья (6 класс)
Одноклассники, сверстники, друзья (6 класс) Система работы ШМО по формированию у педагогов оценочных умений в свете ФГОС
Система работы ШМО по формированию у педагогов оценочных умений в свете ФГОС Подготовка к переговорам
Подготовка к переговорам