Слайд 2Цель урока
Изучить химические свойства и стадии получения серной кислоты

Слайд 3Химические свойства
С основаниями (реакция нейтрализации)
H2SO4 + NaOH -> NaHSO4 +
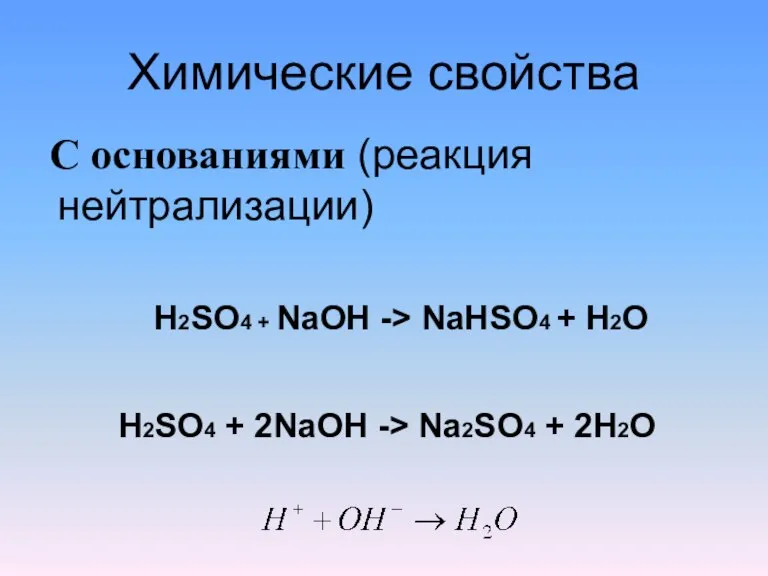
H2O
H2SO4 + 2NaOH -> Na2SO4 + 2H2O
Слайд 4Химические свойства
С металлами (стоящие в ряду напряжения до водорода)
Zn +

H2SO4 -> ZnSO4 + H2
Слайд 5Химические свойства
С солями
BaCl2 + H2SO4 -> BaSO4 + 2HCl
Хлорид бария

является качественным реактивом на H2SO4
Слайд 6Концентрированная серная кислота
Cu + 2H2SO4 -> CuSO4 + SO2 + 2H2O

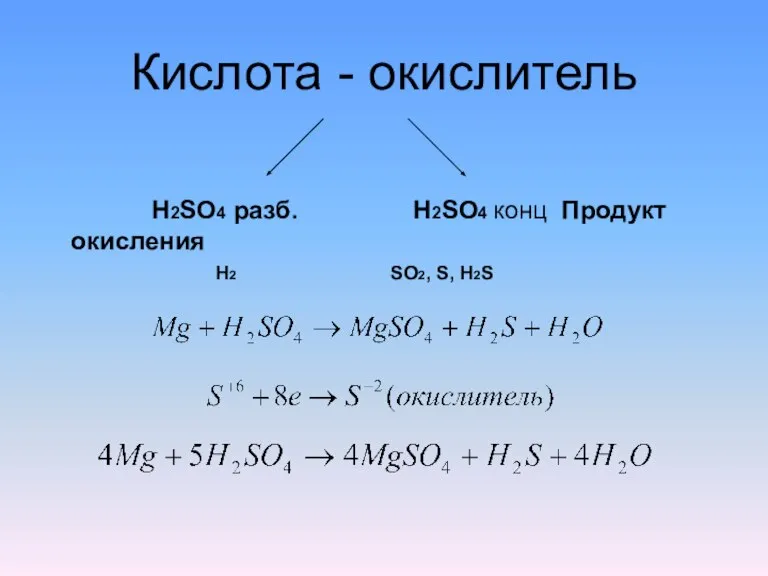
Слайд 7Кислота - окислитель
H2SO4 разб. H2SO4 конц Продукт окисления
H2 SO2, S, H2S
Слайд 8Производство серной кислоты
I стадия – получение сернистого газа SO2
Получение из пирита

Слайд 9Производство серной кислоты
II стадия – получение SO3
2-я стадия

Слайд 10Производство серной кислоты
III стадия – получение H2SO4
3-я стадия

Слайд 11Выводы
Серная кислота может являться реагентом для получения водорода
Серная кислота является сильным

окислителем
Серная кислота взаимодействует не только с металлами стоящие в ряду напряжений до водорода, но и со стоящими после него.
Хлорид бария может являться качественным реагентом на сульфат-анион
Производство серной кислоты является сложным многостадийным химическим процессом
Слайд 12Проверь себя
Вариант I Вариант II
В 1. А
Б 2. Г
А 3. А
А

4. В
В 5. Б











 Обеспечение двигательной активности учащихся средствами физической культуры
Обеспечение двигательной активности учащихся средствами физической культуры Деньги и финансовые институты
Деньги и финансовые институты 20140511_urok_evraziya
20140511_urok_evraziya Презентация на тему Умножение многозначного числа на двузначное число
Презентация на тему Умножение многозначного числа на двузначное число  Окно Овертона, как технология социального изменения
Окно Овертона, как технология социального изменения Боровичский край
Боровичский край Тема урока «АЛГОРИТМЫ»
Тема урока «АЛГОРИТМЫ» Эмоциональное состояние личности
Эмоциональное состояние личности Дегтебетон. Классификация дегтебетона
Дегтебетон. Классификация дегтебетона Культурные традиции народов Европы. 11 класс
Культурные традиции народов Европы. 11 класс 1 сентября - День знаний
1 сентября - День знаний Древняя Русь
Древняя Русь Мексиканский медичи. Евгенио Лопез Алоносо
Мексиканский медичи. Евгенио Лопез Алоносо Способы очистки питьевой воды
Способы очистки питьевой воды Модель
Модель МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕДОШКОЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «ДЕТСКИЙ САД № 47 «ЗЕЛЕНЫЙ ОГОНЕК» КОМПЕНСИРУЮЩЕГО ВИДА» г. Север
МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕДОШКОЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «ДЕТСКИЙ САД № 47 «ЗЕЛЕНЫЙ ОГОНЕК» КОМПЕНСИРУЮЩЕГО ВИДА» г. Север Курсовое проектирование
Курсовое проектирование Основы дизайн-проектирования. Геометрические построения как способ гармонизации. Работы учащихся
Основы дизайн-проектирования. Геометрические построения как способ гармонизации. Работы учащихся Г.Р. Державин
Г.Р. Державин Отдел продаж ОТК
Отдел продаж ОТК Школа Саммерхилл. Великобритания, Лейстон
Школа Саммерхилл. Великобритания, Лейстон Компьютерная графика
Компьютерная графика Великая цель образования – это не знания, а действия. Герберт Спенсер
Великая цель образования – это не знания, а действия. Герберт Спенсер Выбор профессии
Выбор профессии Семья Ермолаевых
Семья Ермолаевых Бизнес-проект на тему: Игровое будущее
Бизнес-проект на тему: Игровое будущее World informational sources. Advertising
World informational sources. Advertising Снег и лёд в поэзии, пословицах, поговорках.Веселая викторина
Снег и лёд в поэзии, пословицах, поговорках.Веселая викторина