электропроводностью и теплопроводностью.
Для металлов характерна металлическая кристаллическая решетка.
У атомов металлов на внешнем уровне 1-3 электрона.
У атомов металлов на внешнем уровне 1-3 электрона.
Металлы являются восстановителями и окислителями.
Для металлов характерна металлическая кристаллическая решетка.
Металлы обладают электропроводностью и теплопроводностью.
При взаимодействии с кислородом металлы принимают электроны.
Все металлы активно взаимодействуют с кислотами.
Металлы Сu, Au, Ag не взаимодействуют с водой даже при нагревании.
Мg, Be относятся к щелочноземельным металлам.
УБЕРИ ЛИШНЕЕ О МЕТАЛЛАХ





 Международное гуманитарное право.
Международное гуманитарное право. «Люблю тебя мой край родной»
«Люблю тебя мой край родной» Авторынок России
Авторынок России Домовые церкви Васильевского острова от 1-й до 6-й линии
Домовые церкви Васильевского острова от 1-й до 6-й линии Создание Почтового Ящика На narod.ru
Создание Почтового Ящика На narod.ru Геннадий Михасенко «Кандаурские мальчишки»
Геннадий Михасенко «Кандаурские мальчишки» Логический тест А ты знаешь
Логический тест А ты знаешь Наука в СССР в 1940-1980-е гг
Наука в СССР в 1940-1980-е гг Instagram-марафоны. Взаимный PR
Instagram-марафоны. Взаимный PR ТЕМА
ТЕМА Социальная активность онлайн и блоггеры Эмин Гусейнзаде
Социальная активность онлайн и блоггеры Эмин Гусейнзаде Уютный домик для скворцов
Уютный домик для скворцов США
США Моделирование вокодера цифровой системы передачи
Моделирование вокодера цифровой системы передачи Алгоритмы в нашей жизни 5 класс
Алгоритмы в нашей жизни 5 класс Статика 10 класс
Статика 10 класс Презентация на тему Длина окружности и площадь круга
Презентация на тему Длина окружности и площадь круга  Школа будущего
Школа будущего П24-Пульс рынка-14.10.22
П24-Пульс рынка-14.10.22 The Empire State Building is one of the American symbols
The Empire State Building is one of the American symbols Формирование мнения в Интернете
Формирование мнения в Интернете Изучаем себя
Изучаем себя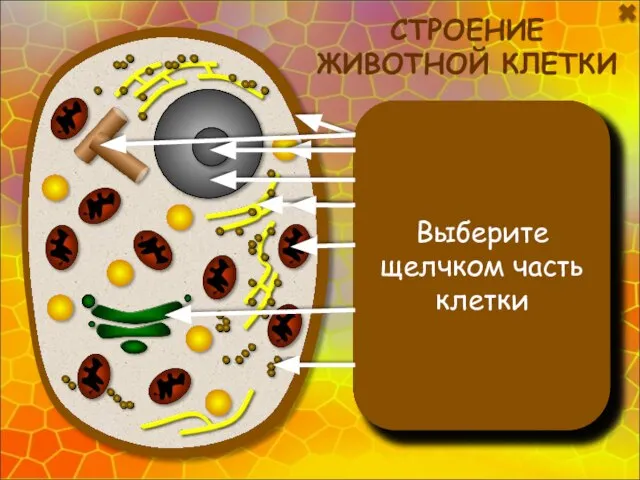 Презентация на тему Строение животной клетки
Презентация на тему Строение животной клетки Презентация на тему Гласные и – ы после Ц в разных частях слова 5 класс
Презентация на тему Гласные и – ы после Ц в разных частях слова 5 класс  Миллионы невинных людей погибло в годы Великой Отечественной Войны. Тысячи детей остались сиротами и пострадали от жестокостей фа
Миллионы невинных людей погибло в годы Великой Отечественной Войны. Тысячи детей остались сиротами и пострадали от жестокостей фа Маркетинг в современном мире
Маркетинг в современном мире Комплексный детокс от Артлайф
Комплексный детокс от Артлайф IT-инфраструктура
IT-инфраструктура