Слайд 2План
Декларирование ЛС.
Регистрация и сертификация ИМН.
Документы, подтверждающие качество ИМН и других товаров

аптечного ассортимента.
Слайд 3Декларирование лекарственных средств

Слайд 4Подтверждение соответствия лекарственных средств требованиям, которые предъявляются к ним действующим законодательством, проводится

в обязательном порядке в форме декларирования лекарственных средств.
Слайд 5Декларирование лекарственных средств введено с 01.01.2007 г.
Приказом Министерства промышленности и энергетики

от 26.12.2006 г. № 425 утверждены «Методические рекомендации по принятию и регистрации декларации о соответствии лекарственных средств».
Слайд 6Подтверждению соответствия в форме декларирования подлежат ЛС,
зарегистрированные в установленном порядке и

состоящие из смешанных или несмешанных продуктов для использования в терапевтических целях,
расфасованные в виде дозированных лекарственных форм или
в упаковке для розничной продажи
(коды 931000-937000 Общероссийского классификатора продукции ОК 005-93).
Слайд 7
Декларированию не подлежат ЛС:
изготовленные в аптеках по рецептам врачей, требованиям

учреждений здравоохранения,
внутриаптечная заготовка,
субстанции,
ЛС, предназначенные для проведения клинических испытаний или для проведения регистрации ЛС.
Слайд 8Декларация о соответствии
это документ, удостоверяющий соответствие выпускаемой в обращение продукции требованиям

технических регламентов. (ФЗ РФ от 27.12.2002г. № 184-ФЗ «О техническом регулировании»).
Слайд 9Процесс декларирования подразумевает
участие в нем:
органа по сертификации,
аккредитованной испытательной

лаборатории,
Декларанта – производителя (поставщика).
На сегодняшний день в РФ аккредитовано в установленном порядке 7 органов по сертификации ЛС (4 в Москве, С-Петербурге, Екатеринбурге, Новосибирске), осуществляющих регистрацию декларации о соответствии и около 70 технически компетентных и независимых испытательных лабораторий, аккредитованных на проведение испытаний ЛС для целей декларирования соответствия.
Слайд 10При подтверждении соответствия в форме декларирования Декларант самостоятельно:
выбирает испытательную лабораторию и

орган по сертификации, который регистрирует декларации о соответствии,
может осуществлять отбор образцов для проведения экспертизы (или может поручить отбор образцов на договорной основе испытательной лаборатории или органу по сертификации).
Слайд 11Декларация о соответствии ЛС принимается самим производителем или продавцом (юридическим или физическим

лицом, зарегистрированным в качестве ИП, либо выполняющим функции иностранного изготовителя на основании договора с ним).
При принятии декларации производитель (поставщик) декларирует, что продукт, который он выпускает в обращение, соответствует стандартам качества, принятым в РФ. При этом он предъявляет необходимые доказательства.
Слайд 12Собственные доказательства
паспорт (протокол анализа) производителя (для отечественных ЛС);
сертификат качества фирмы (для

зарубежных ЛС);
документы, подтверждающие происхождение ЛС;
протоколы входного контроля (испытаний) на сырье, полупродукты, субстанции и материалы, используемые в производстве ЛС;
документы, подтверждающие происхождение сырья, используемого в производстве данного ЛС.
Слайд 13Доказательства с участием третьей стороны
С участием аккредитованного испытательного центра (лаборатории):
протоколы испытаний, проведенных

по показателям качества и безопасности, установленным в нормативной документации на данное ЛС.
С участием органа по сертификации:
сертификаты соответствия, выданные на производство или систему качества (СМК), сертифицированные в Системе сертификации ГОСТ Р.
Слайд 14Принятая изготовителем (продавцом) декларация о соответствии лекарственного средства подлежит регистрации в органе

по сертификации, аккредитованном в установленном порядке.
Регистрация носит заявительный характер.
Реестр зарегистрированных деклараций о соответствии ведется органом по сертификации.
Декларация о соответствии может быть направлена на регистрацию только в один орган по сертификации по выбору изготовителя (продавца).
Слайд 15Декларация о соответствии принимается в отношении каждой серии (партии) ЛС, выпускаемой в

обращение.
Декларация о соответствии принимается на срок, установленный изготовителем (продавцом) ЛС, но не более установленного срока годности ЛС.
Предоставление копий деклараций о соответствии не предусмотрено. Сведения о декларации о соответствии указываются в сопроводительной документации на товар.
Слайд 16В настоящее время провести идентификацию сведений о декларации о соответствии можно по

базе данных зарегистрированных деклараций, размещенной на сайте ФГУ «Центр экспертизы и контроля качества медицинской продукции» Росздравнадзора.
В соответствии со ст. 28 ФЗ № 184-ФЗ «О техническом регулировании» установлена обязанность лиц, являющихся заявителями (продавец продукции) предъявлять заинтересованным лицам документы, свидетельствующие о подтверждении соответствия продукции установленным требованиям (декларации о соответствии или их копии).
При этом, заинтересованными лицами могут являться центры контроля качества в субъектах РФ, оптовые фармацевтические организации, розничные аптечные организации, а также потребители.
Слайд 17Таким образом,
Ответственность за качество ЛС несут производители ЛС или лица, выполняющие функции

иностранного изготовителя (на основании договора с ним в части обеспечения соответствия поставляемой продукции).
У каждого участника фармацевтического рынка должна быть внедрена система обеспечения качества.
Каждый субъект обращения ЛС несет ответственность за качество реализуемых препаратов. Каждый на своем участке – производитель, поставщик, аптека.
Если производитель выпускает качественные ЛС, а при транспортировке и хранении допущены нарушения, в результате которых качество ЛС пострадало, такие препараты выявляются в результате мониторинга качества и подлежат изъятию из обращения.
Слайд 18Регистрация и сертификация изделий медицинского назначения

Слайд 19Регистрация ИМН проводится Росздравнадзором с целью их допуска к
производству,
импорту,
продаже

и
применению на территории РФ.
Слайд 20Регистрация ИМН и мед. техники проводится на основании результатов соответствующих испытаний и

оценок, подтверждающих качество, эффективность и безопасность изделий.
Слайд 21В настоящее время существует несколько типов испытаний, которые необходимо пройти для успешной

регистрации медицинского изделия:
1. Технические испытания;
2. Токсикологические испытания;
3. Медицинские исследования;
4. Экспертиза досье на изделие медицинского назначения (медицинскую технику).
Слайд 22Держателем Регистрационного Удостоверения может быть как юридическое лицо, так и индивидуальный предприниматель.
Срок

действия регистрационного удостоверения не ограничен.
Регистрационные удостоверения заносятся в единый Реестр.
Слайд 23Кроме того на территории РФ для ИМН действует обязательная процедура подтверждения соответствия

продукции стандартам качества. Это документы:
Декларация о соответствии
Сертификат ГОСТ Р
Согласно действующему законодательству, контроль качества и безопасности медицинских изделий осуществляет Минздрав России и Ростехрегулирование (Госстандарт) РФ.
Слайд 24Медицинские изделия классифицируются по уровню потенциального риска их использования, в зависимости от

которого применяются специальные правила и процедуры сертификации.
Всего выделяется четыре класса риска: низкий, средний, повышенный и высокий.
При этом учитывается, как долго изделие контактирует с пациентом, каким образом оно проникает в тело человека, какое воздействие оно оказывает.
Слайд 25Обязательная сертификация – бланк желтого цвета
Добровольная сертификация – бланк синего цвета

Слайд 26Санитарно-эпидемиологическое заключение, оно же «гигиенический сертификат» – документ, подтверждающий, что продукция соответствуют

установленным гигиеническим нормам(ГН) и санитарным правилам (СанПиН).
Санитарно-гигиенический сертификат выдается Роспотребнадзором после проведения экспертизы продукции (условий производства, ТУ) на основании протокола испытаний и предъявленных документов. Срок действия гигиенического сертификата 5 лет.
Слайд 27Товары аптечного ассортимента и документы,
подтверждающие их качество.



























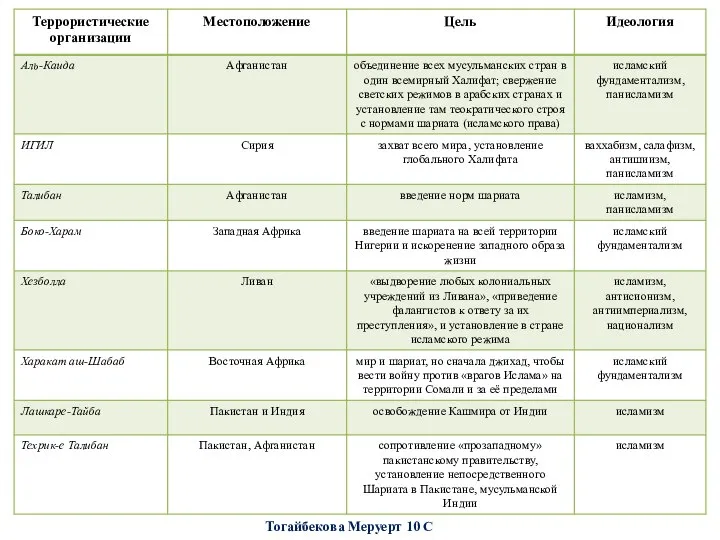 Террористические организации
Террористические организации Викторина по русским народным сказкам и сказкам А.Пушкина
Викторина по русским народным сказкам и сказкам А.Пушкина Какой я
Какой я Развитие психики и сознания
Развитие психики и сознания Рони Ритшель
Рони Ритшель Концептуальное основание современного В2В маркетинга. Концепция маркетинга взаимодействия
Концептуальное основание современного В2В маркетинга. Концепция маркетинга взаимодействия Защита информации от несанкционированного доступа
Защита информации от несанкционированного доступа Стратегический менеджмент в условиях спонтанных изменений
Стратегический менеджмент в условиях спонтанных изменений Я - личный помощник. Измени себя и свою жизнь
Я - личный помощник. Измени себя и свою жизнь Зодчество Древней Греции.
Зодчество Древней Греции. Презентация на тему Сущность и основные понятия этики. Мораль. Типы этики
Презентация на тему Сущность и основные понятия этики. Мораль. Типы этики  Мы познакомимся с чудной страной, Не признающий застой и покой. В этой стране можем деньги вложить И производство свое запустить В
Мы познакомимся с чудной страной, Не признающий застой и покой. В этой стране можем деньги вложить И производство свое запустить В  Карликовая игрунка или пальчиковая обезьяна (Finger Monkey)
Карликовая игрунка или пальчиковая обезьяна (Finger Monkey) ТЕМА 3
ТЕМА 3 МАТЕРИНСТВО И ОТЦОВСТВО
МАТЕРИНСТВО И ОТЦОВСТВО Глагол. Урок-обобщение
Глагол. Урок-обобщение Проект 3: Развитие инновационной деятельности в Технологическом институте, г. Эрдэнэт. - презентация
Проект 3: Развитие инновационной деятельности в Технологическом институте, г. Эрдэнэт. - презентация Люблю берёзку русскую
Люблю берёзку русскую Основные причины психологического бесплодия. Онлайн курс по подготовке к ЭКО
Основные причины психологического бесплодия. Онлайн курс по подготовке к ЭКО Фотоклуб Перспектива
Фотоклуб Перспектива Die Aufgabe “d”
Die Aufgabe “d” Практика в Горьковской дирекции по ремонту пути, подработка в период летних каникул
Практика в Горьковской дирекции по ремонту пути, подработка в период летних каникул Основы грузовой и коммерческой работы
Основы грузовой и коммерческой работы Молодежный инновационный конвент способствует поддержке и повышению престижа молодого ученого в обществе Комитет по молодежной
Молодежный инновационный конвент способствует поддержке и повышению престижа молодого ученого в обществе Комитет по молодежной  13 признаков учителя
13 признаков учителя Тема: Повесть Н.В.Гоголя «Тарас Бульба». Отец и сыновья. Характеры главных героев
Тема: Повесть Н.В.Гоголя «Тарас Бульба». Отец и сыновья. Характеры главных героев Термические ожоги (5 класс)
Термические ожоги (5 класс) Культура Древнего Востока Выполнила ученица 10 класса «В» Коньшина Настя
Культура Древнего Востока Выполнила ученица 10 класса «В» Коньшина Настя