Слайд 2Кальций в земной коре
Среди металлов к самым распространенным в природе элементам относится

кальций. Массовая доля кальция в земной коре – 4,1%. Строение атомов кальция, элемента главной подгруппы II группы ПС Д. И. Менделеева, обуславливает его химическую активность. Поэтому в среде, насыщенной кислородом и водными парами, существование кальция в форме простого вещества невозможно. Зато в составе соединений кальций участвует в образовании пластов горных пород, что позволило широко использовать породы и минералы, образованные им, в строительстве, архитектуре, скульптуре.
Слайд 3Кальций в земной коре
В образовании соединений кальция огромную роль играл углекислый газ,

который являлся продуктом жизнедеятельности организмов и в обилии содержался и в атмосфере, и в воде. При его участии образовывались соли, в том числе карбонаты СaCO3 и гидрокарбонаты кальция Ca(HCO3)2. Большая часть этих солей была смыта природными водами и снесена реками в Мировой океан, насытив его воды ионами кальция. На протяжении миллионов лет растворенные в морской воде соединения кальция использовались как строительный материал для наружных скелетов беспозвоночных – моллюсков, полипов и др. В неживой природе минерал, который почти на 100% состоит из карбоната кальция, - это кальцит.
Слайд 4Кальций в земной коре
Карбонат
кальция
Кальцит

Слайд 5Памуккале
Памуккале́— природный объект в провинции Денизли на юго-западе Турции. Ослепительно белые террасы

(травертиновые образования) возникли на склоне горы в результате отложения солей из насыщенных кальцием источников.
Слайд 7Мрамор
Мрамор (от греч. мармарос – «блестящий камень») представляет собой горную породу, состоящую

из кристаллов минерала кальцита. Мраморы различаются по свойствам, поскольку обладают различным строением. Строение зависит от условий возникновения, от химического состава и строения известняков, из которых образовался данный конкретный мрамор. Мраморы могут быть сложены из более или менее крупных зерен кальцита. Например, греческие мраморы – паросский, добываемый на острове Парос, и пентелийский из горы Пентиликон – среднезернистые. Каррарский мрамор из Италии – мелкозернистый.
Слайд 8Мрамор
В России каррарский мрамор использовали при строительстве нескольких фонтанов Петергофа. Благодаря зернистому

строению мраморы не предрасположены к растрескиванию. Окончательная обработка пемзой и полировка придают их поверхности блеск и прочность. Окраска мрамора зависит от содержащихся в нем химических примесей. На Урале разрабатывают месторождение, дающее белый, белый с желтыми прожилками, черный, серо-белый, серый с прожилками, пестрый и др. мраморы. Белые сорта являются самыми предпочтительными для ваяния. Окрашенные мраморы тивдийский розовый, красный из Прибайкалья, кремовый, медовый, серый с Урала применяются для облицовки стен, колонн.
Слайд 10Мрамор
Мраморный дворец в Санкт-Петербурге, построенный по проекту Антонио Ринальди
Розовый мрамор в облицовке

колонн
Слайд 12Мрамор
Ханский дворец в Бахчисарае.

Слайд 13Известь
В качестве сырья для производства извести используется мел, известняк и другие природные

источники CaCO3. Термическим разложением кальцита получают негашеную, или жженую, известь - оксид кальция: CaCO3→CaO+CO2
Обжиг известняка проводят в специальных печах при 900-1100⁰ С. Этот процесс называют кальцинированием. Сырье смешивают с коксом и сжигают в токе воздуха. Известь образуется в виде крупных комьев серого или желтоватого цвета, содержит много примесей.
Чтобы известь могла служить связующим материалом, ее «гасят» водой, и получают гашеную известь. CaO+H2O→Ca(OH)2 +65кДж
Слайд 14Известь
Гашение сопровождается выделением большого количества тепла, вода закипает, водяные пары разрыхляют известь,

и она превращается в высокодисперсный порошок.
Известь – основа строительства, фресковой живописи. С глубокой древности стены культовых зданий и дворцов украшали настенной росписью – фресками. Прежде чем создавать фреску, стены покрывали слоем специального грунта – штукатурки, содержащей известь.
Слайд 15Известь
Известь негашеная
комовая.
Известь
гашеная

Слайд 16Известь
Фреска с изображением Посейдона и его жены Амфитриты.

Слайд 17Вывод
Такими образом, соединения кальция в строительстве и природе встречаются повсеместно. Я не

представляю свою жизнь без соединения кальция.
















 Федерализм
Федерализм Молоко
Молоко Производная и её геометрический смысл
Производная и её геометрический смысл Инвестиционно-финансовая группа
Инвестиционно-финансовая группа Беспроводная передача электричества
Беспроводная передача электричества Презентация на тему Кодирование графической информации
Презентация на тему Кодирование графической информации Использование деятельного подхода в ОД при формировании ОБЖ
Использование деятельного подхода в ОД при формировании ОБЖ Он-лайн система управленческого учета
Он-лайн система управленческого учета Типы реакций
Типы реакций Энергия солнца в Вашем Доме!
Энергия солнца в Вашем Доме! Московские лабораторииэкономики и технологии знанийпредставляют
Московские лабораторииэкономики и технологии знанийпредставляют Электроёмкость. Конденсаторы
Электроёмкость. Конденсаторы Измерение высоты здания разными способами
Измерение высоты здания разными способами Словообразования
Словообразования Восточная Европа
Восточная Европа Презентация на тему Инвестиции
Презентация на тему Инвестиции Получение наличных средств в сети круглосуточных банкоматов Сбербанка России и других банков по всему миру Безналичная оплата то
Получение наличных средств в сети круглосуточных банкоматов Сбербанка России и других банков по всему миру Безналичная оплата то Предпосылки петровских преобрахований
Предпосылки петровских преобрахований Люблю я Кавказ
Люблю я Кавказ Принцип построения сети ОКС №7. Режимы сигнализации
Принцип построения сети ОКС №7. Режимы сигнализации Программы обучения онлайн 2020
Программы обучения онлайн 2020 Дорогие ребята! Мы шагаем в проект «Среди миров»
Дорогие ребята! Мы шагаем в проект «Среди миров» Кашира
Кашира International Corporate Match Race 10-11 September 2011 Yacht Club of Greece
International Corporate Match Race 10-11 September 2011 Yacht Club of Greece Уголовный процесс Чешской республики
Уголовный процесс Чешской республики Парад студенчества 2018
Парад студенчества 2018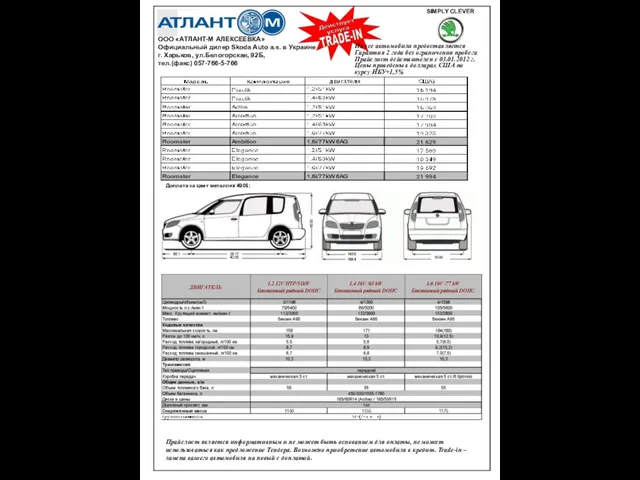 На все автомобили предоставляется Гарантия 2 года без ограничения пробега Прайслист действителен с 03.01.2012 г. Цены приведены в долла
На все автомобили предоставляется Гарантия 2 года без ограничения пробега Прайслист действителен с 03.01.2012 г. Цены приведены в долла О создании Восточно-Сибирского научно образовательного инновационного комплекса в Республике Бурятия
О создании Восточно-Сибирского научно образовательного инновационного комплекса в Республике Бурятия