Содержание
- 2. С О Е Д И Н Е Н И Я С Е Р Ы
- 3. степень окисления серы -2 Сероводород - Н2S Сульфиды неметаллов – CS2, P2S3 Сульфиды металлов – Al2S3,
- 4. Н2S СЕРОВОДОРОД Это - ядовитый газ со специфическим запахом, тяжелее воздуха и кислорода, растворимый в воде.
- 5. Получение: водород + сера H2 + S ----H2S сульфид металла + сильная кислота ZnS + 2HCL---ZnCl2
- 6. Сульфиды металлов - соли от сероводородной кислоты Сульфиды образованы очень слабой кислотой, поэтому все подвергаются гидролизу
- 7. степень окисления серы + 4 Сернистый газ –SO2 Сернистая кислота –H2SO3 Сульфиты – K2SO3, BaSO3
- 8. СЕРНИСТЫЙ ГАЗ SO2 Оксид серы(lV) – сернистый газ, являющийся одним из главных загрязнителей атмосферного воздуха, кислотный
- 9. Получение: разложение сернистой кислоты H2SO3 -----SO2 + H2O сгорание серы S + O2 ---SO2 обжиг сульфидов
- 10. Химические свойства: с водой SO2 + H2O---H2SO3 с основными оксидами SO2 + BaO---BaSO3 с щелочами SO2
- 11. Составьте уравнения реакций оксида серы (Vl) с водой, оксидом натрия, гидроксидом кальция, оксидом алюминия. Назовите продукты
- 12. Сернистая кислота – очень слабая, неустойчивая, легко разлагается на сернистый газ и воду (является аналогом угольной
- 13. степень окисления серы + 6 Серный ангидрид или оксид серы (Vl) –SO3 Серная кислота –H2SO4 Сульфаты
- 14. Оксид серы (Vl) – кислотный оксид, получается при окислении сернистого газа 2SO2 + O2---2SO3 Химические свойства
- 15. Н2SO4 Два вида солей от серной кислоты: средние – сульфаты CaSO4 и кислые – гидросульфаты Ba(HSO4)2
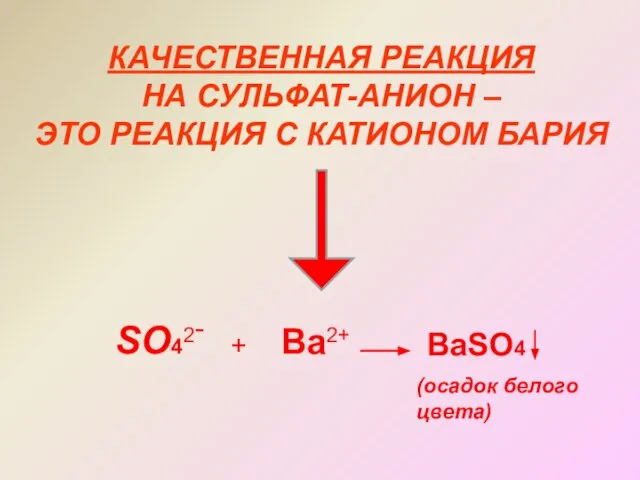
- 16. КАЧЕСТВЕННАЯ РЕАКЦИЯ НА СУЛЬФАТ-АНИОН – ЭТО РЕАКЦИЯ С КАТИОНОМ БАРИЯ SO42- + Ba2+ BaSO4 (осадок белого
- 17. Н2SO4 Серная кислота - тяжелая бесцветная жидкость, которая бывает концентрированная и разбавленная, в зависимости от этого
- 18. Взаимодействие разбавленной и концентрированной кислоты с металлами разной активности
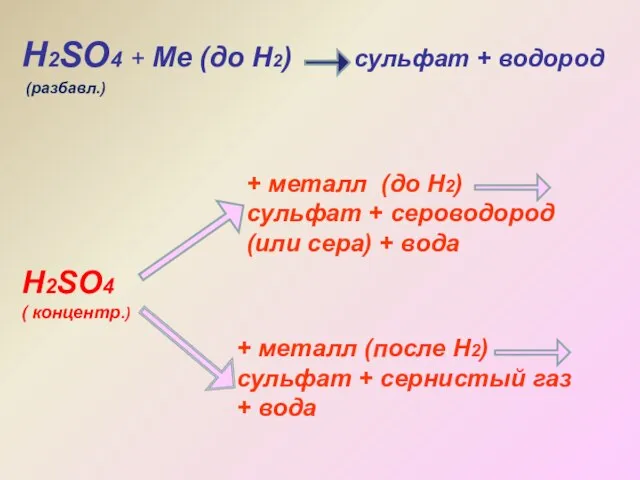
- 19. Н2SO4 + Ме (до Н2) сульфат + водород Н2SO4 ( концентр.) + металл (до Н2) сульфат
- 20. Выполните задание по вариантам: 1 вариант – сернистый газ 2 вариант – серная кислота Вам даны
- 21. Это простое вещество Это соединение с высшей степенью окисления серы 3. Это сильный электролит 4. Это
- 22. Сульфат меди(ll) Сульфат алюминия Сульфат бария Сульфат хрома(lll) Сульфат железа(ll) Сульфат кобальта Найдите соответствие между названием
- 23. Самостоятельная работа по вариантам:
- 24. 1 вариант 2 вариант Составить о.в.р: Серная кислота разб. + натрий 2. Серная кислота разб. +
- 26. Скачать презентацию




















 Инструкция по монтажу проходного элемента Muotokate на металлочерепицу Монтерроса
Инструкция по монтажу проходного элемента Muotokate на металлочерепицу Монтерроса Презентация на тему Матренин двор
Презентация на тему Матренин двор Презентация на тему Официально-деловой стиль ФУНКЦИОНАЛЬНЫЕ СТИЛИ РУССКОГО ЛИТЕРАТУРНОГО ЯЗЫКА
Презентация на тему Официально-деловой стиль ФУНКЦИОНАЛЬНЫЕ СТИЛИ РУССКОГО ЛИТЕРАТУРНОГО ЯЗЫКА День Победы
День Победы Презентация ЖК ЖАСМИН
Презентация ЖК ЖАСМИН Управление реализацией стратегии
Управление реализацией стратегии Потенциал развития ресурсной базы металлургической промышленностиСибири и Дальнего Востока.Проблемы и перспективы
Потенциал развития ресурсной базы металлургической промышленностиСибири и Дальнего Востока.Проблемы и перспективы Простейшие задачи
Простейшие задачи Основы фотокомпозиции. Задания для учащихся
Основы фотокомпозиции. Задания для учащихся English Literature
English Literature THiNK center
THiNK center Рекомендации по заполнению форм технологических карт межведомственного взаимодействия
Рекомендации по заполнению форм технологических карт межведомственного взаимодействия Prezentatsia10
Prezentatsia10 "Открывая новое, создаем себя"
"Открывая новое, создаем себя" “Энергоэффективности на региональном уровне в Архангельской, Астраханской и Калининградской областях”
“Энергоэффективности на региональном уровне в Архангельской, Астраханской и Калининградской областях”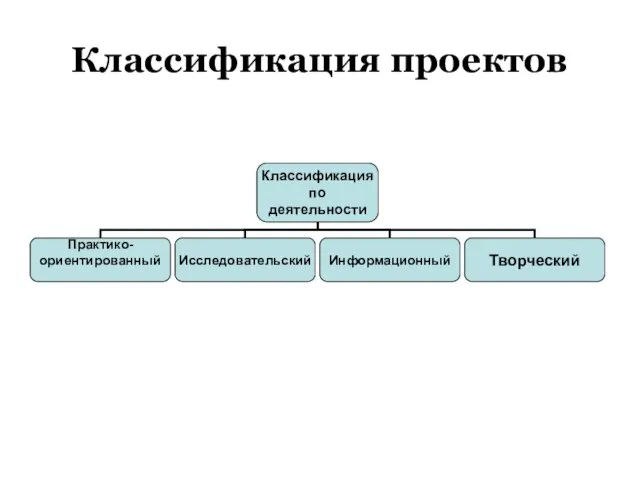 Классификация проектов
Классификация проектов Роспись по шелку
Роспись по шелку О лекарственном обеспечении отдельных категорий граждан
О лекарственном обеспечении отдельных категорий граждан Дорога в самостоятельную жизнь
Дорога в самостоятельную жизнь Презентация на тему Русская культура Серебряного века
Презентация на тему Русская культура Серебряного века  Общероссийская конференция МЕТОДИКА И ПЕДАГОГИЧЕСКАЯ ПРАКТИКА Электронный журнал Конференц-зал
Общероссийская конференция МЕТОДИКА И ПЕДАГОГИЧЕСКАЯ ПРАКТИКА Электронный журнал Конференц-зал Четырёхзначные числа
Четырёхзначные числа Социально-психологический портрет военного, сотрудника подразделения “Cпецназ”
Социально-психологический портрет военного, сотрудника подразделения “Cпецназ” Соблюдение соответствия образовательной организации лицензионным требованиям
Соблюдение соответствия образовательной организации лицензионным требованиям Увольнение с военной службы и пребывание в запасе
Увольнение с военной службы и пребывание в запасе Современное декоративное искусство. 5 класс
Современное декоративное искусство. 5 класс Дрифт - мой любимый вид автоспорта
Дрифт - мой любимый вид автоспорта ВОСПИТАТЕЛЬНЫЙ ПОТЕНЦИАЛ СЕМЬИ Смесь из любви и дисциплины – Вот золотая середина; И словно врач, что вены отворяет, Она и ранит, но и исцеляет…
ВОСПИТАТЕЛЬНЫЙ ПОТЕНЦИАЛ СЕМЬИ Смесь из любви и дисциплины – Вот золотая середина; И словно врач, что вены отворяет, Она и ранит, но и исцеляет…