Содержание
- 2. Спектроскопия УФ- и видимого диапазона Д.В. Козлов, Г.А. Костин, А.П. Чупахин «Основные принципы спектроскопии и ее
- 3. Электронная (ультрафиолетовая) спектроскопия изучает энергетические переходы между валентными молекулярными орбиталями. E = E1- Е0= hν =
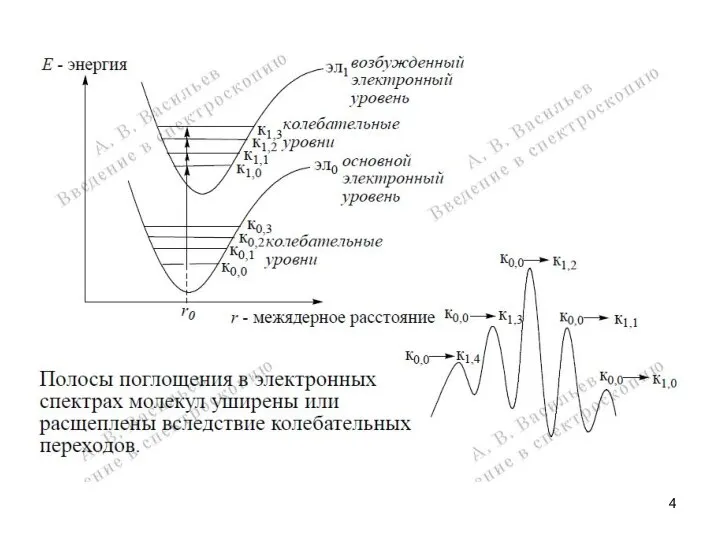
- 5. Характеристика электронных переходов Большинство электронных переходов в молекулах проявляются в диапазоне 200-750 нм, который подразделяется на
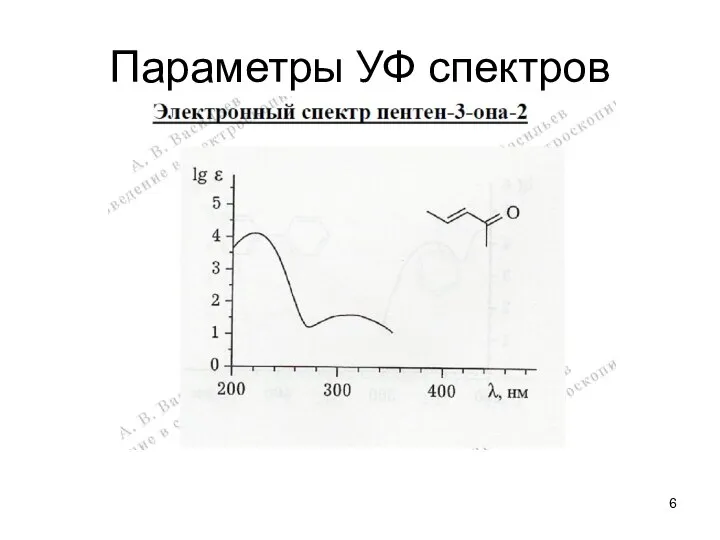
- 6. Параметры УФ спектров
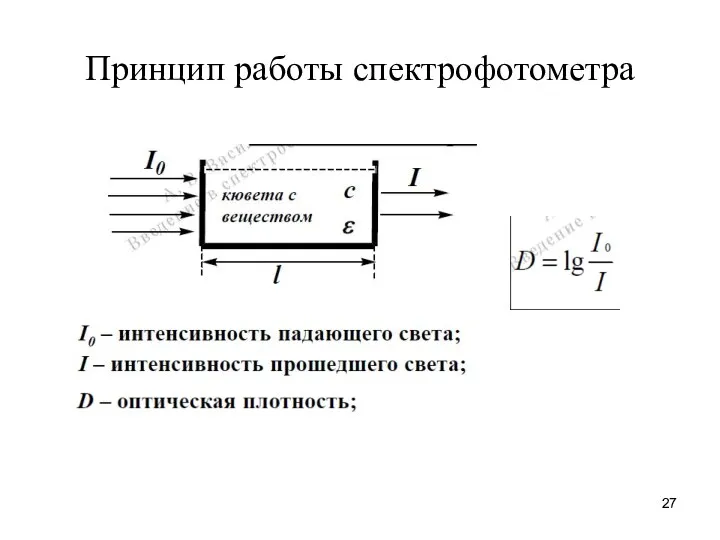
- 7. Закон Бугера-Ламберта-Бера – основной закон оптической спектроскопии D= ε*c*l D – оптическая плотность; с – концентрация
- 8. Спектроскопия УФ- и видимого диапазона Каждый Охотник Желает Знать Где Сидит Фазан
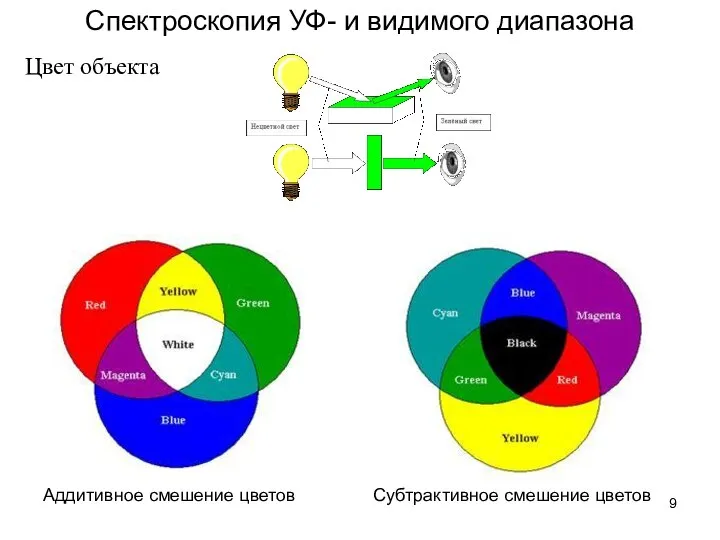
- 9. Спектроскопия УФ- и видимого диапазона Цвет объекта Аддитивное смешение цветов Субтрактивное смешение цветов
- 10. Аддитивное смешение цветов - метод синтеза цвета, основанный на сложении цветов непосредственно излучающих объектов. RGB- система
- 11. Субтрактивный синтез цвета - получение цвета путём вычитания из спектрально-равномерного белого света отдельных спектральных составляющих. CMYK
- 12. Спектроскопия УФ- и видимого диапазона Примерные границы основных цветов спектра Цвет объекта
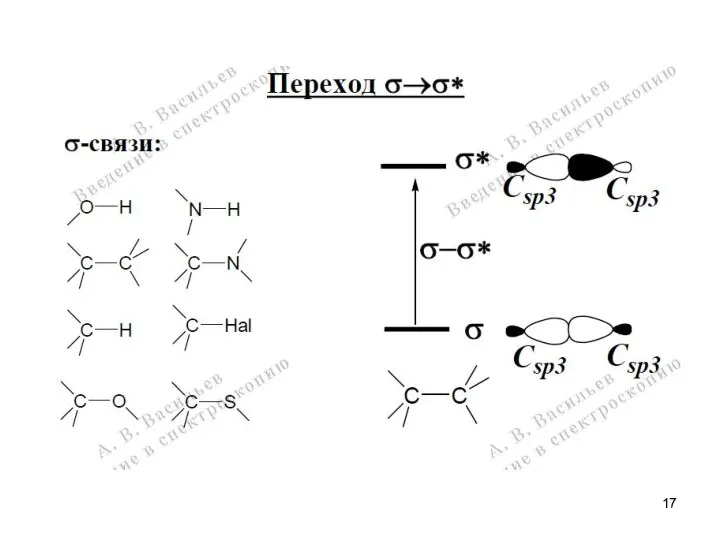
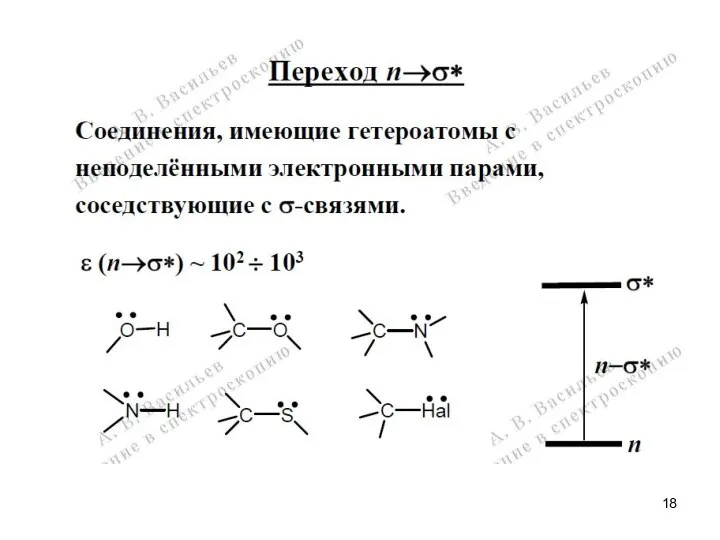
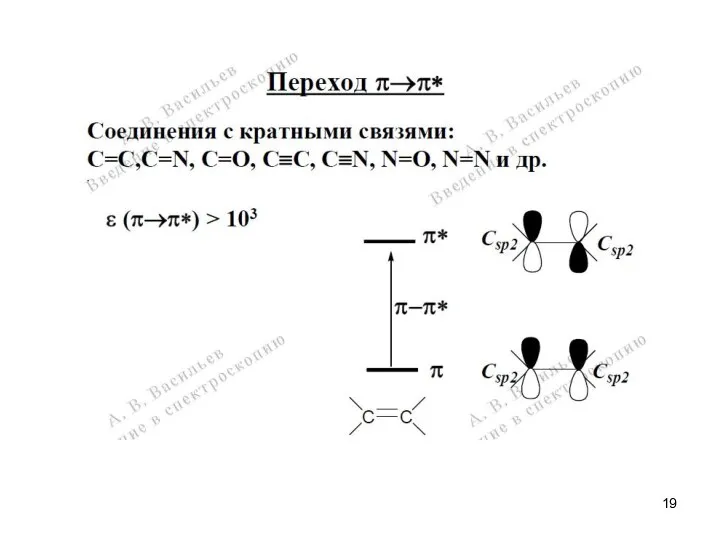
- 13. Энергия переходов
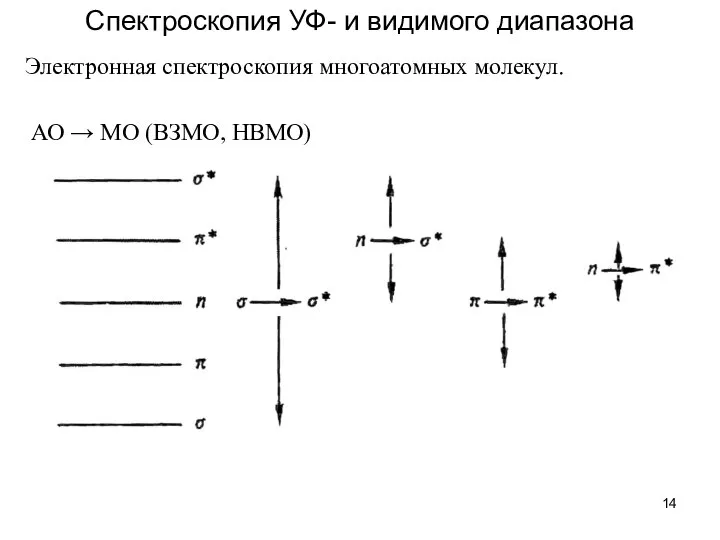
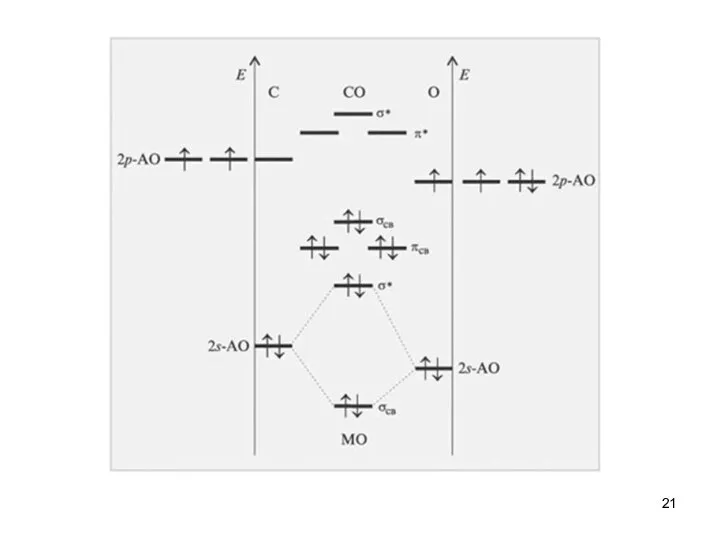
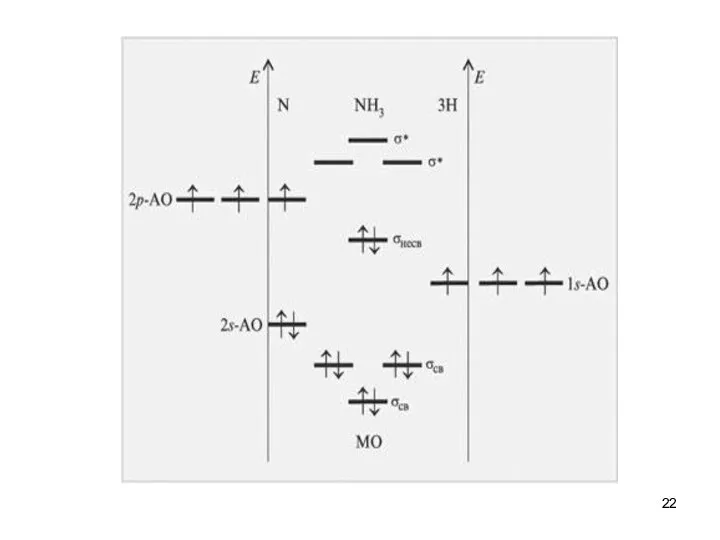
- 14. Спектроскопия УФ- и видимого диапазона Электронная спектроскопия многоатомных молекул. АО → МО (ВЗМО, НВМО)
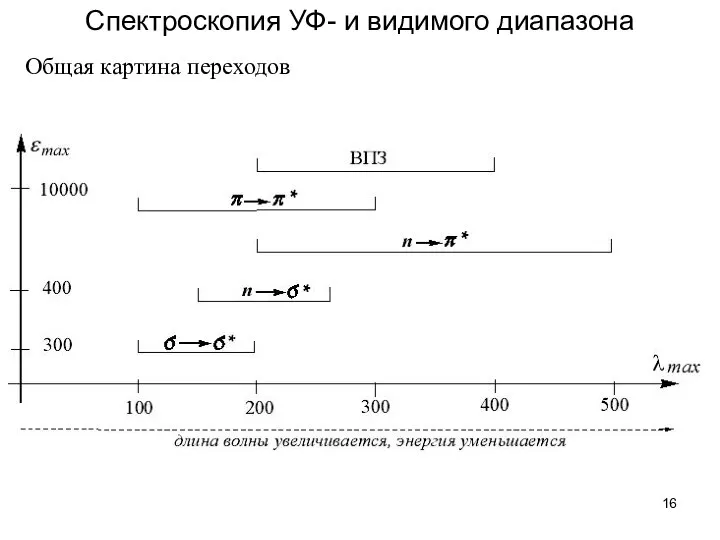
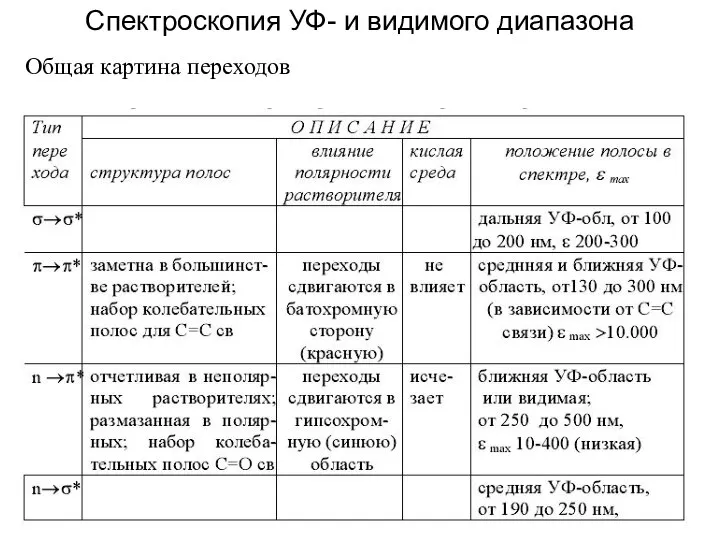
- 16. Спектроскопия УФ- и видимого диапазона Общая картина переходов
- 23. Задача Обосновать изменение окраски в ряду газообразных молекулярных галогенов: F2 - светло-желтый, Сl2 – желто-зеленый, Br2
- 24. Спектроскопия УФ- и видимого диапазона Общая картина переходов
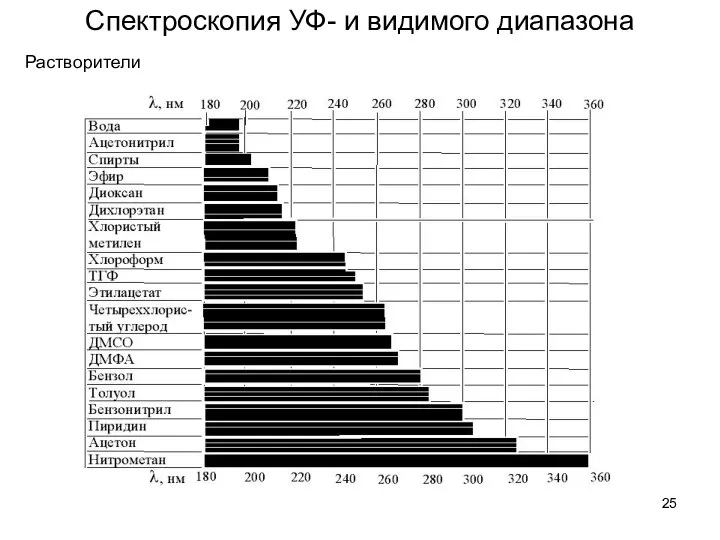
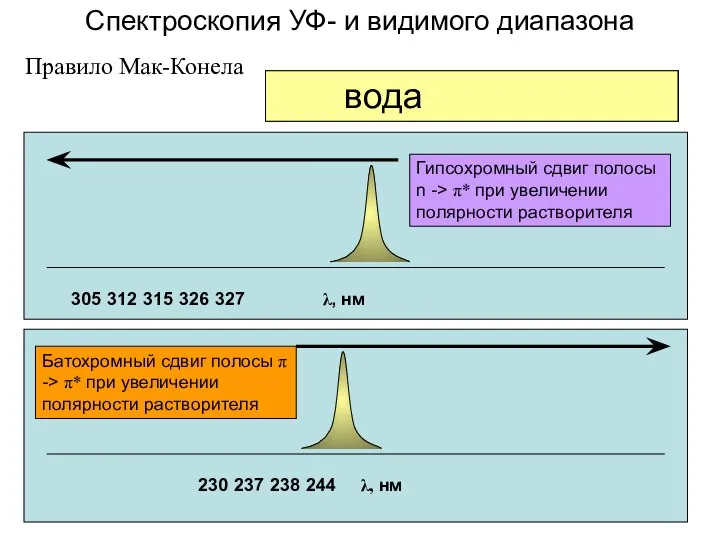
- 25. Спектроскопия УФ- и видимого диапазона Растворители
- 26. 230 237 238 244 λ, нм 305 312 315 326 327 λ, нм гексан диэтиловый эфир
- 27. Принцип работы спектрофотометра
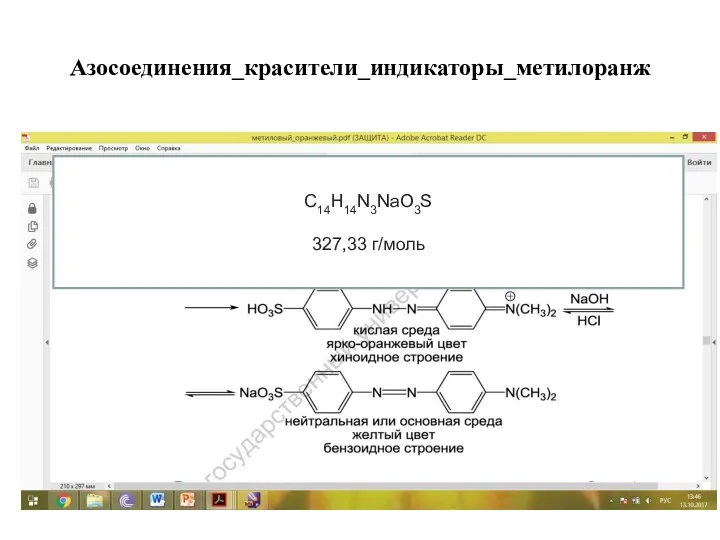
- 28. Азосоединения_красители_индикаторы_метилоранж C14H14N3NaO3S 327,33 г/моль
- 30. Скачать презентацию












 3_Samomenedzhment
3_Samomenedzhment Декор русской избы
Декор русской избы Лекция_БУ и обруд для бур на суше
Лекция_БУ и обруд для бур на суше Внедрение системы веб-аналитики в информационный сайт
Внедрение системы веб-аналитики в информационный сайт Состояние электрона в многоэлектронном атоме. Периодическая система элементов Менделеева. Спонтанное и вынужденное излучение. Ла
Состояние электрона в многоэлектронном атоме. Периодическая система элементов Менделеева. Спонтанное и вынужденное излучение. Ла DUOLITH SD1Storz Medical AG (Швейцария)
DUOLITH SD1Storz Medical AG (Швейцария) КФС без границ. Первые бизнес-шаги в новом маркетинге
КФС без границ. Первые бизнес-шаги в новом маркетинге Metal–metal multiple bonded intermediates in catalysis
Metal–metal multiple bonded intermediates in catalysis  РЕФОРМИРОВАНИЕ СИСТЕМЫ УПРАВЛЕНИЯ ОХРАНОЙ ТРУДА В СОВРЕМЕННЫХ УСЛОВИЯХ РАЗВИТИЯ ЭКОНОМИКИДиректор Департамента заработной пла
РЕФОРМИРОВАНИЕ СИСТЕМЫ УПРАВЛЕНИЯ ОХРАНОЙ ТРУДА В СОВРЕМЕННЫХ УСЛОВИЯХ РАЗВИТИЯ ЭКОНОМИКИДиректор Департамента заработной пла Государственные символы Российской Федерации и Москвы(исследовательская и творческая работа)
Государственные символы Российской Федерации и Москвы(исследовательская и творческая работа) Beverone - международный партнерский проект
Beverone - международный партнерский проект Итоги I четверти
Итоги I четверти Память
Память Инструкция по монтажу элементов к оформлению витрин
Инструкция по монтажу элементов к оформлению витрин Ярмарка вакансий. ИКЦ Безопасность гидротехнических сооружений
Ярмарка вакансий. ИКЦ Безопасность гидротехнических сооружений Кафе Бременские музыканты
Кафе Бременские музыканты Студенческое научное общество Юридического факультета Северо-Западного института управления РАНХиГС
Студенческое научное общество Юридического факультета Северо-Западного института управления РАНХиГС Легкий способ продавать товары и услуги в интернете через Postmarket.kz
Легкий способ продавать товары и услуги в интернете через Postmarket.kz Организация Шркстан
Организация Шркстан Интегрированный урок в начальной школе
Интегрированный урок в начальной школе Состав Вооруженных Сил Российской Федерации
Состав Вооруженных Сил Российской Федерации Предмет философии
Предмет философии 5_Нейродинамические_свойства_человека
5_Нейродинамические_свойства_человека Осторожно -ДЕТИ!
Осторожно -ДЕТИ! Эволюционно-генетические аспекты иммунологии репродукции
Эволюционно-генетические аспекты иммунологии репродукции Роль самооценки в формировании личности
Роль самооценки в формировании личности Изменение имён прилагательных по родам и числам
Изменение имён прилагательных по родам и числам Общегосударственное противодействие терроризму
Общегосударственное противодействие терроризму