Содержание
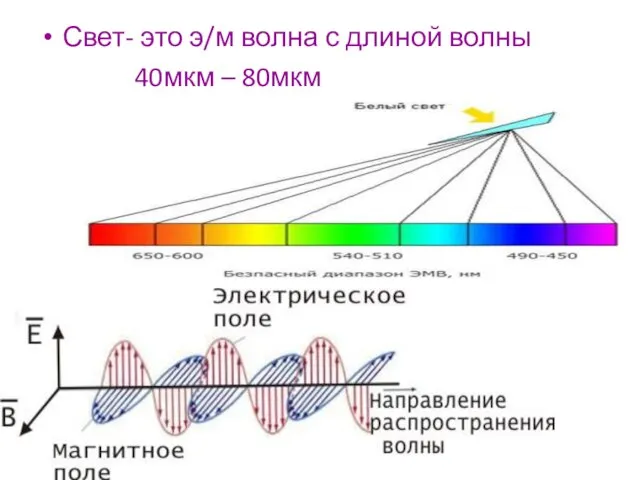
- 2. Свет- это э/м волна с длиной волны 40мкм – 80мкм
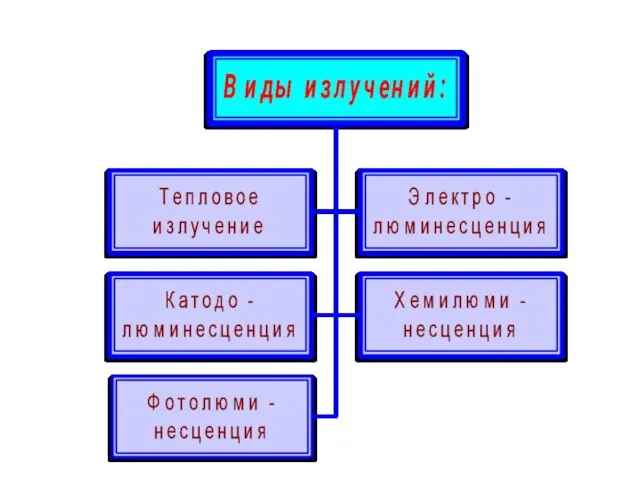
- 3. Для того чтобы атом начал излучать, ему необходимо передать определенную энергию.
- 5. Спектры и спектральные аппараты Спектр с латинского «дух, приведение»
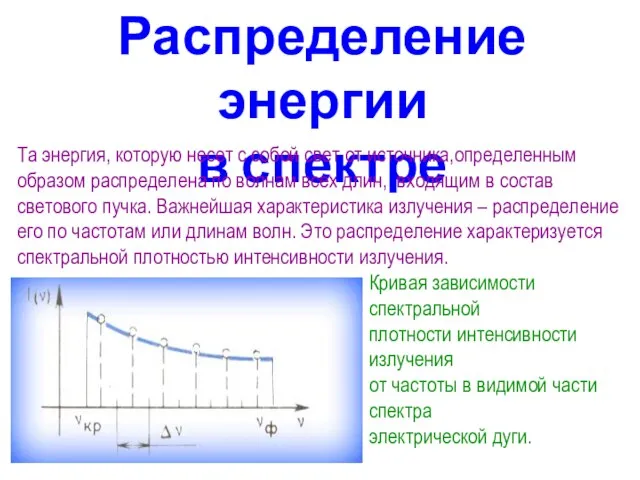
- 6. Распределение энергии в спектре Та энергия, которую несет с собой свет от источника,определенным образом распределена по
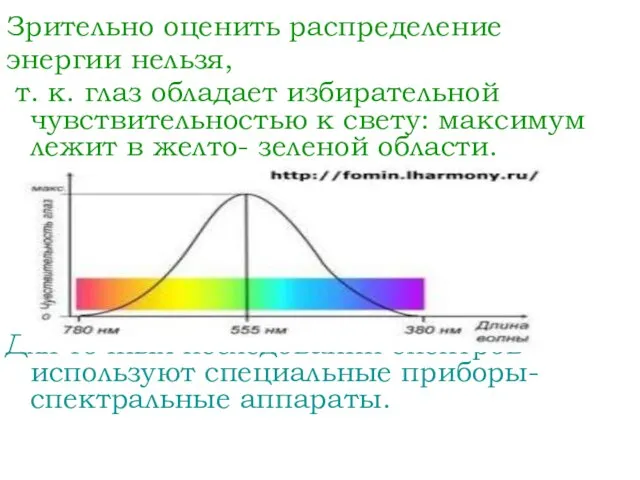
- 7. Зрительно оценить распределение энергии нельзя, т. к. глаз обладает избирательной чувствительностью к свету: максимум лежит в
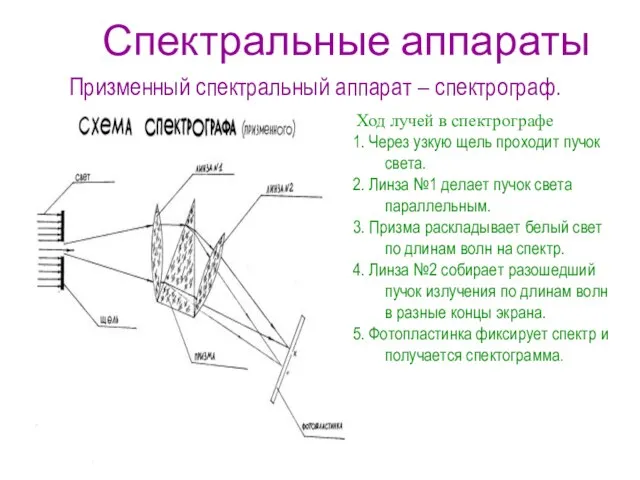
- 8. Спектральные аппараты Ход лучей в спектрографе 1. Через узкую щель проходит пучок света. 2. Линза №1
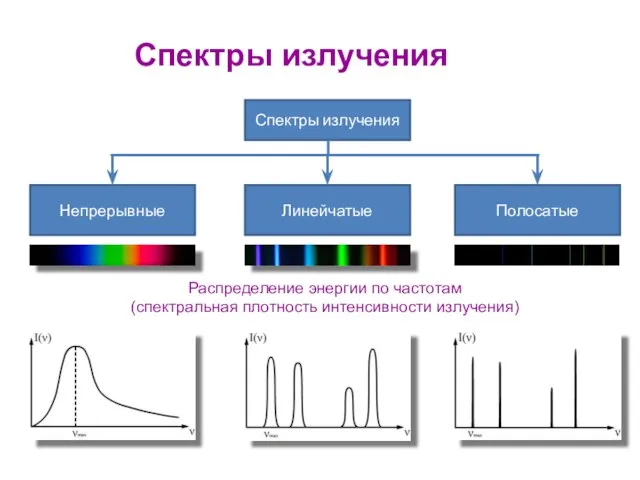
- 9. Распределение энергии по частотам (спектральная плотность интенсивности излучения) Спектры излучения
- 10. Дают тела, находящиеся в твердом, жидком состоянии, а также плотные газы. Чтобы получить, надо нагреть тело
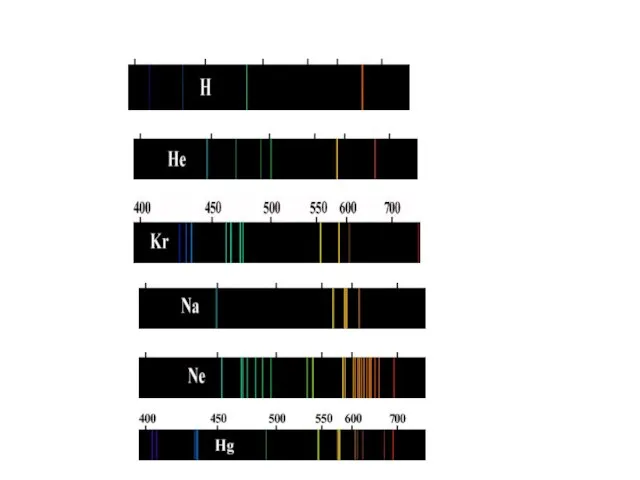
- 11. Дают все вещества в газообразном атомном (но не молекулярном) состоянии (атомы практически не взаимодействуют друг с
- 12. Спектр состоит из отдельных полос, разделенных темными промежутками. Каждая полоса представляет собой совокупность большого числа очень
- 13. Если пропускать белый свет сквозь холодный, неизлучающий газ, то на фоне непрерывного спектра источника появятся темные
- 14. Густав Роберт Кирхгоф 1824 - 1887 Роберт Вильгельм Бунзен 1811 - 1899 Спектральный анализ – метод
- 16. Длины волн (или частоты) линейчатого спектра какого-либо вещества зависят только от свойств атомов этого вещества, но
- 17. Открываются новые элементы: рубидий, цезий и др; Узнали химический состав Солнца и звезд; Определяют химический состав
- 19. Скачать презентацию








 ШКОЛА ОТВЕТСТВЕННЫХ РОДИТЕЛЕЙ Информационно-методическое пособие для медицинских работников и педагогов Автор-составитель Т.Р.
ШКОЛА ОТВЕТСТВЕННЫХ РОДИТЕЛЕЙ Информационно-методическое пособие для медицинских работников и педагогов Автор-составитель Т.Р.  Вулканы Камчатки
Вулканы Камчатки Животные живого уголка
Животные живого уголка Оценка эффективности здоровьесберегающей деятельности школы родителями учащихся
Оценка эффективности здоровьесберегающей деятельности школы родителями учащихся Открытия и изобретения в химии
Открытия и изобретения в химии Скоро начинаем: ждем пока все соберутся…
Скоро начинаем: ждем пока все соберутся… ВКР: Разработка услуги по утилизации автомобилей в сервисном центре ООО АвтоДепо
ВКР: Разработка услуги по утилизации автомобилей в сервисном центре ООО АвтоДепо Население мира
Население мира Влияние радиации на человека
Влияние радиации на человека Датский волшебник и его сказки
Датский волшебник и его сказки Виды информации
Виды информации Результаты диагностики сформированности познавательных универсальных учебных действий
Результаты диагностики сформированности познавательных универсальных учебных действий Правовые основы воинской службы
Правовые основы воинской службы Село Загоскино История нашего села Загоскино – это часть истории России. Загоскинская земля славится не дворцами и небоскрёбами,
Село Загоскино История нашего села Загоскино – это часть истории России. Загоскинская земля славится не дворцами и небоскрёбами,  Экономическое учение Адама Смита
Экономическое учение Адама Смита Работа с паямив системе интернет-трейдинга Aton-Line
Работа с паямив системе интернет-трейдинга Aton-Line Content_Changes
Content_Changes Школа БЕЗ наркотиков
Школа БЕЗ наркотиков Презентація(1)(1)
Презентація(1)(1) Организация ремонтной службы предприятия. Её задачи и функции
Организация ремонтной службы предприятия. Её задачи и функции Кровь: состав и значение
Кровь: состав и значение Итоговая презентация 4 группы
Итоговая презентация 4 группы Элективные курсы для предпрофильной подготовки по физике
Элективные курсы для предпрофильной подготовки по физике Проектирование Сайта по аренде картингов Go kart
Проектирование Сайта по аренде картингов Go kart 5/ Цифрове відео
5/ Цифрове відео Экваториальные леса Южной Америки
Экваториальные леса Южной Америки Путешествие в Великобританию
Путешествие в Великобританию Программа поддержки приложений для социальной сети Mой Мир@Mail.ru Вирин Федор, директор по исследованиямхолдинга Mail.ru,
Программа поддержки приложений для социальной сети Mой Мир@Mail.ru Вирин Федор, директор по исследованиямхолдинга Mail.ru,