Слайд 2Выделяют следующие особенности комплексов переходных металлов, определяющих их каталитическую активность:
способность образовывать комплексы

с молекулами различных типов, которые, входя в координационную сферу металла – комплексообразователя, активируются, что обеспечивает легкость их дальнейшего взаимодействия.
Слайд 4Выделяют следующие особенности комплексов переходных металлов, определяющих их каталитическую активность:
образование комплексов с

координирующим ионом или атомом металла понижает энергию связи реагирующих молекул субстратов, что уменьшает энергии активации их последующих реакций по сравнению с некоординированными молекулами.
Слайд 5Выделяют следующие особенности комплексов переходных металлов, определяющих их каталитическую активность:
в координационной сфере

металла молекулы изменяют свои кислотные или основные свойства, и возникает возможность кислотно-основного взаимодействия при тех значениях рН, при которых свободная молекула не реагирует.
если имеется запрет по симметрии молекулярных орбиталей, препятствующий взаимодействию молекул, то при реакции в координационной сфере металла он может сниматься или значительно ослабляться.
металлокомплексный катализ позволяет осуществить реакции многоэлектронного окисления и восстановления, в которых молекула субстрата в координационной сфере сразу принимает или отдает несколько электронов.
Слайд 6Основные типы реакций, катализируемых комплексами металлов
Гидрирование:металлокомплексы на основе платиновых металлов, иридиевые и

комплексы, Al(C2H5)3 , катализаторы Циглера – Натты, также гидриды металлоценов
Синтезы с участием оксида углерода: октакарбонил Со, фосфиновые и фосфитные комплексы Rh, Ni(СО)4
Полимеризация, димеризация, олигомеризация олефинов и ацетиленов:катализаторы Циглера – Натты и др.
Окисление углеводородов в карбонильные соединения и эпоксиды:комплексы Pd, гексакарбонил молибдена Мо(СО)6 или ацетилацетонат ванадила VO(C3H7O2)2.
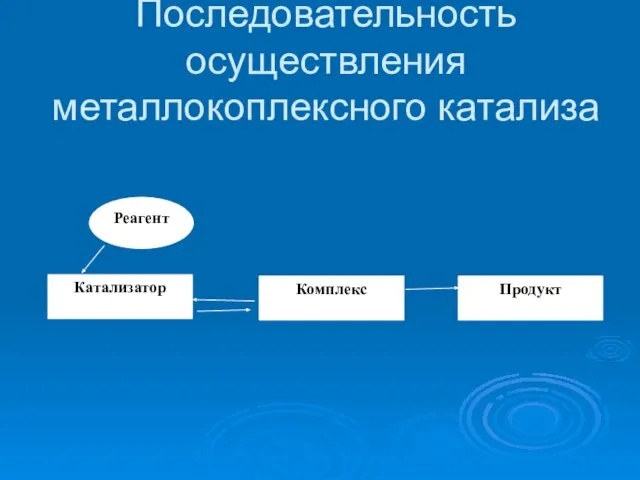
Слайд 7Последовательность осуществления металлокоплексного катализа
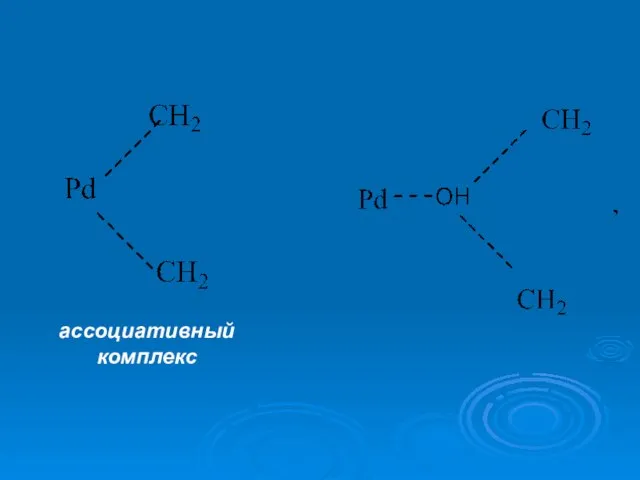
Слайд 8С2Н4+ O2=СН3СНО (уксусный ангидрид–ацетальдегид)
катализатором является комплексное соединение PdCl2. При этом протекают следующие

стадии:
1) PdCl2(С2Н4)(ОН-) PdCl2(С2Н4ОН) (Б1)
2) PdCl2(С2Н4ОН)- PdCl2+ СН3СНО+Н+ (Б2)
Б1, Б2 – окисленная и восстановленная форма палладия соответственно.
Слайд 10Каталитическая активность
где а – каталитическая активность; Ф – отражает величину свободной

энергии металл-лигандного комплекса – снижение закомплексованности (например для PdХ2-4, в ряду Х-=Br‑, Cl‑, F- повышается активность с понижением закомплексованности атомов палладия).
Слайд 12Ферменты
Ферменты (или энзимы) представляют собой высокоспециализированный класс белков, обеспечивающих высокие скорости химических

реакций, протекающих в клетках живых организмов.
Слово «фермент» происходит от латинского fermentum – закваска; другое установившееся название ферментов – энзимы – происходит от греческого en zyme – в дрожжах (термин предложил Ф. В. Кюне в 1878 г.)
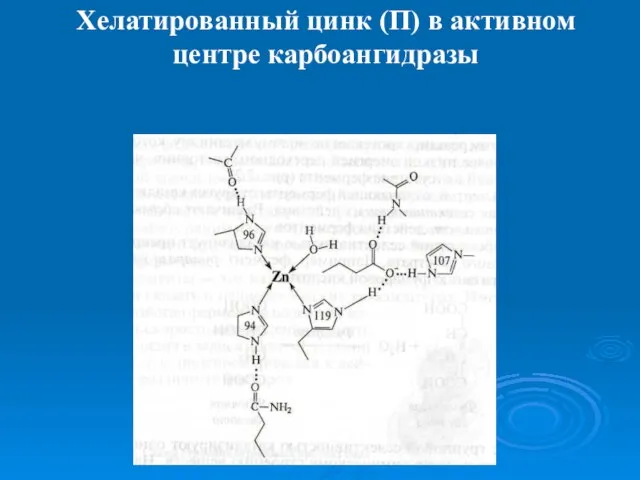
Слайд 14Хелатированный цинк (П) в активном
центре карбоангидразы
Слайд 15Схема, поясняющая механизм снижения энергии активации реакции за счет ферментативного катализа (индекс
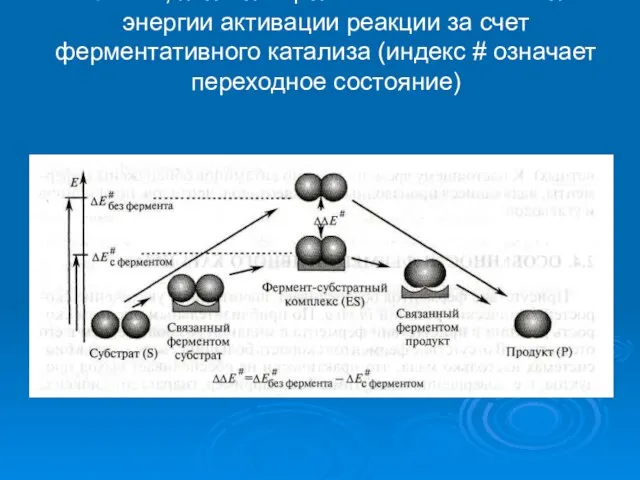
# означает переходное состояние)












 coffee
coffee Спектакли на этой неделе
Спектакли на этой неделе Виды земляных сооружений
Виды земляных сооружений Типи декларацій
Типи декларацій Сайт бесплатных объявлений Купи.ру
Сайт бесплатных объявлений Купи.ру СПИД -болезнь номер один
СПИД -болезнь номер один В мире басен
В мире басен Применение теоремы Пифагора
Применение теоремы Пифагора Национальный состав России
Национальный состав России Проект Тотальная читка
Проект Тотальная читка Всё успевать
Всё успевать Как решать типичные проблемы стартапов?
Как решать типичные проблемы стартапов? Важность реакции на негатив в социальных медиа
Важность реакции на негатив в социальных медиа Презентация на тему Невидимые друзья и враги: вирусы
Презентация на тему Невидимые друзья и враги: вирусы  Технология составления рабочих программ по учебным предметам и курсам внеурочной деятельности
Технология составления рабочих программ по учебным предметам и курсам внеурочной деятельности Резьба по кости. История появления резьбы по кости
Резьба по кости. История появления резьбы по кости Нефть и нефтепродукты
Нефть и нефтепродукты Предпринимательская деятельность. Факторы производства
Предпринимательская деятельность. Факторы производства Презентация на тему Здоровячок - морячок
Презентация на тему Здоровячок - морячок 4 класс Урок русского языка (программа «Гармония»)
4 класс Урок русского языка (программа «Гармония») Great Patriotic War
Great Patriotic War Смысл жизни
Смысл жизни Поддержка систем дистанционного обучения
Поддержка систем дистанционного обучения Are you as green as grass?
Are you as green as grass? Зона степей
Зона степей Страховая защита и безопасность на транспорте. Перспективы развития законодательства в сфере страхования на транспорте, обязател
Страховая защита и безопасность на транспорте. Перспективы развития законодательства в сфере страхования на транспорте, обязател Периодизация психического развития детей. Возрастные кризы. Типы воспитания
Периодизация психического развития детей. Возрастные кризы. Типы воспитания Количество кружков и секций в БГТЭПТК.
Количество кружков и секций в БГТЭПТК.