Содержание
- 2. Французский ученый Луи де Бройль (1892—1987), выдвинул в 1923 г. гипотезу об универсальности корпускулярно-волнового дуализма: не
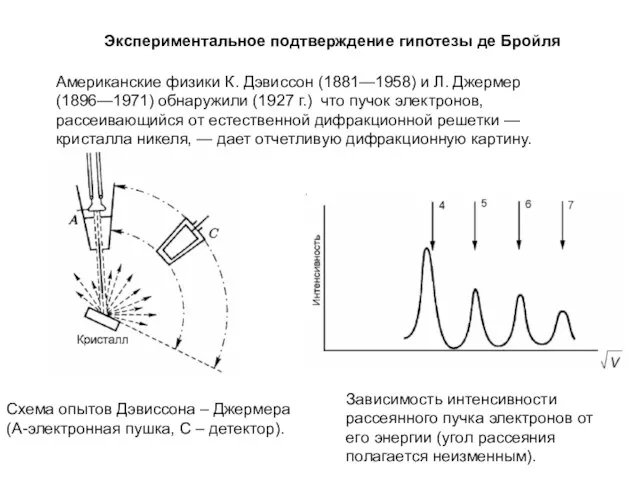
- 3. Экспериментальное подтверждение гипотезы де Бройля Американские физики К. Дэвиссон (1881—1958) и Л. Джермер (1896—1971) обнаружили (1927
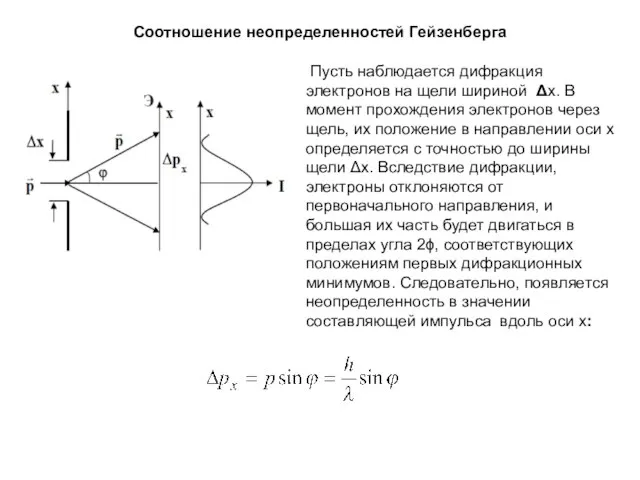
- 4. Соотношение неопределенностей Гейзенберга Пусть наблюдается дифракция электронов на щели шириной Δx. В момент прохождения электронов через
- 5. Первый дифракционный минимум определяется из условия: λ – длина волны де Бройля. Исключая sinϕ , получим:
- 6. В квантовой теории рассматривается также соотношение неопределенностей для энергии E и времени t. Неопределенности этих величии
- 7. Волновая функция и ее свойства Интенсивность волн де Бройля в данной точке пространства связана с числом
- 8. Величина имеет смысл плотности вероятности ρw Сама волновая функция Ψ имеет смысл амплитуды вероятности. Условие нормировки
- 9. Волновая функция позволяет вычислить средние значения физических величин, характеризующих данный микрообъект. Например, среднее расстояние имеет вид:
- 10. Общее уравнение Шредингера Основное уравнение нерелятивистской квантовой механики имеет вид m - масса частицы; - оператор
- 11. Уравнение Шредингера для стационарных состояний Важным частным случаем общего уравнения Шредингера, является уравнение Шредингера для стационарных
- 12. После упрощений получим уравнение Шредингера для стационарных состояний: или Физический смысл имеют только регулярные волновые функции
- 13. Движение свободной частицы Пусть свободная частица движется вдоль оси x. Для такой частицы U(x)=0. Уравнение Шредингера
- 14. Частица в одномерной прямоугольной "потенциальной яме" с бесконечно высокими "стенками" Рассмотрим частицу в одномерной "потенциальной яме"
- 15. Этим граничным условиям удовлетворяет решение уравнения Шредингера при и Поскольку то Таким образом, энергия частицы в
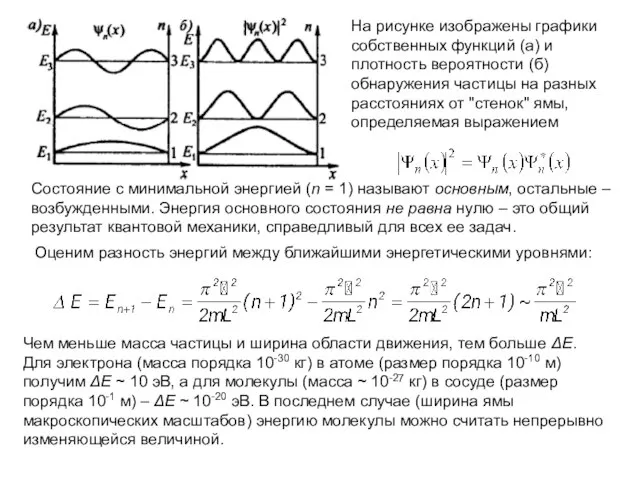
- 16. На рисунке изображены графики собственных функций (а) и плотность вероятности (б) обнаружения частицы на разных расстояниях
- 18. Скачать презентацию












 Презентация на тему Эдуард Мане
Презентация на тему Эдуард Мане  Правоохранительные органы Российской Федерации
Правоохранительные органы Российской Федерации Организация сопровождаемого проживания граждан с нарушениями
Организация сопровождаемого проживания граждан с нарушениями 学校
学校 Типы сварных швов
Типы сварных швов Отчет о размещении вакансий
Отчет о размещении вакансий СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ
СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ Сравнительный анализ развития лыжероллеров
Сравнительный анализ развития лыжероллеров Прыжки в длину
Прыжки в длину Презентация на тему Механические колебания 11 класс
Презентация на тему Механические колебания 11 класс  Понятия частей речи
Понятия частей речи Презентация Нагрузки и воздействия
Презентация Нагрузки и воздействия Презентация на тему Разнообразие животных
Презентация на тему Разнообразие животных  English theater
English theater  Класс Однодольные, характерные признаки растений семейства злаковых
Класс Однодольные, характерные признаки растений семейства злаковых Еңбек нормасы. Өнім нормасы
Еңбек нормасы. Өнім нормасы Формы и методы профессиональной ориентации
Формы и методы профессиональной ориентации e70f443261a743aba5fb4ba5defd798a
e70f443261a743aba5fb4ba5defd798a Функциональные стили речи
Функциональные стили речи Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100"
Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100" Презентация на тему Вельможи Древнего ЕГИПТА
Презентация на тему Вельможи Древнего ЕГИПТА  Маршалы Великой Отечественной войны
Маршалы Великой Отечественной войны Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона
Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона Природный газ
Природный газ Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы
Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы Оркестр. Инструменты симфонического оркестра
Оркестр. Инструменты симфонического оркестра МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА
МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА  Богиня Молва (Фама, Осса)
Богиня Молва (Фама, Осса)