Слайд 2
Элементы содержания блока С-3:
- классификация химических реакций;
-химические свойства классов органических

соединений;
-условия протекания химических реакций;
-обратимые и необратимые реакции;
-химическое равновесие и условия его смещения;
-качественные реакции на классы органических веществ ;
-способы получения органических веществ;
-окислительно-восстановительные реакции;
-гидролиз органических веществ;
-генетическая связь между классами органических соединений.
Задания блока С-3 относятся к высокому уровню сложности, задание должно выполнено в виде развернутого ответа.
Слайд 3Необходимо знать:
1. Именные реакции (Вюрца, Вагнера, Марковникова, З айцева,К учерова,З инина,Г

уставсона, Дюма,Кольбе)
2. Способы увеличения или уменьшения углеродной цепочки( Вюрца, Гриньяра, алкилирование, димеризация, декарбоксилирование)
3. Качественные реакции( с бромной водой, с раствором перманганата калия, с реактивом Фелинга, с реактивом Толленса, с раствором хлорида железаIII, биуретовая реакция, ксантопротеиновая)
4.Условия протекания реакций( температура, катализатор, серная кислота, водный или спиртовый раствор щелочи)
5.Направление О.В.Р. в зависимости от состава, строения вещества, характера среды.
6.Ориетанты I и II рода,индукционный и мезомерный эффект.
7.Специфические свойства муравьиной кислоты.
8.Учитывать возможности взаимодействия продуктов реакции между собой.
Слайд 41Именные реакции:
Вюрца С 2Н 5Cl +2 Na +C 3H 7Cl→ C5
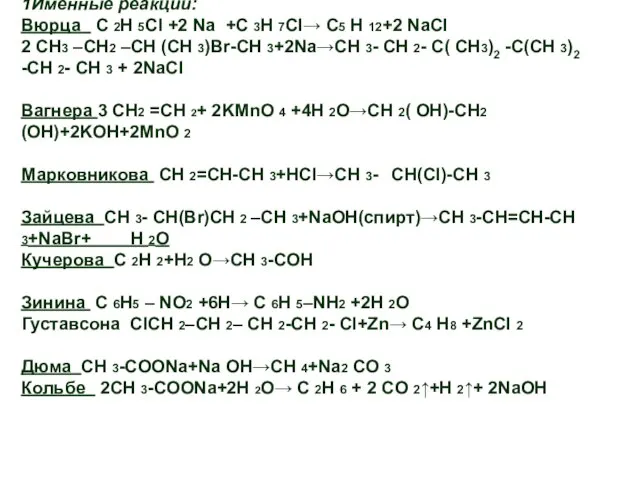
H 12+2 NaCl
2 CH3 –CH2 –CH (CH 3)Br-CH 3+2Na→CH 3- CH 2- C( CH3)2 -C(CH 3)2 -CH 2- CH 3 + 2NaCl
Вагнера 3 CH2 =CH 2+ 2KMnO 4 +4H 2O→CH 2( OH)-CH2 (OH)+2KOH+2MnO 2
Марковникова СН 2=СН-СН 3+НCl→CH 3- CH(Cl)-CH 3
Зайцева СН 3- СН(Вr)CH 2 –CH 3+NaOH(спирт)→СH 3-CH=CH-CH 3+NaBr+ H 2O
Кучерова C 2H 2+H2 O→CH 3-CОН
Зинина C 6H5 – NO2 +6H→ C 6H 5–NH2 +2H 2O
Густавсона ClCH 2–CH 2– CH 2-CH 2- Cl+Zn→ C4 H8 +ZnCl 2
Дюма CH 3-COONa+Na OH→CH 4+Na2 CO 3
Кольбе 2CH 3-COONa+2H 2O→ C 2H 6 + 2 CO 2↑+H 2↑+ 2NaOН
Слайд 5
Изменение длины углеродной цепи:
1. Реактив Гриньяра
СН3 -Mg –Cl+C 2H5 -Cl→

C3H8 +MgCl2
CO2 + CH3-Mg-Cl→ CH3-COOMgCl→ CH3 –COOH +MgCl2
2. Реакция алкилирования
С6 H6 +СН3 –Сl→ C6 Н5 –СН3 +HCl
3. Реакция декарбоксилирования
С6 H5 -COOH→ C6H6 +CO2 ↑
CH3 – CH2 -COONa +NaOH→ C2H6 + Na2CO3
4.Димеризация 2 С2Н2 → винилацетилен
5. Полимеризация
СН2 =СН- СОО –СН3 → Поливинилацетат
Слайд 6
Качественные реакции 1. С2 Н2 + 2 {Ag(NH 3) 2} OH→ C2

Ag 2↓+4 NH3 ↑ + 2Н2 О 2. СH3 COH+2{ Ag(NH3 ) 2 }OH → CH3 COOH+2Ag ↓ +4NH 3 ↑+H 2O 3. C H3 COH + 2 {Ag(NH3 ) 2 }OH → CH 3C00NH4 +2Ag↓ +3 NH3 ↑+ H2 O 4 CH 3COH +Ag 2O +NH 3 → CH 3COONH 4+2Ag↓ 5 CH3 COH+ 2Cu(OH) 2→ CH3 COOH +Cu 2O↓+ 2H 2O 6 C6 H 12O6 + 2Сu( OH) 2 → CH2 OH-(CHOH) 4-COOH +Cu 2O↓+ 2 H 2O 7 C6 H12 O6 +2{ Ag(NH3 ) 2} OH → CH 2OH –(CHOH) 4-COOH+2Ag↓ + 2 H 2O 8 2 C3 H8 O3 + Cu(OH) 2→ Глицерат меди II+ 2H 2O 9 HCOOH+ 2 {Ag(N H3 ) 2} OH → CO 2+2Ag+ 4NH3 + 2H 2O
Слайд 7Условия протекания реакций
3.
С Н
2
5
ОН
2
425
о
ZnO

CH CH CH CH
2
2
+
H O
2
(реакция Лебедева)
2
+
H
2
5.
+
CuO
CH
3
C
O
H
+
H O
2
+
Cu
1.
+
180
о
H O
2
CH CH
2
2
Слайд 87.
+
Cl
2
FeCl
3
Cl
+
HCl
10.
СH2 CHBr
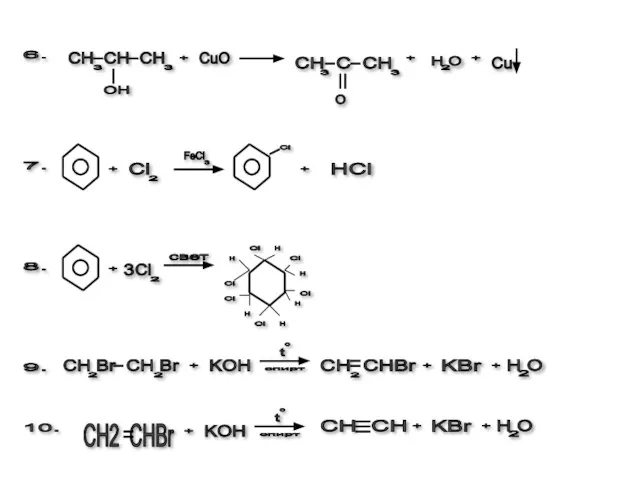
+
KOH
спирт
t
о
СH CH
+
KBr
+
9.
СH Br CH Br
2
2
+
KOH
спирт
t
о
СH CHBr
+
KBr
+
2
8.
+
Cl
2
3
свет
Cl
Cl
Cl
Cl
Cl
Cl
H
H
H
H
H
H
6.
СH CH CH
3
3
ОН
+
CuO
СH C CH
O
3
3
+
H O
2
+
Cu
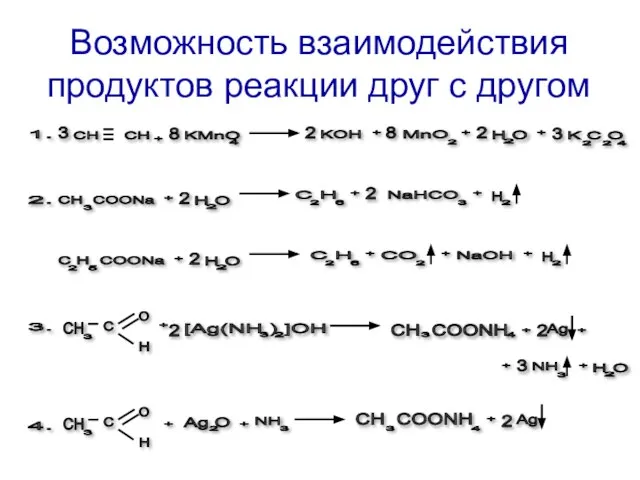
Слайд 9Возможность взаимодействия продуктов реакции друг с другом
1.
3
+
NH
2
3
KMnO
4
KOH
2
+
MnO
2
8
+
2
+
2.
СH COONa
+
2
C H
6
+
NaHCO
3
+
H
2
2
С H COONa
2
5
+
2
2
C H
6
+
CO
2
+
NaOH
+
H
2
3.
CH
3
C
O
H
+
[Ag(NH ) ]OH
3
2
СH COONH
3
4
+
Ag
4.
CH
3
C
O
H
+
Ag O
2
+
3
СH COONH
3
4
+
Ag
K C O
3
2
2
4
СH CH
8
2
2
NH
3
+
3
+
+
2
Слайд 10Цепочки превращений с различным объёмом информации о веществах
Открытая
Полуоткрытая
Полузакрытая
Закрытая
Сверхзакрытая
A
Б
В
+Г
A

В
...
...
...
+Б
A
...
...
Г
+Б
-В
A
+В
-Д
+Г
...
...
...
+В
...
-Б
+А
...
Слайд 11Демонстрационный материал ЕГЭ 2010
2
C H
4
2
C H
4
Сl
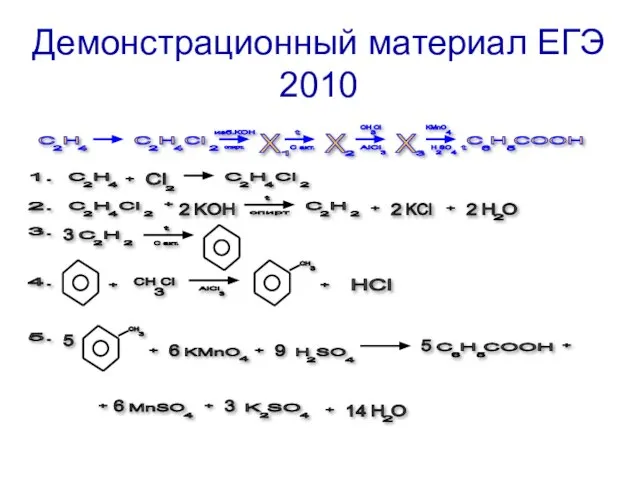
2
X
X
X
2
1
3
C H COOH
6
5
KOH
спирт.
t
изб.
С акт.
t
Слайд 12Тренировочный материал ЕГЭ 2010
CH
4
X
X
2
1
кат.
t
HCHO

Слайд 13
C2H2 →X1 → X2 → C6H5OK → X3→ X4
3 C2H2 → C6H6
C6H6
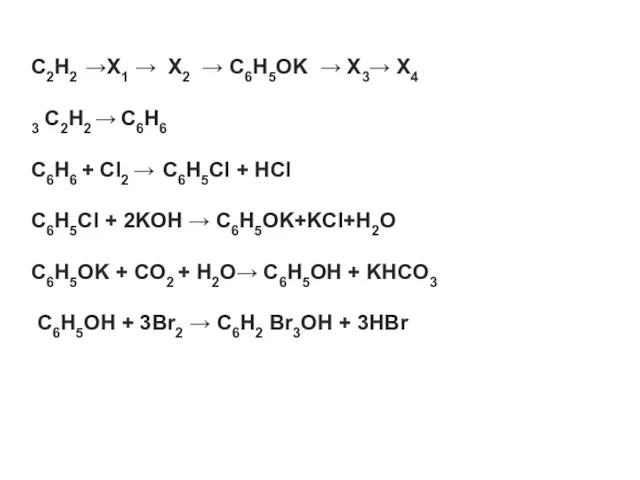
+ Cl2 → C6H5Cl + HCl
C6H5Cl + 2KOH → C6H5OK+KCl+H2O
C6H5OK + CO2 + H2O→ C6H5OH + KHCO3
C6H5OH + 3Br2 → C6H2 Br3OH + 3HBr
Слайд 14
C6H12O6 → X →этилацетат → X→ C2H5-O-C3H7
C6H12O6 → 2 C2H5OH +
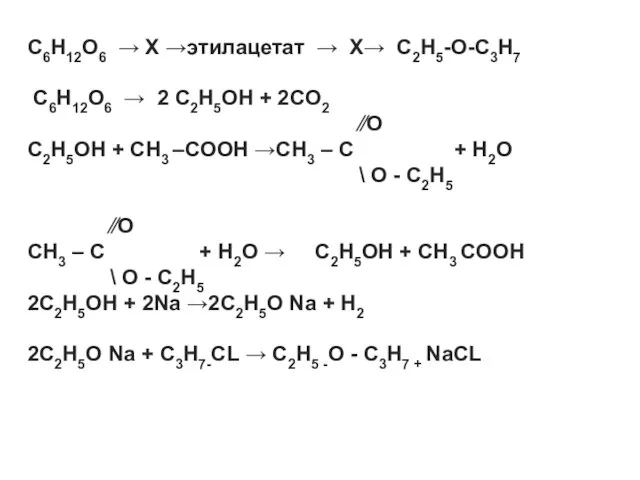
2CO2
⁄⁄O
C2H5OH + CH3 –COOH →CH3 – C + H2O
\ O - C2H5
⁄⁄O
CH3 – C + H2O → C2H5OH + CH3 COOH
\ O - C2H5
2C2H5OH + 2Na →2C2H5O Na + H2
2C2H5O Na + C3H7-CL → C2H5 -O - C3H7 + NaCL
Слайд 15
C2H6 → X1 → X2 → X3 → X2 → X4
C2H6
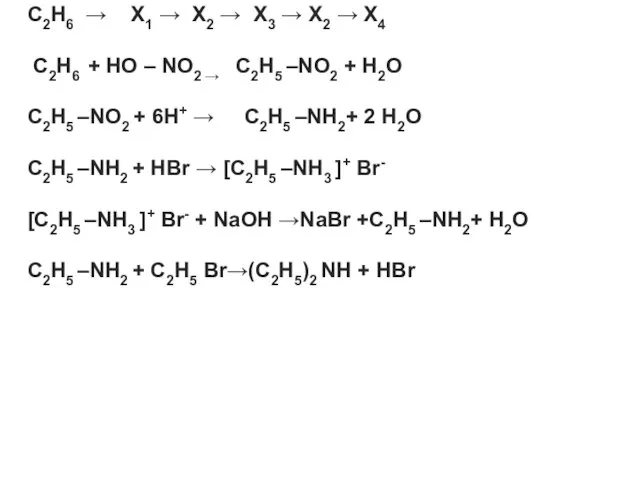
+ HO – NO2 → C2H5 –NO2 + H2O
C2H5 –NO2 + 6H+ → C2H5 –NH2+ 2 H2O
C2H5 –NH2 + HBr → [C2H5 –NH3 ]+ Br-
[C2H5 –NH3 ]+ Br- + NaOH →NaBr +C2H5 –NH2+ H2O
C2H5 –NH2 + C2H5 Br→(C2H5)2 NH + HBr
Слайд 16
пропанол-2 →X1 → X2 →пропин→ X3→ пропанол-2
CH3 - CH2 - CH2 -OH→
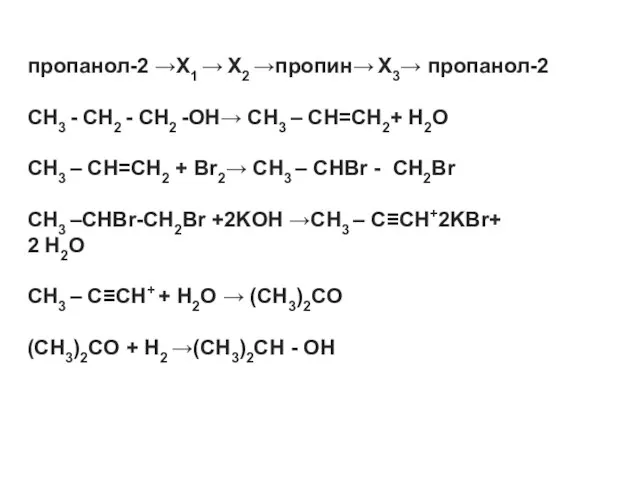
CH3 – CH=CH2+ H2O
CH3 – CH=CH2 + Br2→ CH3 – CHBr - CH2Br
CH3 –CHBr-CH2Br +2KOH →CH3 – C≡CH+2KBr+
2 H2O
CH3 – C≡CH+ + H2O → (CH3)2CO
(CH3)2CO + H2 →(CH3)2CH - OH
Слайд 17
пропанол-1 →X1 → X2 →Х3→ ацетон→ пропанол-2
CH3 - CH2 - CH2 -OH→
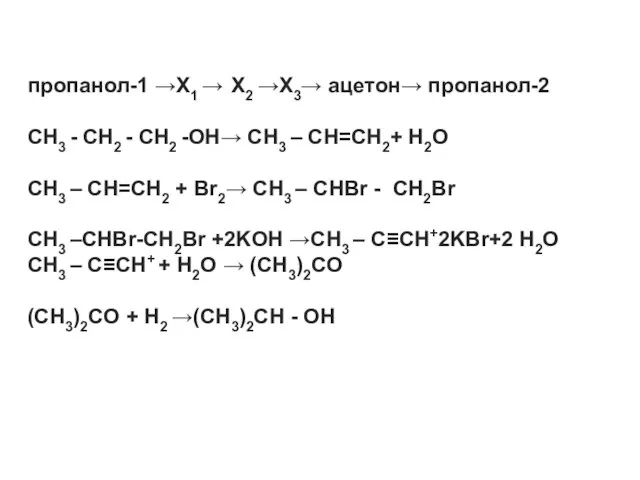
CH3 – CH=CH2+ H2O
CH3 – CH=CH2 + Br2→ CH3 – CHBr - CH2Br
CН3 –CHBr-CH2Br +2KOH →CH3 – C≡CH+2KBr+2 H2O
CH3 – C≡CH+ + H2O → (CH3)2CO
(CH3)2CO + H2 →(CH3)2CH - OH
Слайд 18CaCO3 →CaC2→X1→C2Ag2→ X1→ винилацетилен
CaCO3+ 4С →CaC2 + 3СО
C2H2 + 2[Ag (NH3)2]OH→ AgC≡CAg

+ 4NH3+2H2O
AgC≡CAg +2HCl → C2H2+ 2AgCl↓
2 C2H2→ H2C = CH – C ≡ CH
Слайд 19
Этанол →X1 → X2 → Ag2C2 → X2 → X3
C2H5OH →
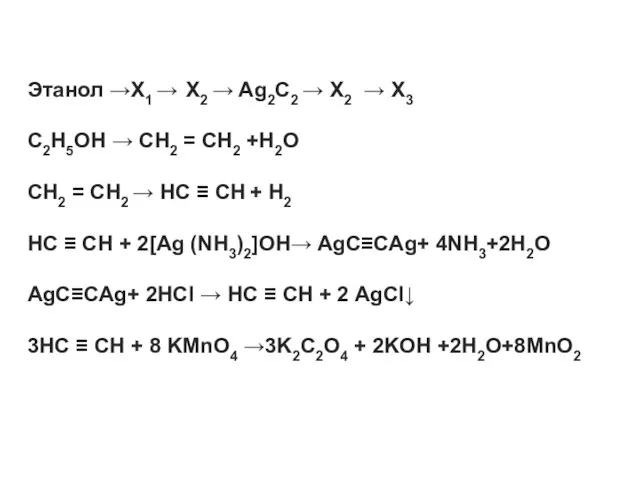
CH2 = CH2 +H2O
CH2 = CH2 → HC ≡ CH + H2
HC ≡ CH + 2[Ag (NH3)2]OH→ AgC≡CAg+ 4NH3+2H2O
AgC≡CAg+ 2HCl → HC ≡ CH + 2 AgCl↓
3HC ≡ CH + 8 KMnO4 →3K2C2O4 + 2KOH +2H2O+8MnO2


















 Послание дружбы детям стран СНГ
Послание дружбы детям стран СНГ Магистерская программа Ядерная медицина
Магистерская программа Ядерная медицина 10б
10б Презентация на тему Прямая пропорциональность (7 класс)
Презентация на тему Прямая пропорциональность (7 класс) www.spbmapo.ru
www.spbmapo.ru Презентация на тему Первая печатная книга на Руси
Презентация на тему Первая печатная книга на Руси  Острая сердечная недостаточность
Острая сердечная недостаточность «Приведение ЛВС ОУ в соответствие с правилами устройства электроустановок»
«Приведение ЛВС ОУ в соответствие с правилами устройства электроустановок» Мои достижения
Мои достижения Презентация на тему Теоремы синусов и косинусов 9 КЛАСС
Презентация на тему Теоремы синусов и косинусов 9 КЛАСС Источник взывающего, церковь Дизайн Христа
Источник взывающего, церковь Дизайн Христа Презентация на тему Welcome to Australia
Презентация на тему Welcome to Australia  Русский язык на международной арене
Русский язык на международной арене  Презентация на тему "Що можна робити в бібліотеці?" - скачать презентации по Педагогике
Презентация на тему "Що можна робити в бібліотеці?" - скачать презентации по Педагогике Николай Михайлович Ромадин (1903–1987)
Николай Михайлович Ромадин (1903–1987) Разрезы. Соединение на чертеже вида и разреза особые случаи применения
Разрезы. Соединение на чертеже вида и разреза особые случаи применения Презентация на тему Жизнь и творчество Марка Твена
Презентация на тему Жизнь и творчество Марка Твена Агния Львовна Барто
Агния Львовна Барто Образы борьбы и победы в искусстве Задачи урока: Раскрыть образный строй одной из самых знаменитых симфоний – Симфонии №5 Людви
Образы борьбы и победы в искусстве Задачи урока: Раскрыть образный строй одной из самых знаменитых симфоний – Симфонии №5 Людви Роза из салфетки к праздничному столу
Роза из салфетки к праздничному столу с
с Стыд, вина и извинение
Стыд, вина и извинение Фитнес. Тренировочные принципы
Фитнес. Тренировочные принципы Актаныш
Актаныш Презентация на тему Евпатий Коловрат
Презентация на тему Евпатий Коловрат  С днём рождения !!!
С днём рождения !!! Форматирование текстового документа
Форматирование текстового документа Презентация к уроку алгебры в 10 классе _Определение синуса, косинуса и тангенса угла_
Презентация к уроку алгебры в 10 классе _Определение синуса, косинуса и тангенса угла_