Содержание
- 2. Примеры применение метода химической модификации белков Отслеживание in vivo конъюгатов белков с флуорофорами Пегилирование белков с
- 3. Методы обнаружения «существенных» и «избыточных» а.о. 1. Направленный (сайт-специфический) мутагенез. 2. Химическая модификация боковых групп а.о.
- 4. Типы химических модификаций 1. Модификация отдельных а.о. с помощью селективных химических реагентов. 2. Модификация двух функциональных
- 5. Особенности химической модификации белков Химические свойства идентичных функциональных групп в аминокислотах и в белках различаются по
- 6. Условия среды для химических модификаций природных белков pH 6-8 реакция в водном растворе
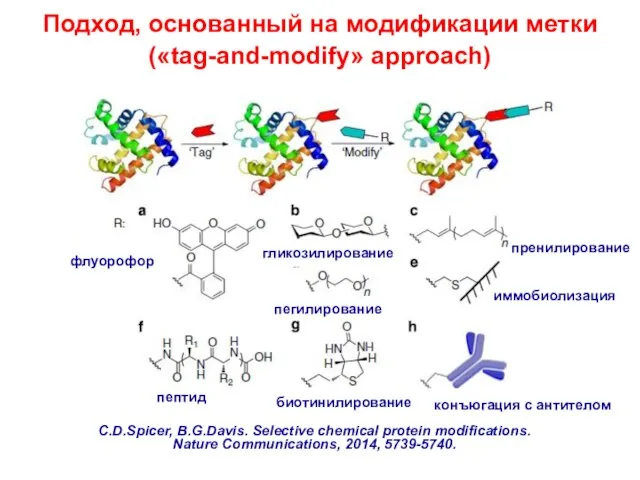
- 7. Подход, основанный на модификации метки («tag-and-modify» approach) C.D.Spicer, B.G.Davis. Selective chemical protein modifications. Nature Communications, 2014,
- 8. Функциональные группы белков, которые могут быть модифицированы 1. α-NH2 –группа и ε-NH2-группа остатков Lys. 2. Вторичная
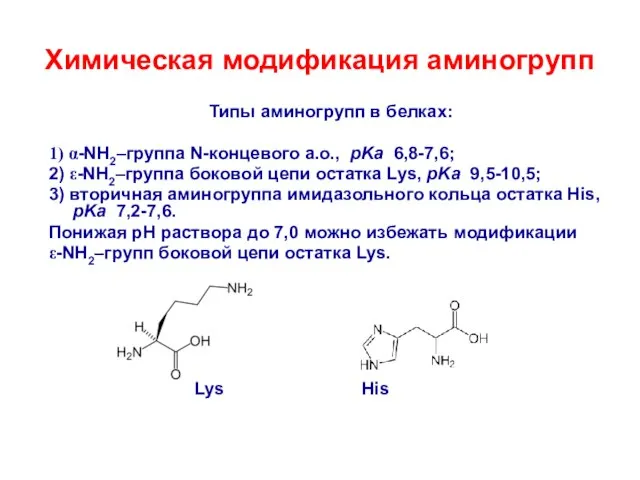
- 9. Химическая модификация аминогрупп Типы аминогрупп в белках: 1) α-NH2–группа N-концевого а.о., pKa 6,8-7,6; 2) ε-NH2–группа боковой
- 10. ε-NH2–группа боковой цепи остатка Lys может быть модифицирована следующими методами: 1) ацилирование; 2) арилирование; 3) реакция
- 11. Ацилирование ε-NH2–группы Lys Ацилирование можно вести с помощью: 1) симметричных ангидридов (уксусного, трифторуксусного, янтарного, малеинового, цитраконового);
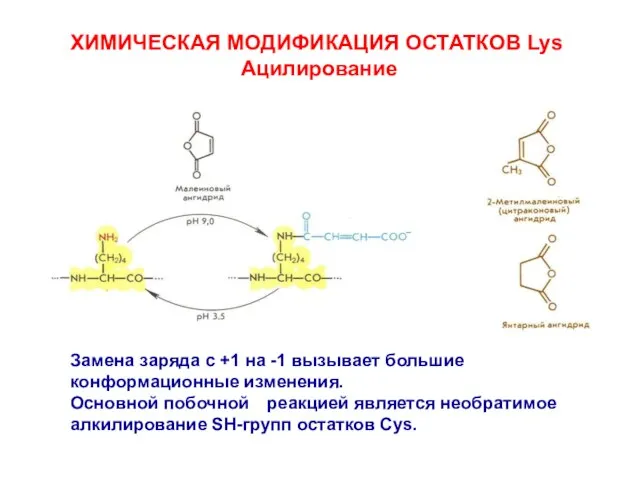
- 12. ХИМИЧЕСКАЯ МОДИФИКАЦИЯ ОСТАТКОВ Lys Ацилирование Замена заряда с +1 на -1 вызывает большие конформационные изменения. Основной
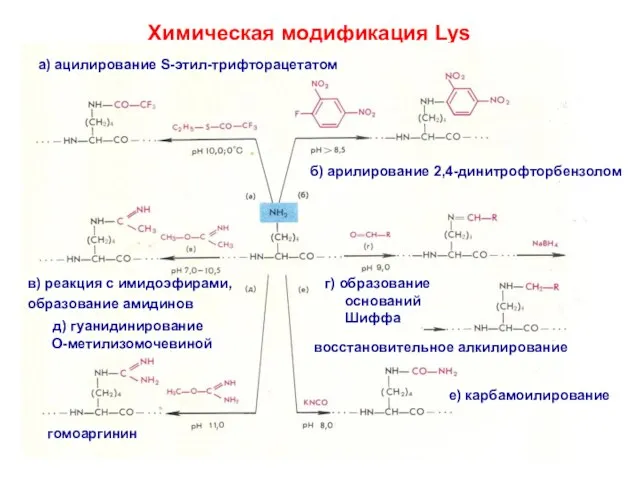
- 13. Химическая модификация Lys а) ацилирование S-этил-трифторацетатом д) гуанидинирование О-метилизомочевиной б) арилирование 2,4-динитрофторбензолом в) реакция с имидоэфирами,
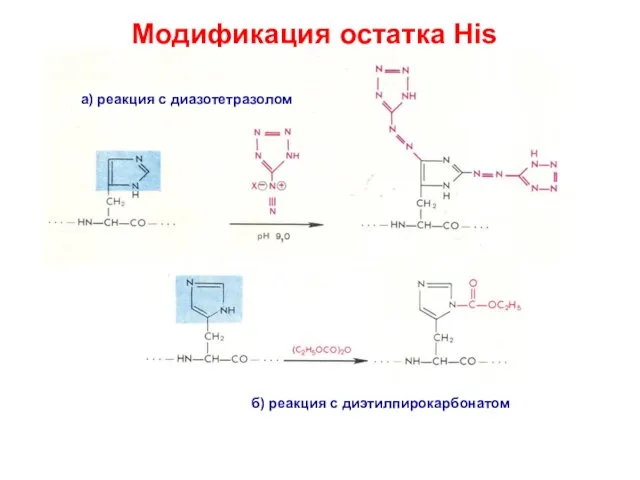
- 14. Модификация остатка His а) реакция с диазотетразолом б) реакция с диэтилпирокарбонатом
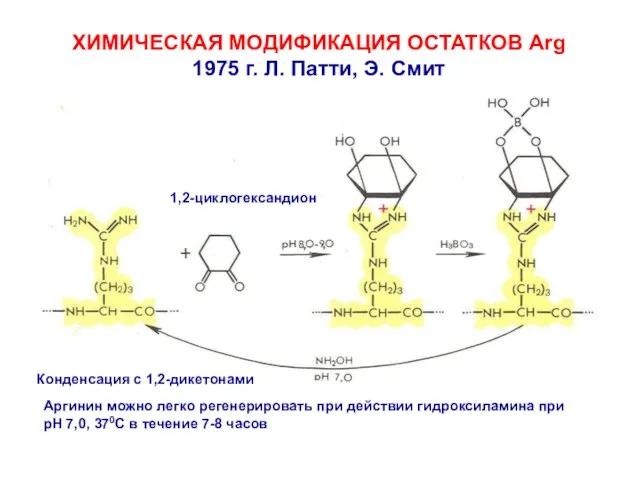
- 15. ХИМИЧЕСКАЯ МОДИФИКАЦИЯ ОСТАТКОВ Arg 1975 г. Л. Патти, Э. Смит Конденсация с 1,2-дикетонами 1,2-циклогександион Аргинин можно
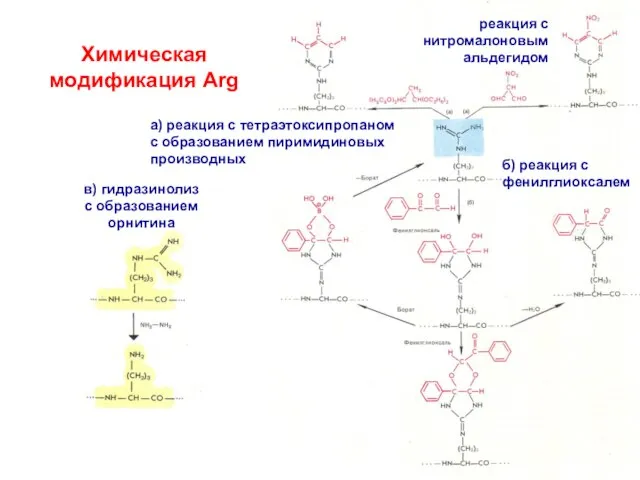
- 16. Химическая модификация Arg реакция с нитромалоновым альдегидом а) реакция с тетраэтоксипропаном с образованием пиримидиновых производных б)
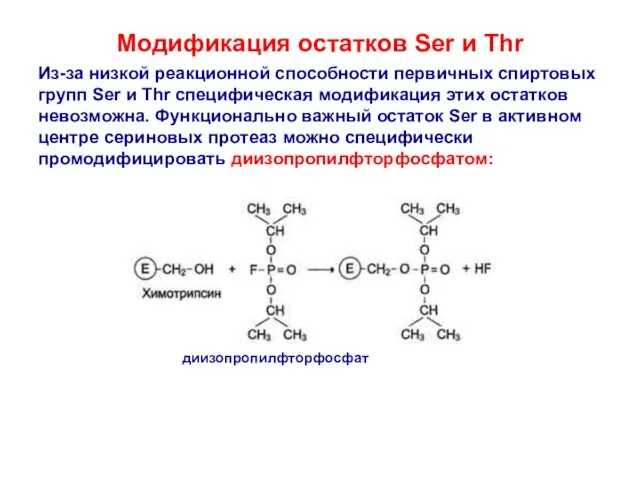
- 17. Модификация остатков Ser и Thr Из-за низкой реакционной способности первичных спиртовых групп Ser и Thr специфическая
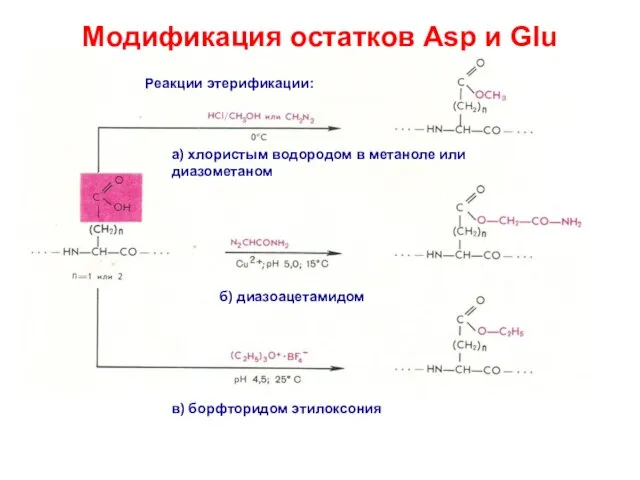
- 18. Модификация остатков Asp и Glu Реакции этерификации: б) диазоацетамидом а) хлористым водородом в метаноле или диазометаном
- 19. Модификация остатка Met Алкилирование иодацетамидом с образованием карбоксиметилсульфониевой соли
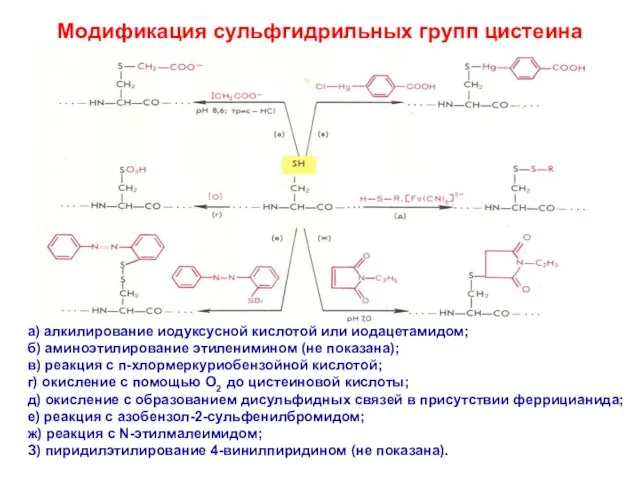
- 20. Модификация сульфгидрильных групп цистеина а) алкилирование иодуксусной кислотой или иодацетамидом; б) аминоэтилирование этиленимином (не показана); в)
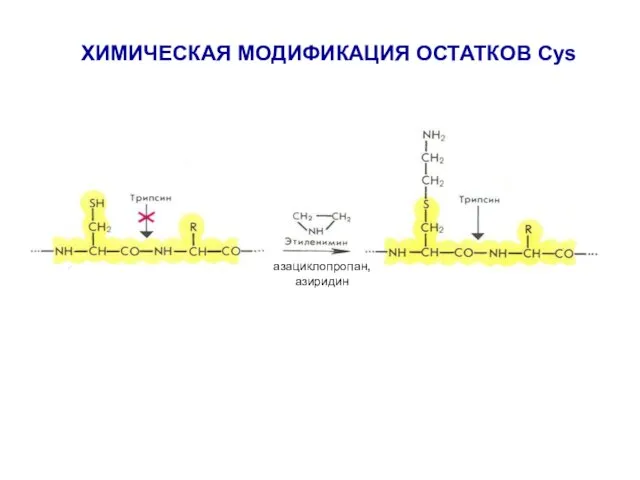
- 21. ХИМИЧЕСКАЯ МОДИФИКАЦИЯ ОСТАТКОВ Cys азациклопропан, азиридин
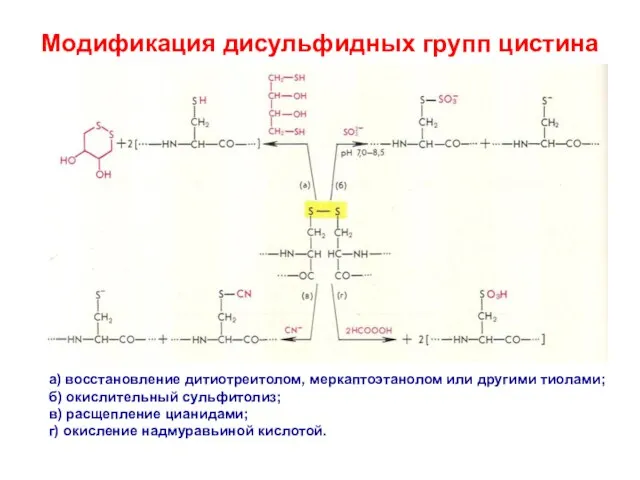
- 22. Модификация дисульфидных групп цистина а) восстановление дитиотреитолом, меркаптоэтанолом или другими тиолами; б) окислительный сульфитолиз; в) расщепление
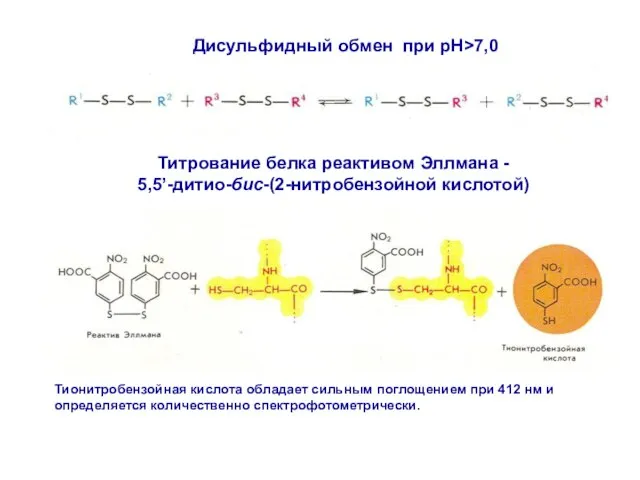
- 23. Титрование белка реактивом Эллмана - 5,5’-дитио-бис-(2-нитробензойной кислотой) Дисульфидный обмен при pH>7,0 Тионитробензойная кислота обладает сильным поглощением
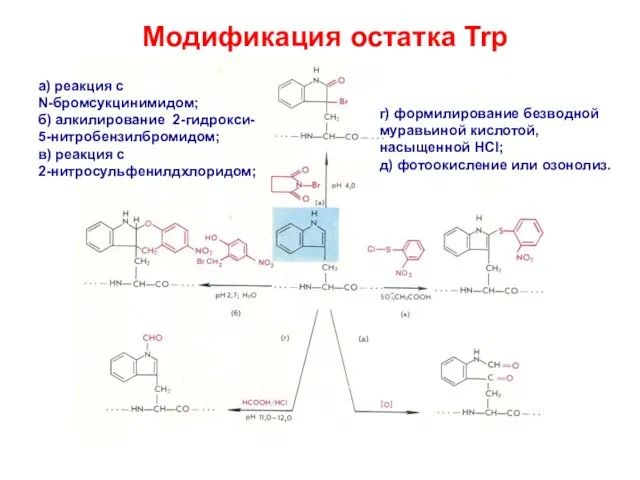
- 24. Модификация остатка Trp а) реакция с N-бромсукцинимидом; б) алкилирование 2-гидрокси- 5-нитробензилбромидом; в) реакция с 2-нитросульфенилдхлоридом; г)
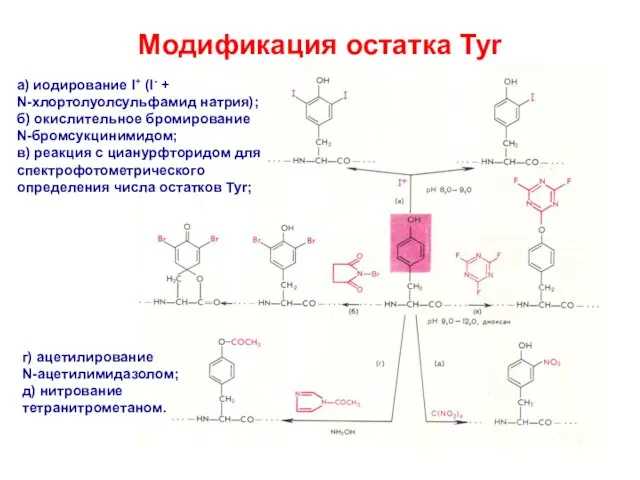
- 25. Модификация остатка Tyr а) иодирование I+ (I- + N-хлортолуолсульфамид натрия); б) окислительное бромирование N-бромсукцинимидом; в) реакция
- 26. Кросс-сшивающие или бифункциональные реагенты Кросс-сшивающими или бифункциональынми реагентами называются соединения с двумя реакционноспособными группами. Общая формула
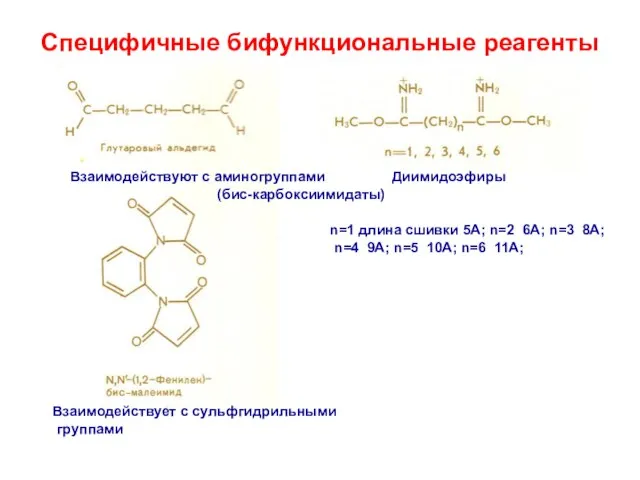
- 27. Специфичные бифункциональные реагенты n=1 длина сшивки 5A; n=2 6A; n=3 8A; n=4 9A; n=5 10A; n=6
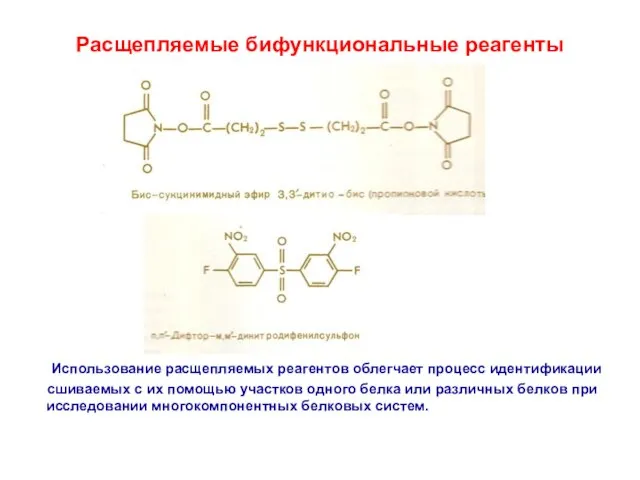
- 28. Расщепляемые бифункциональные реагенты Использование расщепляемых реагентов облегчает процесс идентификации сшиваемых с их помощью участков одного белка
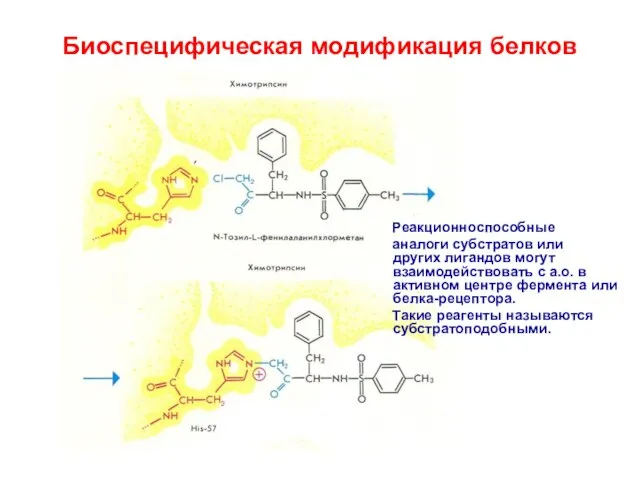
- 29. Биоспецифическая модификация белков Реакционноспособные аналоги субстратов или других лигандов могут взаимодействовать с а.о. в активном центре
- 31. Скачать презентацию










 Аминокислоты. История их открытия
Аминокислоты. История их открытия Презентация на тему Слова-паразиты в речи
Презентация на тему Слова-паразиты в речи  Земноводные и пресмыкающиеся
Земноводные и пресмыкающиеся Презентация на тему Ильменский заповедник
Презентация на тему Ильменский заповедник  Что есть стилистика?
Что есть стилистика? Поп-арт, стрит-арт
Поп-арт, стрит-арт Виды изобразительного искусства
Виды изобразительного искусства Экономика ХХІ
Экономика ХХІ Николай Корнильевич Пимоненко
Николай Корнильевич Пимоненко Презентация на тему Особенности питания и пищеварения у животных
Презентация на тему Особенности питания и пищеварения у животных Исполнение бюджета города Райчихинска за 2011 год
Исполнение бюджета города Райчихинска за 2011 год Mein Traumhaus
Mein Traumhaus Orbiz_Krash-test__initsiativnaya__Osen_2022
Orbiz_Krash-test__initsiativnaya__Osen_2022 Органы очистки организма
Органы очистки организма Старинные танцы
Старинные танцы История и традиции православной Пасхи
История и традиции православной Пасхи Аномальные зоны России
Аномальные зоны России Презента
Презента Анмимация античного храма
Анмимация античного храма Реорганизация помещения 215
Реорганизация помещения 215 Добро пожаловать!
Добро пожаловать! ВОЛЕЙБОЛ
ВОЛЕЙБОЛ Способы воздействия в межличностной коммуникации
Способы воздействия в межличностной коммуникации Тихий океан
Тихий океан Метод проектов
Метод проектов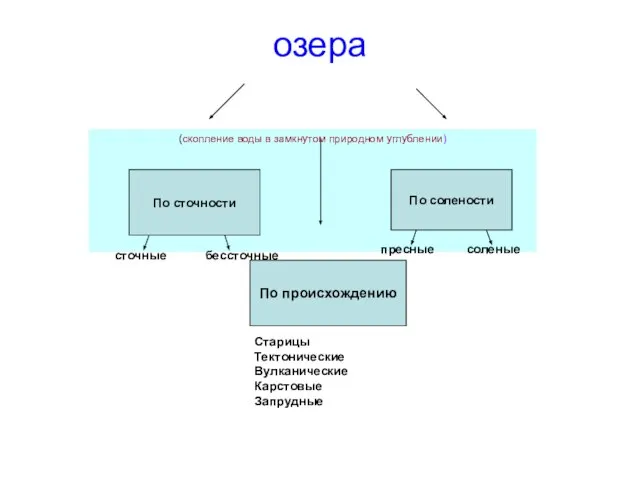 озера
озера Технология изготовления изделий с использованием сложных соединений. Шиповые соединения
Технология изготовления изделий с использованием сложных соединений. Шиповые соединения Порядок приемки объектов озеленения
Порядок приемки объектов озеленения