Содержание
- 2. Белки – основа всего живого Все живые организмы, как животные, так и растительные, содержат белки, которые
- 3. Все белки состоят из аминокислот, которые соединяются в пептидную связь. Пептидной связью называется связь, образующаяся между
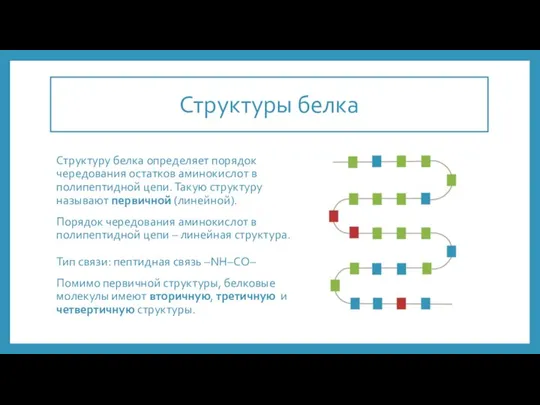
- 4. Структуры белка Структуру белка определяет порядок чередования остатков аминокислот в полипептидной цепи. Такую структуру называют первичной
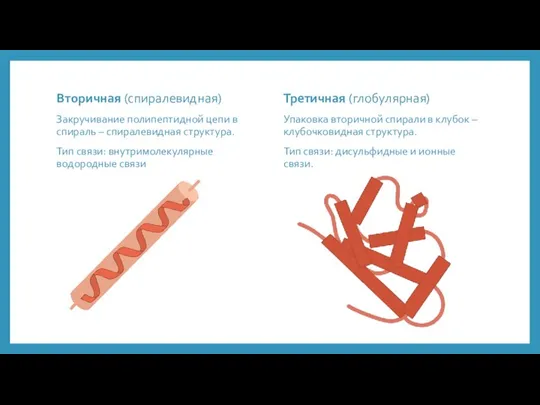
- 5. Вторичная (спиралевидная) Закручивание полипептидной цепи в спираль – спиралевидная структура. Тип связи: внутримолекулярные водородные связи Третичная
- 6. Четвертичная Взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. В состав белка с четвертичной
- 7. Большая заслуга в расшифровке структур белковых молекул принадлежит немецкому химику-органику Э. Г. Фишеру и русскому биохимику
- 8. Химические свойства При нагревании, под действием сильных кислот или оснований, солей тяжелых металлов и некоторых других
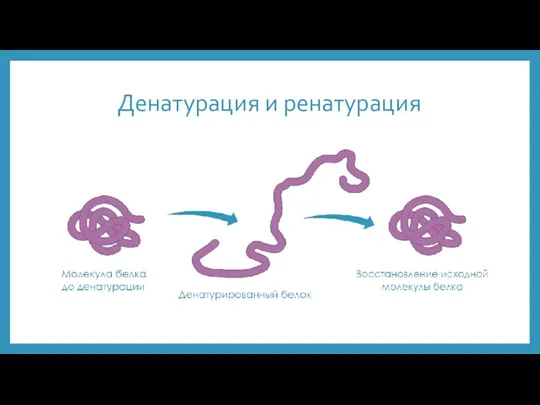
- 9. Денатурация и ренатурация
- 10. Гидролиз Большинство белков свертывается при температуре до 100°с. Именно поэтому все живое гибнет в огне, практически
- 11. Качественные реакции Белки дают две качественные реакции. Биуретовая реакция. При действии на белки свежеполученного осадка гидроксида
- 12. Функции белков Ферментативная функция. Большинство химических реакций в организме протекают в присутствии биологических катализаторов – ферментов,
- 13. Структурная функция. Белки – это строительный материал почти всех тканей: мышечных, опорных, покровных. Защитная функция. Особые
- 15. Скачать презентацию









 Домашние животные. Виды
Домашние животные. Виды Меры безопасности при столкновении с борщевиком Сосновского
Меры безопасности при столкновении с борщевиком Сосновского Biologie ist die wissenschaft von den lebewesen
Biologie ist die wissenschaft von den lebewesen Осенние цветы
Осенние цветы Питание и обмен веществ у микроорганизмов (тема 4)
Питание и обмен веществ у микроорганизмов (тема 4) Сукцессия. Саморазвитие экосистемы
Сукцессия. Саморазвитие экосистемы Лейкоцитарная формула
Лейкоцитарная формула Строение и принцип работы нервной системы
Строение и принцип работы нервной системы Фізіологія ВНД
Фізіологія ВНД Сравнение процесса деления митоза и мейоза и их биологическое значение
Сравнение процесса деления митоза и мейоза и их биологическое значение Плесневые грибы и дрожжи
Плесневые грибы и дрожжи Лисица
Лисица В гостях у бабушки травницы
В гостях у бабушки травницы Клеточная теория
Клеточная теория Діабет. Основними симптомами діабету будь-якого типу
Діабет. Основними симптомами діабету будь-якого типу Классификация бактерий по Берджи. Принцип подразделения бактерий на группы. Микоплазмы. Хламидии. Риккетсии
Классификация бактерий по Берджи. Принцип подразделения бактерий на группы. Микоплазмы. Хламидии. Риккетсии Сцепление генов. Хромосомная теория наследственности. Генетика пола. Сцепленное с полом наследование
Сцепление генов. Хромосомная теория наследственности. Генетика пола. Сцепленное с полом наследование Дыхательная система
Дыхательная система Немембранные органоиды
Немембранные органоиды Открытие ученых России - живые растения, постоянно светящиеся в темноте
Открытие ученых России - живые растения, постоянно светящиеся в темноте Ткани, органы, аппараты и системы органов. Периоды онтогенеза у животных и растений
Ткани, органы, аппараты и системы органов. Периоды онтогенеза у животных и растений Плазмоліз і деплазмоліз
Плазмоліз і деплазмоліз Калориметрические методы анализа биомолекул
Калориметрические методы анализа биомолекул Эволюционные учения
Эволюционные учения Презентация на тему Амурский тигр
Презентация на тему Амурский тигр  Городской парк
Городской парк Мутагенные факторы
Мутагенные факторы Что растёт на клумбе
Что растёт на клумбе