Содержание
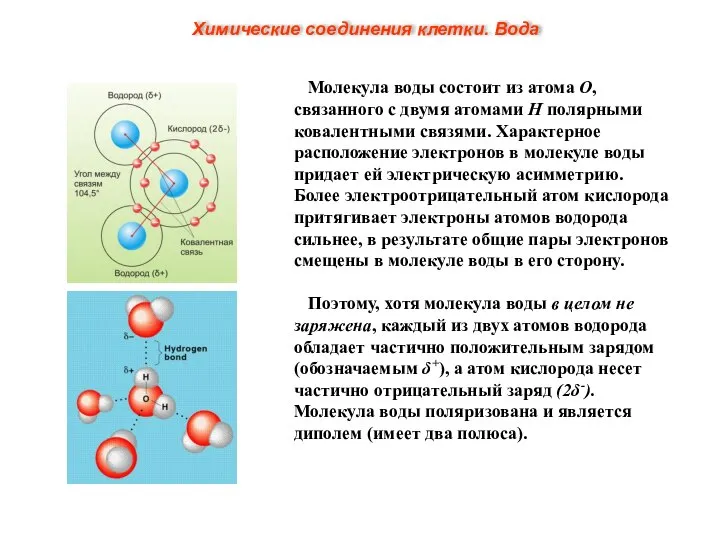
- 4. Молекула воды состоит из атома О, связанного с двумя атомами Н полярными ковалентными связями. Характерное расположение
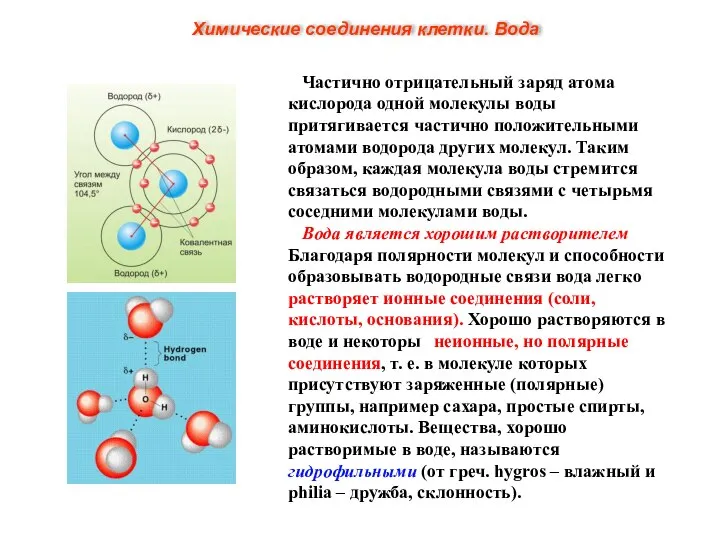
- 5. Полярные свойства воды:
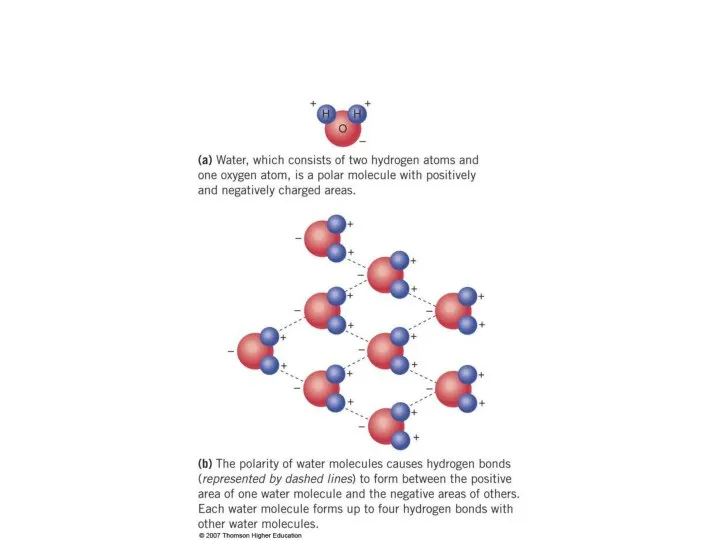
- 6. Частично отрицательный заряд атома кислорода одной молекулы воды притягивается частично положительными атомами водорода других молекул. Таким
- 7. Химические соединения клетки. Вода
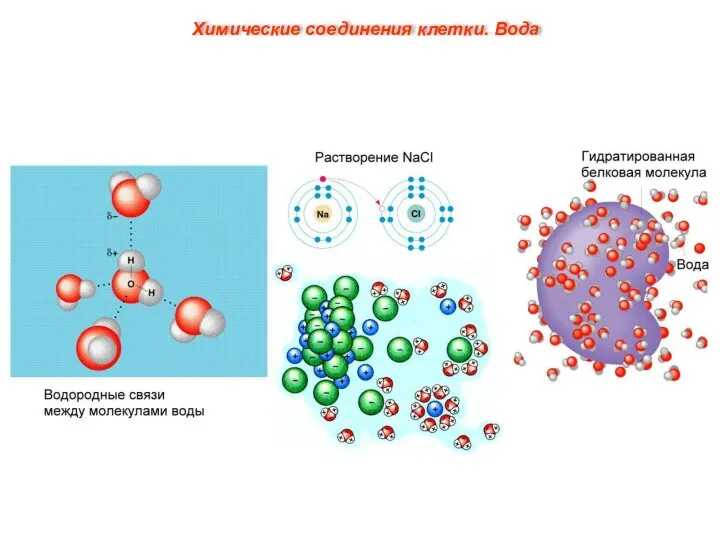
- 8. Вещества, плохо или вовсе нерастворимые в воде, называются гидрофобными (от греч. phobos – страх). К ним
- 9. Вода обладает высокой теплоемкостью, т. е. способностью поглощать тепловую энергию при минимальном повышении собственной температуры. Большая
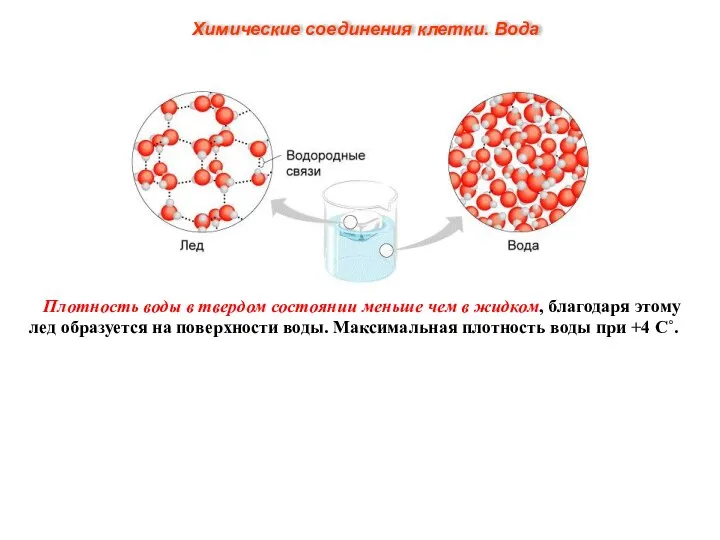
- 10. Плотность воды в твердом состоянии меньше чем в жидком, благодаря этому лед образуется на поверхности воды.
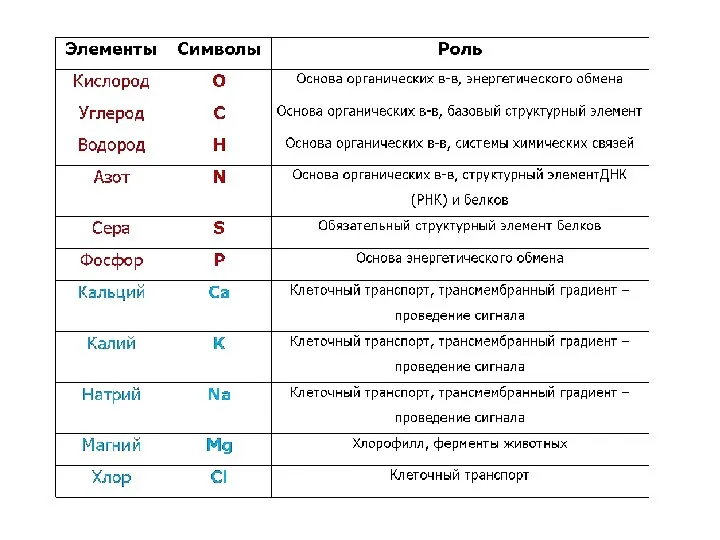
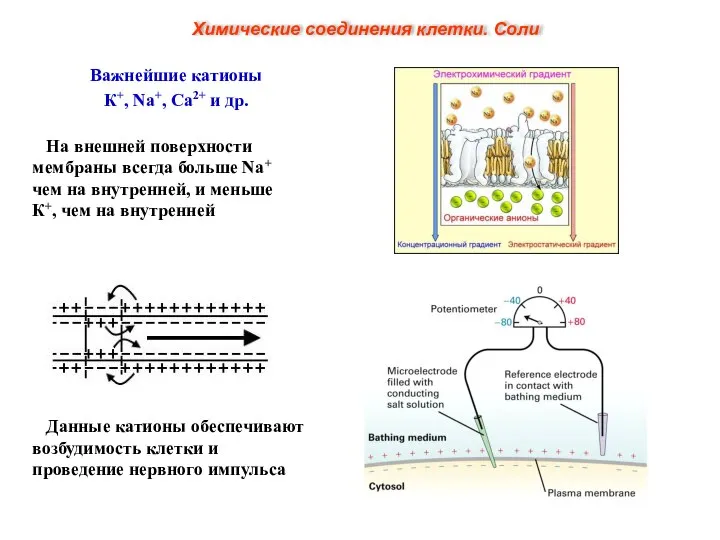
- 11. Важнейшие катионы К+, Na+, Ca2+ и др. Данные катионы обеспечивают возбудимость клетки и проведение нервного импульса.
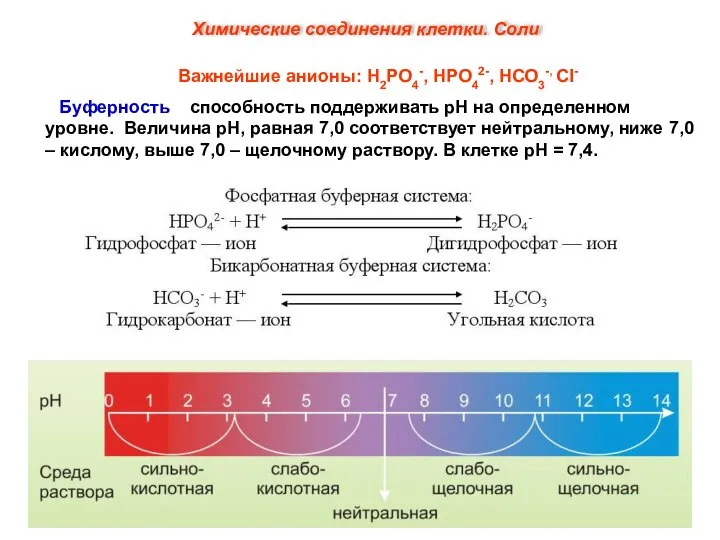
- 12. Важнейшие анионы: Н2РО4-, НРО42-, НСО3-, Сl- Буферность – способность поддерживать рН на определенном уровне. Величина рН,
- 13. Буферность клетки: способность поддерживать стабильный уровень рН несмотря на привнесение небольшого количества кислот или щелочей. Обычно
- 14. Органические вещества, входящие в состав клетки Chapter 2
- 15. Полимеры Полиме́ры - вещества, состоящие из «мономерных звеньев», соединённых в макромолекулы. Полимер — это высокомолекулярное соединение:
- 16. Углеводы Липиды Пептиды (в т.ч. Белки) Нуклеиновые кислоты
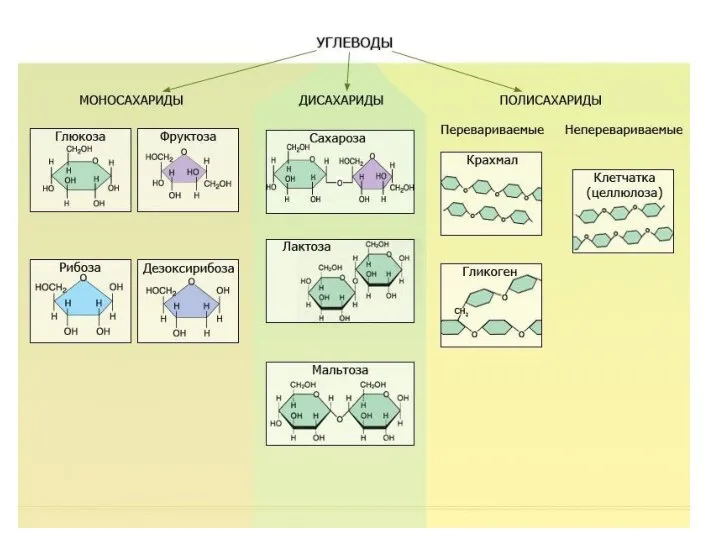
- 17. Углеводы Органические вещества, содержащие углерод, водород и кислород в примерном соотношении 1C:2H:1O Важный источник питательных веществ
- 18. Углеводы
- 19. Липиды Жироподобные органические вещества, не растворимые в воде. Важный источник энергии и способ запасать ее, компоненты
- 20. Основные типы липидов: Нейтральные жиры (жиры и масла - твердые и жидкие при комнатной температуре) Воски
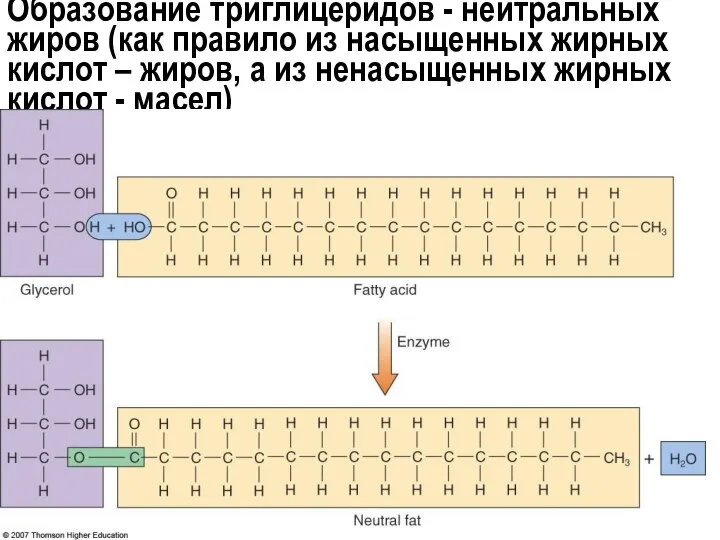
- 21. Образование триглицеридов - нейтральных жиров (как правило из насыщенных жирных кислот – жиров, а из ненасыщенных
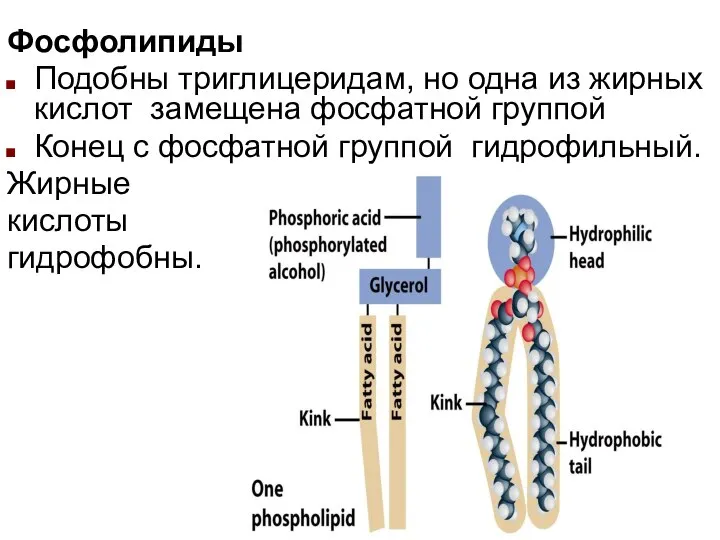
- 22. Фосфолипиды Подобны триглицеридам, но одна из жирных кислот замещена фосфатной группой Конец с фосфатной группой гидрофильный.
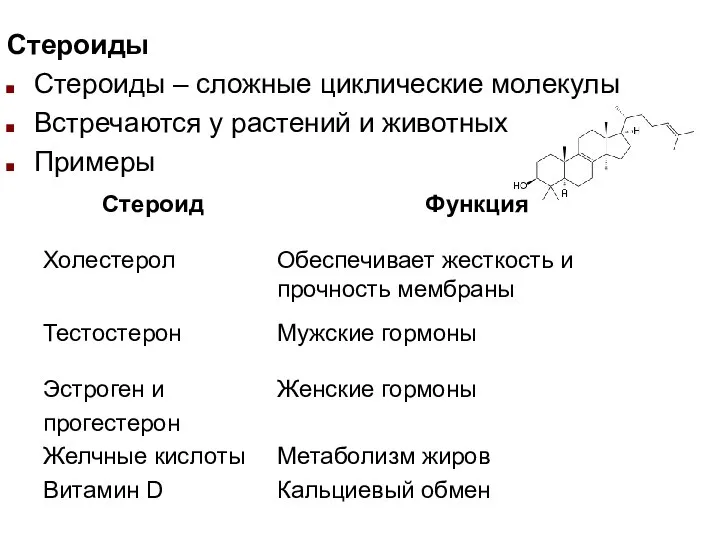
- 23. Стероиды Стероиды – сложные циклические молекулы Встречаются у растений и животных Примеры
- 24. Пептиды, в том числе Белки Высокомолекулярные органические соединения, состоящие из аминокислотных субъединиц Аминокислотные остатки соединены пептидными
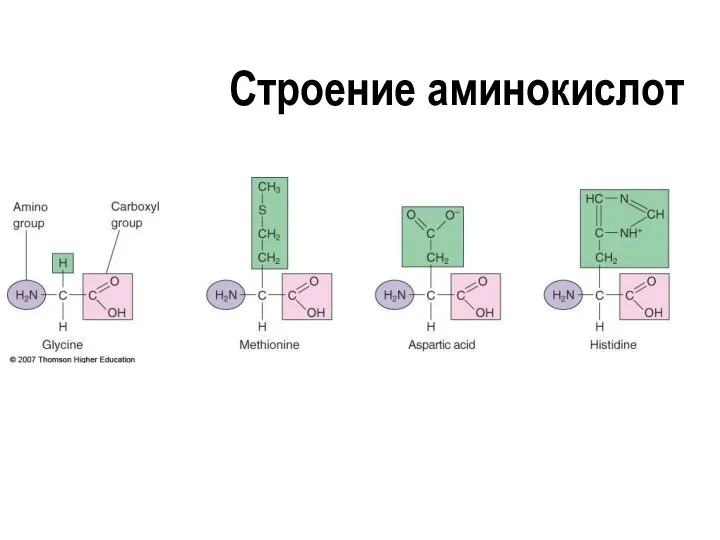
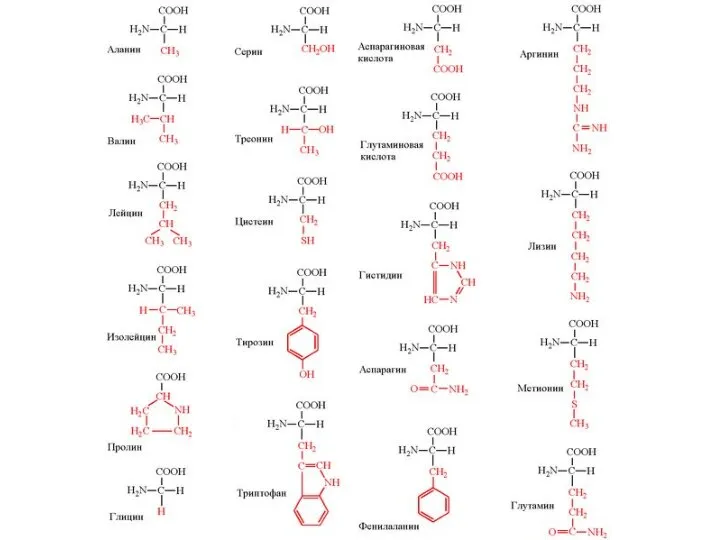
- 25. Строение аминокислот
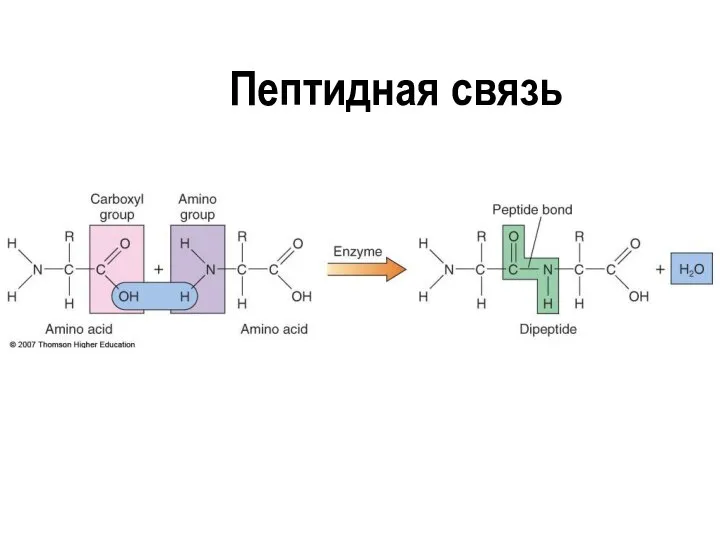
- 26. Пептидная связь
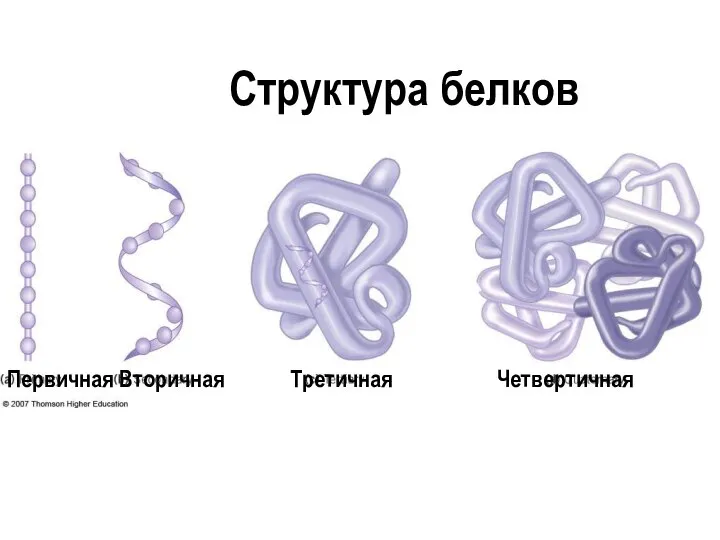
- 28. Структура белков Первичная Вторичная Третичная Четвертичная
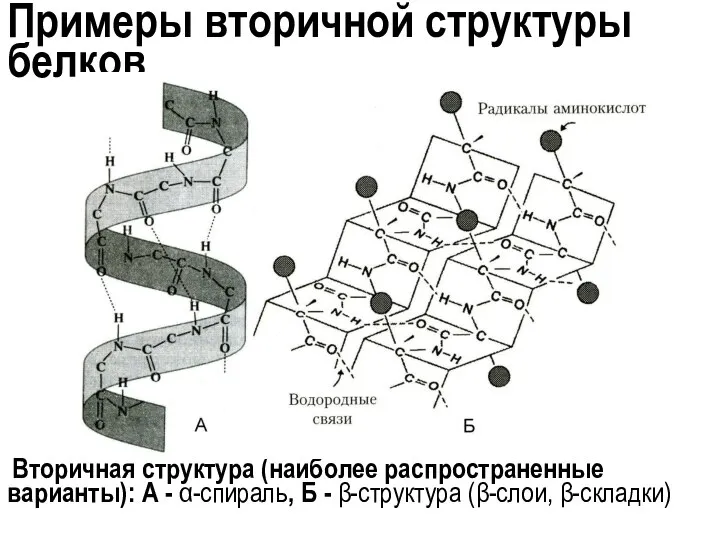
- 29. Примеры вторичной структуры белков Вторичная структура (наиболее распространенные варианты): А - α-спираль, Б - β-структура (β-слои,
- 30. Денатурация белка – разрушение пространственной структуры белка (четвертичной, третичной, вторичной) при внешнем воздействии (например повышении температуры,
- 31. Белки являются амфотерными соединениями, сочетают в себе основные и кислотные свойства, определяемые радикалами аминокислот. Различают кислые,
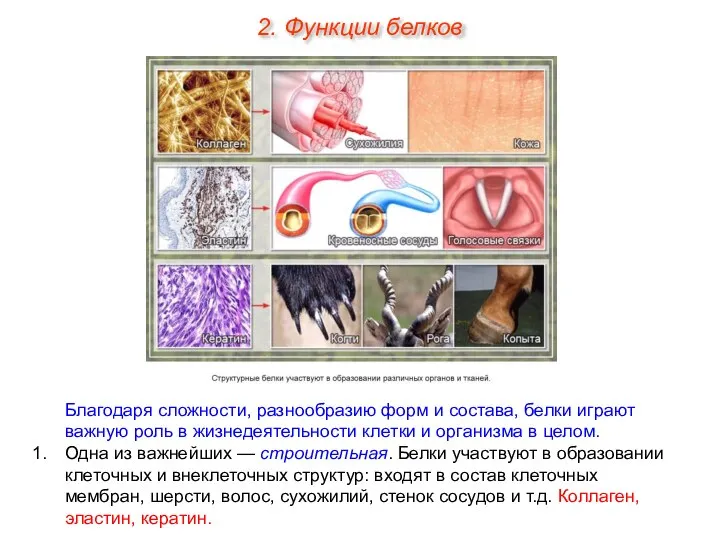
- 32. Благодаря сложности, разнообразию форм и состава, белки играют важную роль в жизнедеятельности клетки и организма в
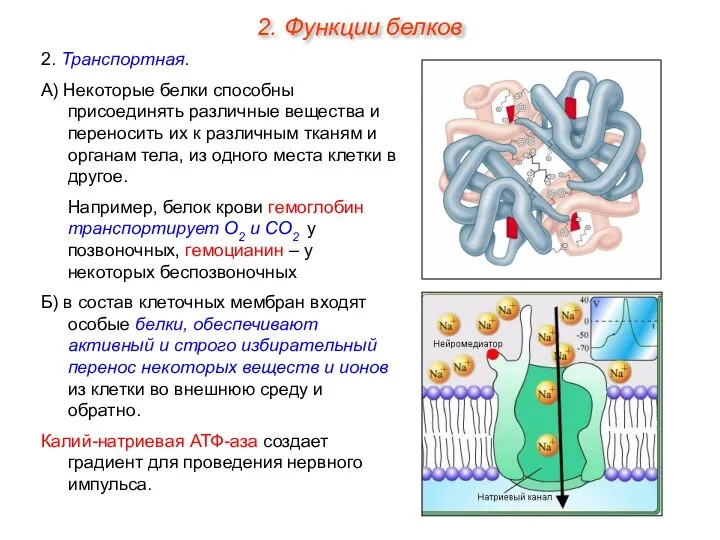
- 33. 2. Транспортная. А) Некоторые белки способны присоединять различные вещества и переносить их к различным тканям и
- 34. 3. Регуляторная. Большая группа белков организма принимает участие в регуляции процессов обмена веществ. Такими белками являются
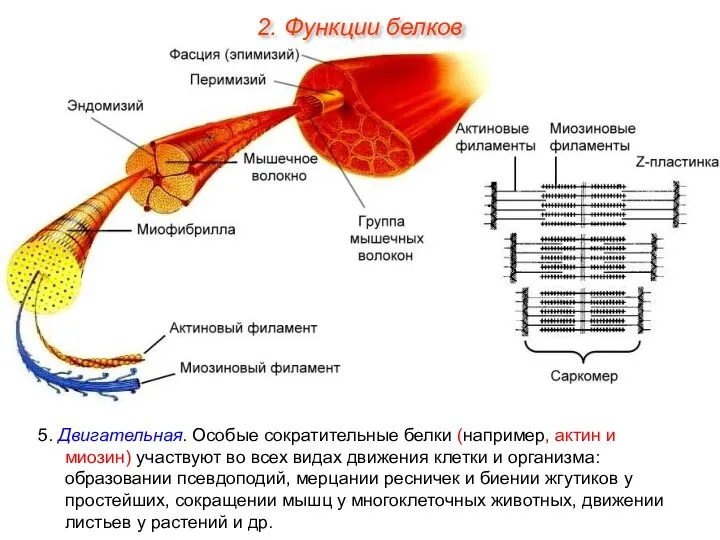
- 35. 5. Двигательная. Особые сократительные белки (например, актин и миозин) участвуют во всех видах движения клетки и
- 36. 6. Весьма важна для жизни клетки сигнальная и рецепторная функция белков. В поверхностную мембрану клетки встроены
- 37. 7. Запасающая. Благодаря белкам в организме могут откладываться про запас некоторые вещества. Например, при распаде гемоглобина
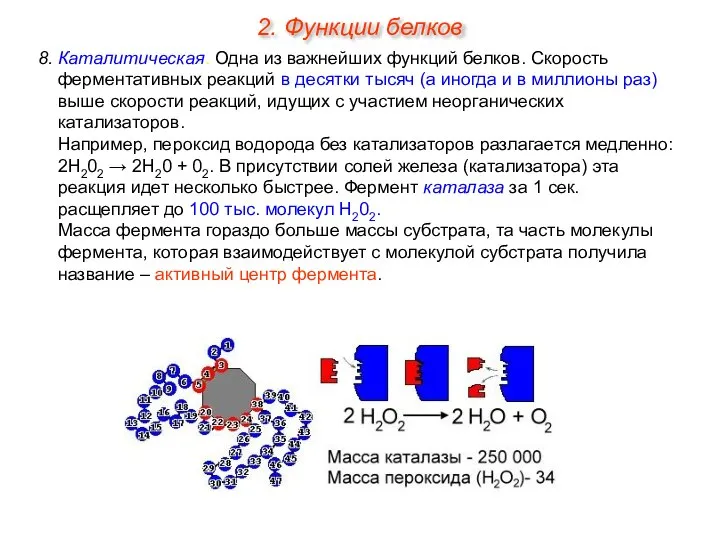
- 38. 8. Каталитическая. Одна из важнейших функций белков. Скорость ферментативных реакций в десятки тысяч (а иногда и
- 40. Скачать презентацию















 Весна идет
Весна идет Ткани растений
Ткани растений § 46. Значение, строение и функционирование нервной системы 8 класс биология
§ 46. Значение, строение и функционирование нервной системы 8 класс биология Введение в ангиологию. Микроциркуляторное русло
Введение в ангиологию. Микроциркуляторное русло 基因表达调控
基因表达调控 Механические ткани. Колленхима
Механические ткани. Колленхима Класс Насекомые
Класс Насекомые Презентация на тему Городские птицы
Презентация на тему Городские птицы  Царство растений
Царство растений Биологическое значение митоза и мейоза. Формы размножения животных
Биологическое значение митоза и мейоза. Формы размножения животных Мы живём среди людей
Мы живём среди людей Минеральное питание растений
Минеральное питание растений Птицы России
Птицы России Эволюция. Антропогенез
Эволюция. Антропогенез Лизосомы. Типы лизосом
Лизосомы. Типы лизосом Основные закономерности наследования. Множественный аллелизм
Основные закономерности наследования. Множественный аллелизм Внутреннее строение корня, стебля
Внутреннее строение корня, стебля Окружающий мир. Животные
Окружающий мир. Животные Презентация на тему РЕФЛЕКС. РЕФЛЕКТОРНАЯ ДУГА
Презентация на тему РЕФЛЕКС. РЕФЛЕКТОРНАЯ ДУГА  Покровы позвоночных разных классов
Покровы позвоночных разных классов Царство Грибы (Mycota)
Царство Грибы (Mycota)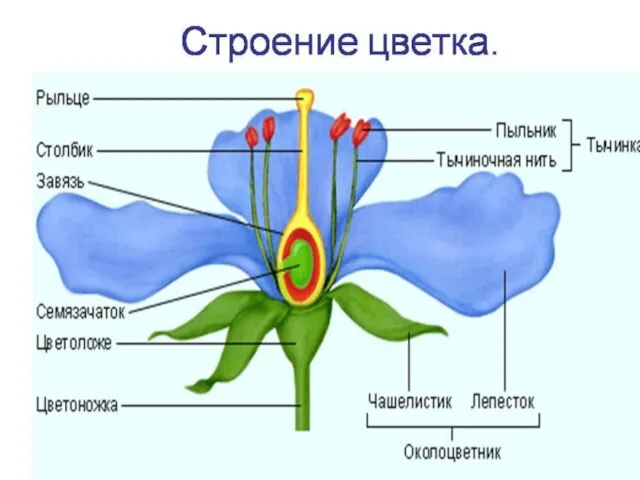 Строение цветка
Строение цветка Prezentatsia_po_biologii_9_klass_na_temu_Somaticheskiy_i_vegetativny_otdely_nervnoy_sistemy
Prezentatsia_po_biologii_9_klass_na_temu_Somaticheskiy_i_vegetativny_otdely_nervnoy_sistemy Презентация на тему Элементарные факторы эволюции
Презентация на тему Элементарные факторы эволюции  Animal Idioms
Animal Idioms Презентация на тему "Липиды" - презентации по Биологии
Презентация на тему "Липиды" - презентации по Биологии Живые участники круговорота веществ в природе
Живые участники круговорота веществ в природе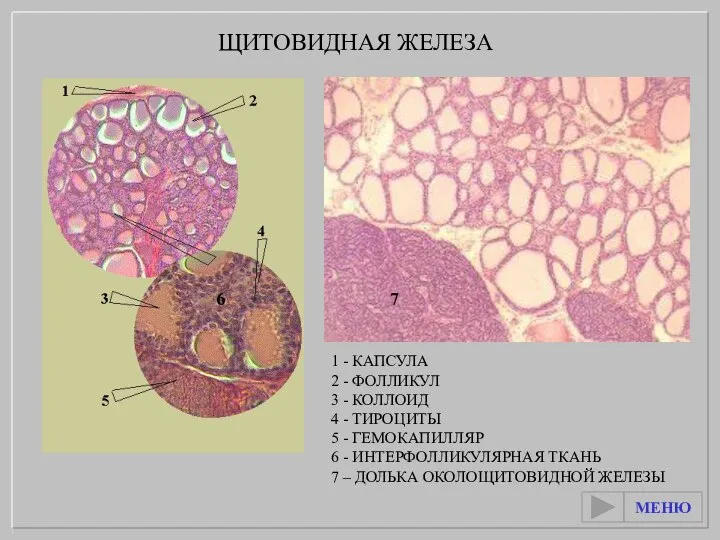 Щитовидная железа
Щитовидная железа