Содержание
- 2. Ферменты Ферменты - это белковые вещества, играющие очень важную роль в различных биохимических процессах в организме.
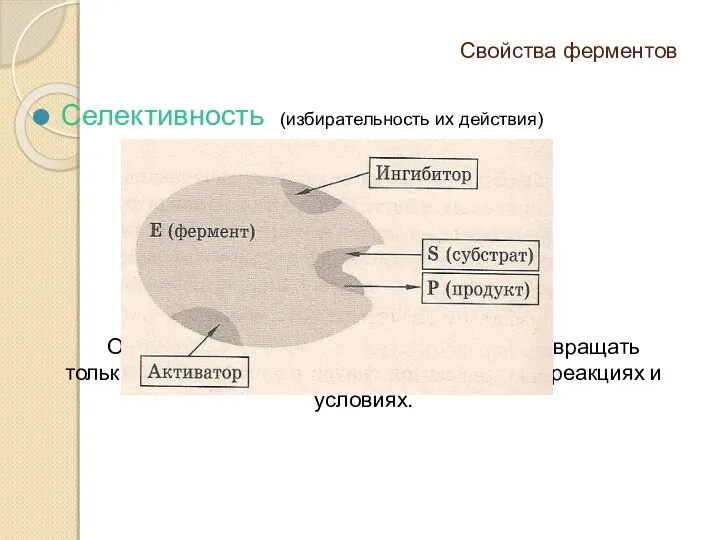
- 3. Свойства ферментов Селективность (избирательность их действия) Определяется способностью фермента превращать только данный тип субстратов в определенных
- 4. Высокая каталитическая активность Добавка незначительной концентрации фермента ускоряет превращение субстрата в 10 8 - 1012 раз.
- 5. Зависимость от температуры Многие ферменты обладают наибольшей эффективностью при температуре человеческого тела, т.е. приблизительно при Человек
- 6. Следующим важным свойством является то, что ферменты находятся в тканях и клетках в неактивной форме (проферменте).
- 7. Ферменты В зависимости от того, какие виды реакций организма катализируют ферменты, они выполняют различные функции. Чаще
- 8. Пищеварительные ферменты Различают три основные категории таких ферментов: амилаза, протеазы, липаза. Амилаза расщепляет углеводы и находится
- 9. Классификация ферментов На Международном биохимическом съезде было принято, что ферменты должны классифицироваться по типу реакции, катализируемой
- 10. Классификация ферментов 1.Оксидоредуктазы - ферменты, катализирующие окислительно-восстановительные реакции, например каталаза: 2 H2O2-->O2+2 H2O 2.Трансферазы - ферменты,
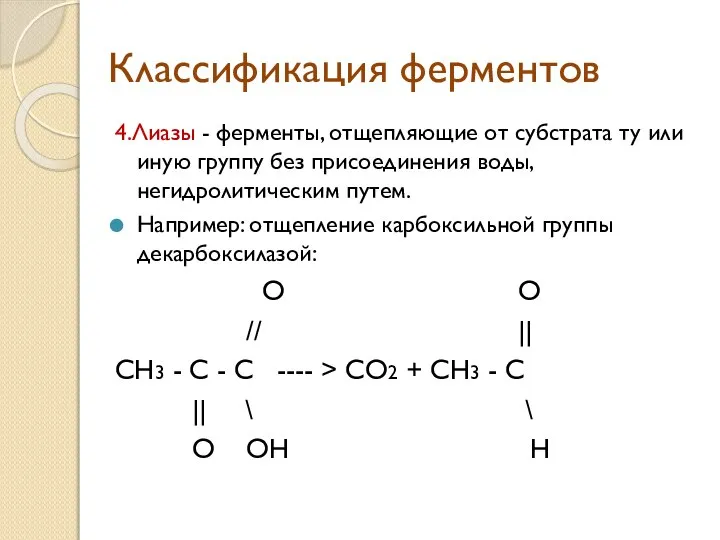
- 11. Классификация ферментов 4.Лиазы - ферменты, отщепляющие от субстрата ту или иную группу без присоединения воды, негидролитическим
- 12. 5.Изомеразы - ферменты, катализирующие превращение одного изомера в другой: глюкозо-6-фосфат --> глюкозо-1-фосфат 6.Синтетазы - ферменты, катализирующие
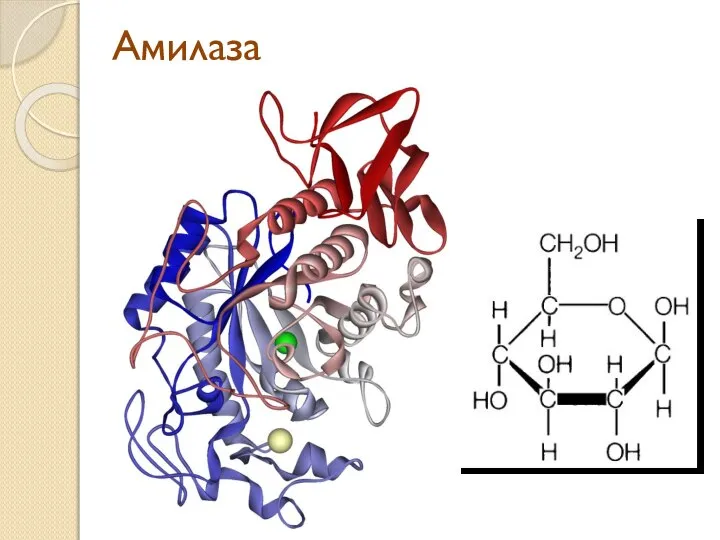
- 13. Амилаза
- 14. Амилаза, расщепляя крахмал и другие углеводы, обеспечивает переваривание углеводов пищи. Из организма амилазу выводят почки вместе
- 15. С диагностической точки зрения наиболее информативным является определение панкреатической амилазы, на активность, которой в крови приходится
- 16. В клинической лабораторной практике распространены две группы методов исследования активности альфа-амилазы в биологических жидкостях: 1.Сахарифицирующие, основанные
- 17. Увеличение активности амилазы более чем в 10 раз: При остром панкреатите активность амилазы в крови и
- 18. Уровень активности амилазы в норме. -в сыворотке 25 - 220 МЕ/Л или 8-32 ЕД -в моче
- 19. Применение ферментов Ферменты используют для смягчения кожи в кожевенной промышленности. Ферменты входят в состав стиральных порошков,
- 20. Применение ферментов Ферменты получили широкое применение в легкой, пищевой и химической промышленности, а также в медицине.
- 22. Скачать презентацию















 Перец Скорпион Тринидада
Перец Скорпион Тринидада Презентация на тему Губит людей и пиво
Презентация на тему Губит людей и пиво  Лучевая болезнь. Патофизиология воздействия ионизирующего излучения
Лучевая болезнь. Патофизиология воздействия ионизирующего излучения Биология – наука о жизни. Методы исследования в биологии
Биология – наука о жизни. Методы исследования в биологии Классификация споровых растений
Классификация споровых растений Пищеварительная система (демонстрационный материал)
Пищеварительная система (демонстрационный материал)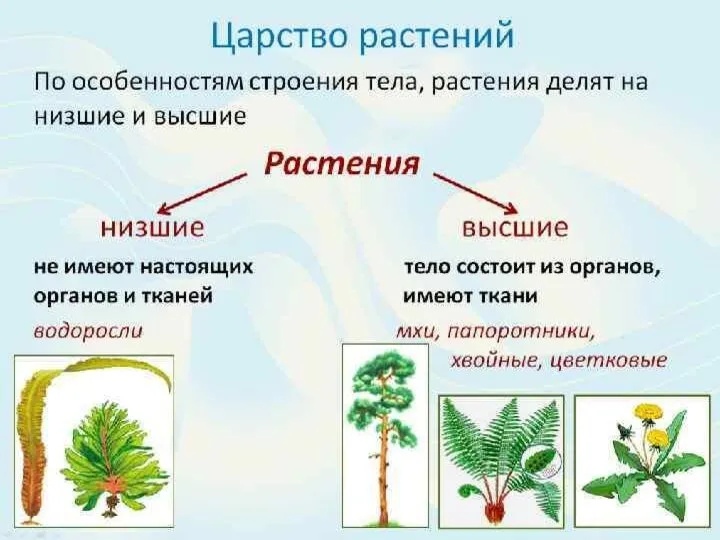 Царство растений
Царство растений Организм человека как биологическая система
Организм человека как биологическая система Дыхание
Дыхание Бионеорганическая химия. Биогенные элементы. (Лекция 5.2)
Бионеорганическая химия. Биогенные элементы. (Лекция 5.2) По следам лягушки-путешественницы. Гаршин Всеволод Михайлович (1855г.-1888г.)
По следам лягушки-путешественницы. Гаршин Всеволод Михайлович (1855г.-1888г.) Отдел формирования (древесные школы)
Отдел формирования (древесные школы) Загальна характеристика класу Ракоподібні
Загальна характеристика класу Ракоподібні Синицы
Синицы Жизнь организмов в морях и океанах
Жизнь организмов в морях и океанах Переваривание и всасывание белков. Продукты белкового обмена
Переваривание и всасывание белков. Продукты белкового обмена Мозг человека
Мозг человека Грибы. Строение грибов
Грибы. Строение грибов Наследование дифференцированного состояния клеток
Наследование дифференцированного состояния клеток Баргузинский заповедник
Баргузинский заповедник Зрительный анализатор
Зрительный анализатор Нервова система
Нервова система Класс Паукообразные. 7 класс
Класс Паукообразные. 7 класс Презентация на тему Строение и значение стебля
Презентация на тему Строение и значение стебля  Лес - Зелёный друг
Лес - Зелёный друг Генетика
Генетика Обобщение и систематизация знаний. Общая характеристика растений
Обобщение и систематизация знаний. Общая характеристика растений Анатомия насекомых
Анатомия насекомых