Содержание
- 2. Аминокислоты – предшественники для синтеза, в первую оче- редь, белка, а также для синтеза других биоактивных
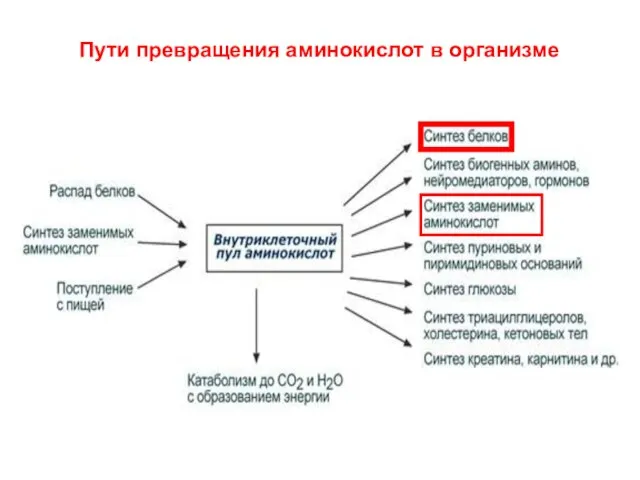
- 3. Пути превращения аминокислот в организме
- 4. Участие аминокислот в обмене Помимо участия в синтезе пептидов и белков, большинство аминокислот участвуют во многих
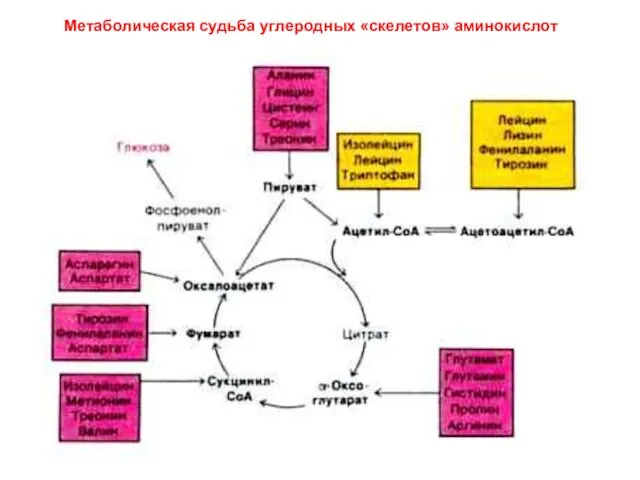
- 5. Метаболическая судьба углеродных «скелетов» аминокислот
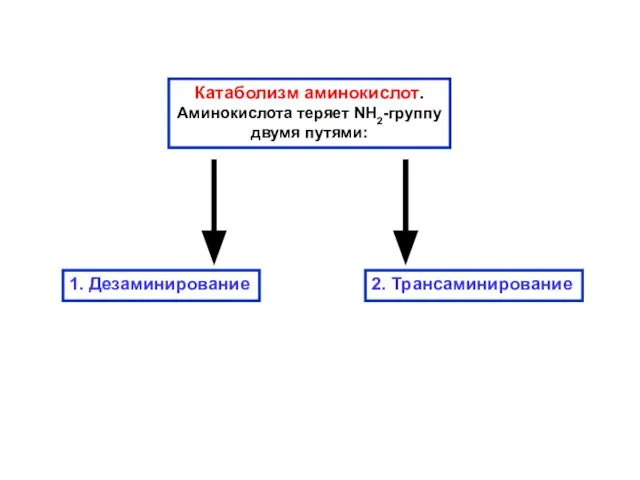
- 6. Катаболизм аминокислот. Аминокислота теряет NH2-группу двумя путями: 1. Дезаминирование 2. Трансаминирование
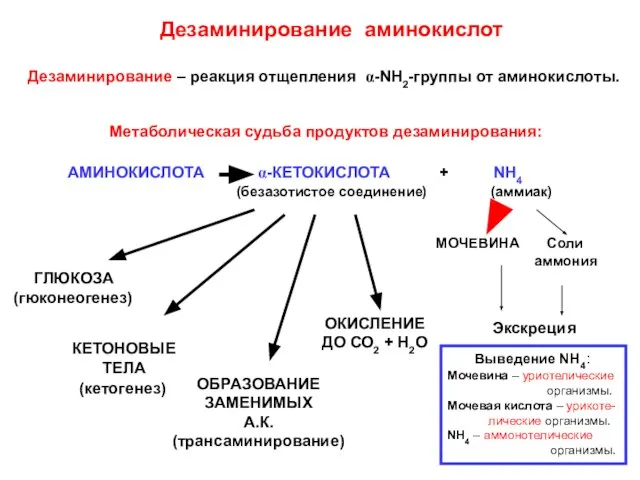
- 7. Дезаминирование аминокислот Дезаминирование – реакция отщепления α-NH2-группы от аминокислоты. АМИНОКИСЛОТА α-КЕТОКИСЛОТА + NH4 (безазотистое соединение) (аммиак)
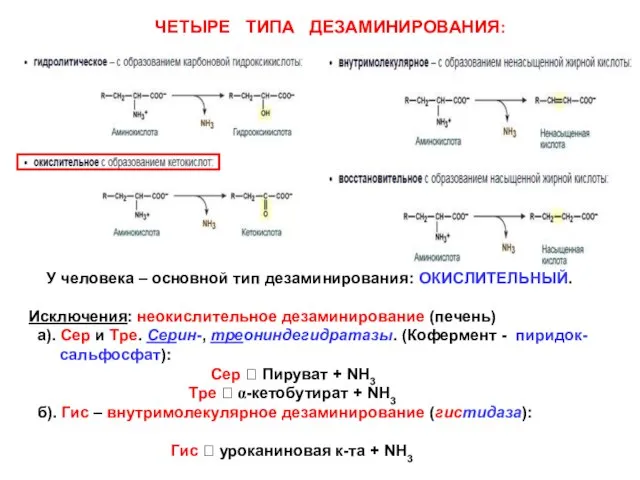
- 8. ЧЕТЫРЕ ТИПА ДЕЗАМИНИРОВАНИЯ: У человека – основной тип дезаминирования: ОКИСЛИТЕЛЬНЫЙ. Исключения: неокислительное дезаминирование (печень) а). Сер
- 9. ОКИСЛИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ Реакция обратима: при повышении [NH4] идёт в обратном направле- нии – восстановительное аминирование α-КГ.
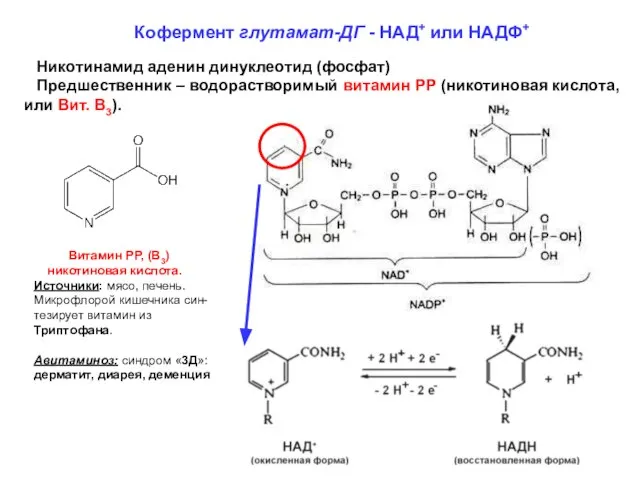
- 10. Кофермент глутамат-ДГ - НАД+ или НАДФ+ Никотинамид аденин динуклеотид (фосфат) Предшественник – водорастворимый витамин РР (никотиновая
- 11. НЕПРЯМОЕ ДЕЗАМИНИОВАНИЕ (ТРАНСДЕЗАМИНИРОВАНИЕ) Большинство аминокислот дезаминируется в две стадии: I стадия: Трансаминирование аминотрансфераза (кофермент ПФ) аминокислота
- 12. ОКСИДАЗЫ L- и D-АМИНОКИСЛОТ Оксидазы присутствуют в печени и почках – дезаминируют неко- торые аминокислоты: Оксидаза
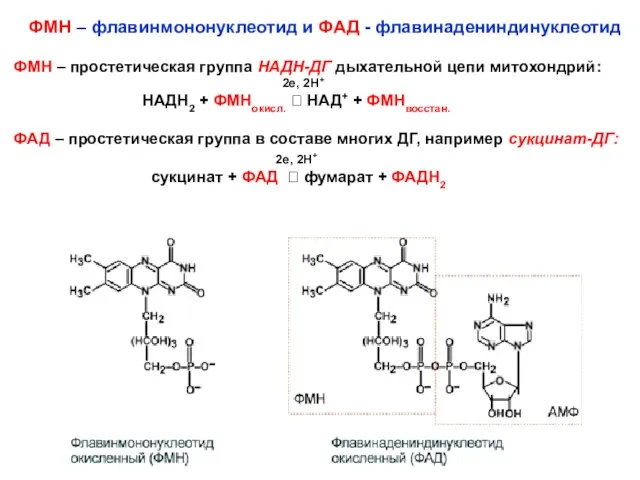
- 13. ФМН – флавинмононуклеотид и ФАД - флавинадениндинуклеотид ФМН – простетическая группа НАДН-ДГ дыхательной цепи митохондрий: 2e,
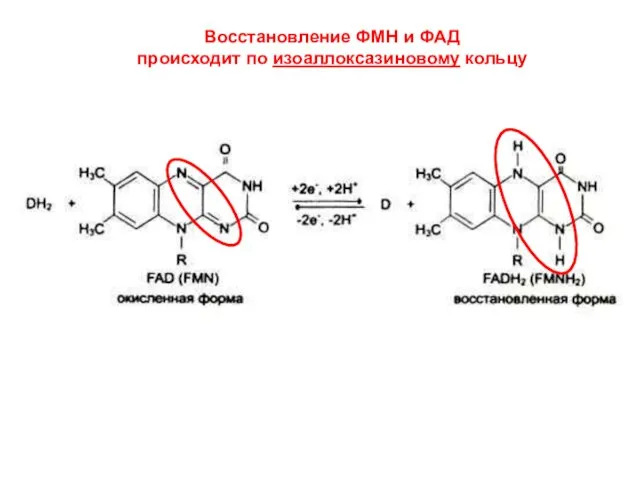
- 14. Восстановление ФМН и ФАД происходит по изоаллоксазиновому кольцу
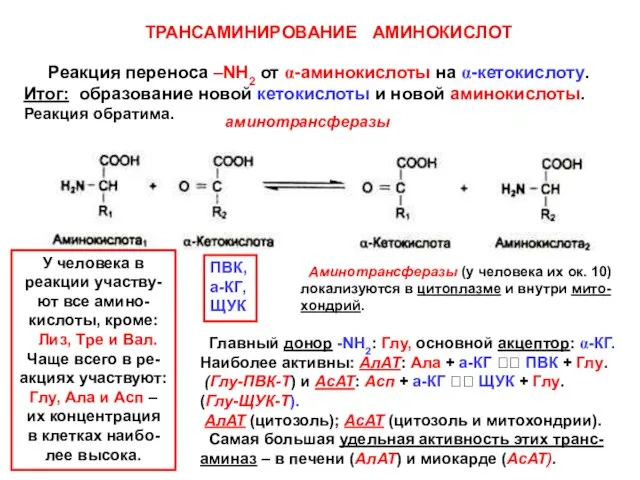
- 15. ТРАНСАМИНИРОВАНИЕ АМИНОКИСЛОТ Реакция переноса –NH2 от α-аминокислоты на α-кетокислоту. Итог: образование новой кетокислоты и новой аминокислоты.
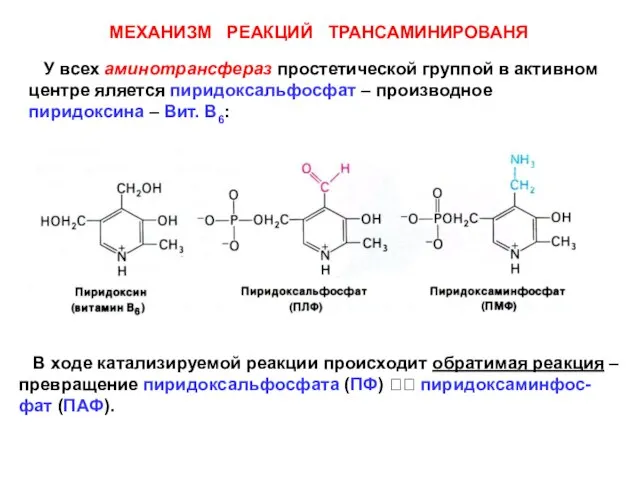
- 16. МЕХАНИЗМ РЕАКЦИЙ ТРАНСАМИНИРОВАНЯ У всех аминотрансфераз простетической группой в активном центре яляется пиридоксальфосфат – производное пиридоксина
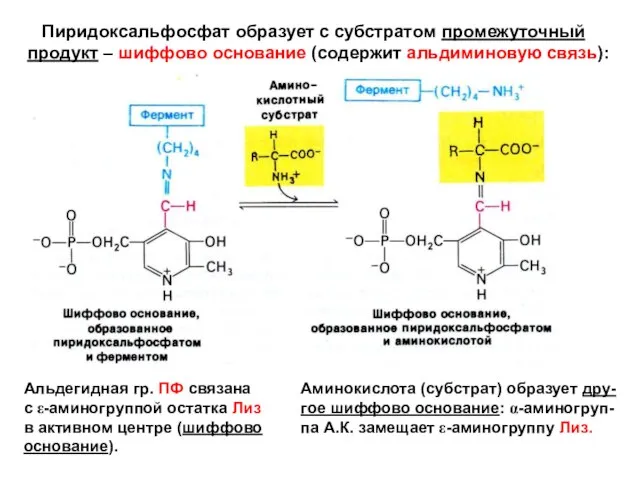
- 17. Пиридоксальфосфат образует с субстратом промежуточный продукт – шиффово основание (содержит альдиминовую связь): Альдегидная гр. ПФ связана
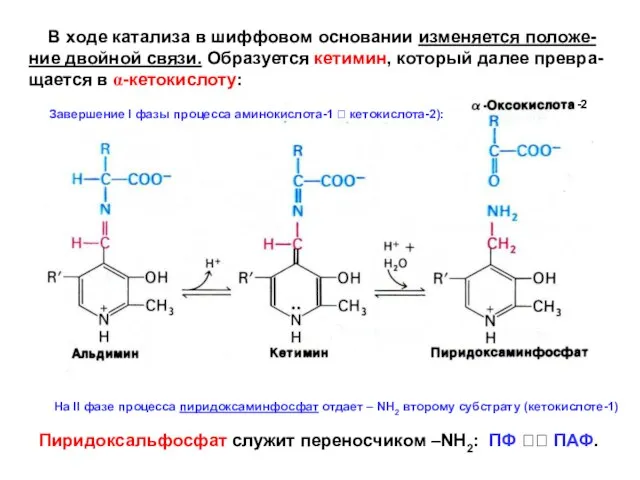
- 18. В ходе катализа в шиффовом основании изменяется положе- ние двойной связи. Образуется кетимин, который далее превра-
- 19. В результате работы аминотрансфераз азот аминогрупп многих А.К. переходит в состав аминогруппы Глу. Эти реакции проходят
- 20. ДЕКАРБОКСИЛИРОВАНИЕ АМИНОКИСЛОТ Реакция отщепления карбоксильной группы с образованем ами- нов: пиридоксальфосфат Реакции декарбоксилирования А.К., в отличие
- 22. Скачать презентацию


![ОКИСЛИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ Реакция обратима: при повышении [NH4] идёт в обратном направле- нии](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/905409/slide-8.jpg)




 Интересные факты о черепахах
Интересные факты о черепахах Строение инфузории и амебы
Строение инфузории и амебы dnk_i_rnk_-_nukleinovye_kisloty
dnk_i_rnk_-_nukleinovye_kisloty Ordering flowers
Ordering flowers Летний лес - полный чудес
Летний лес - полный чудес Терморегуляция. Закаливание. Выделение пота
Терморегуляция. Закаливание. Выделение пота Сибирский багульник
Сибирский багульник Птицы удмуртского края
Птицы удмуртского края Мейоз. Гаметогенез
Мейоз. Гаметогенез Ткани животных и человека
Ткани животных и человека морфология анатомия листа
морфология анатомия листа Понятие изменчивости
Понятие изменчивости Прародина человека
Прародина человека Как зимуют звери в лесу
Как зимуют звери в лесу Плесневые грибы и дрожжи
Плесневые грибы и дрожжи Анаболизм. Автотрофное питание. Фотосинтез. II стадия фотосинтеза - темновая
Анаболизм. Автотрофное питание. Фотосинтез. II стадия фотосинтеза - темновая Памятники природы
Памятники природы Sprache und Gehirn. Anatomische Grundlagen
Sprache und Gehirn. Anatomische Grundlagen 11. Биосинтез углеводов — фотосинтез
11. Биосинтез углеводов — фотосинтез Жизнь в пресных водах
Жизнь в пресных водах Сортоиспытание огурца в открытом грунте на Сергачском государственном сортоиспытательном участке
Сортоиспытание огурца в открытом грунте на Сергачском государственном сортоиспытательном участке Клеточное строение листа
Клеточное строение листа Особенности строения черепа разных групп млекопитающих
Особенности строения черепа разных групп млекопитающих Плейотропия.. Взаимодействие генов
Плейотропия.. Взаимодействие генов Теория эволюции. Первые организмы на Земле и их эволюция
Теория эволюции. Первые организмы на Земле и их эволюция Përçuarja e ujit nëpër bimë
Përçuarja e ujit nëpër bimë Презентация на тему Хвойные леса умеренного пояса и их обитатели
Презентация на тему Хвойные леса умеренного пояса и их обитатели  Радость и печаль Жердевской осени
Радость и печаль Жердевской осени