Содержание
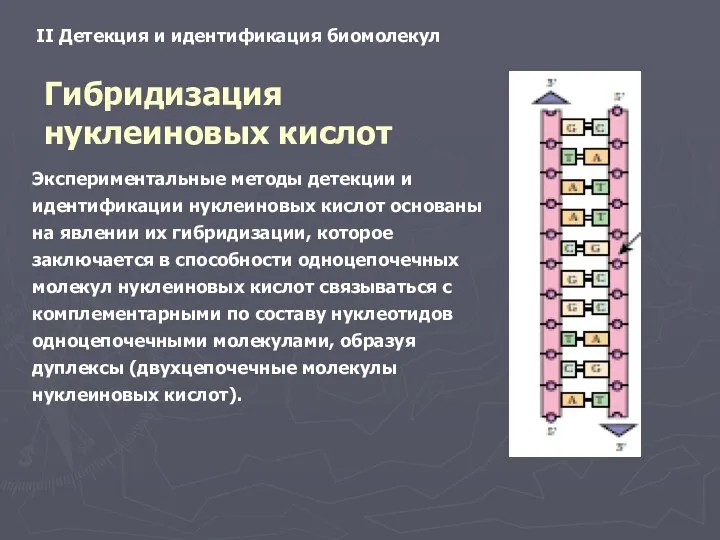
- 2. II Детекция и идентификация биомолекул Гибридизация нуклеиновых кислот Экспериментальные методы детекции и идентификации нуклеиновых кислот основаны
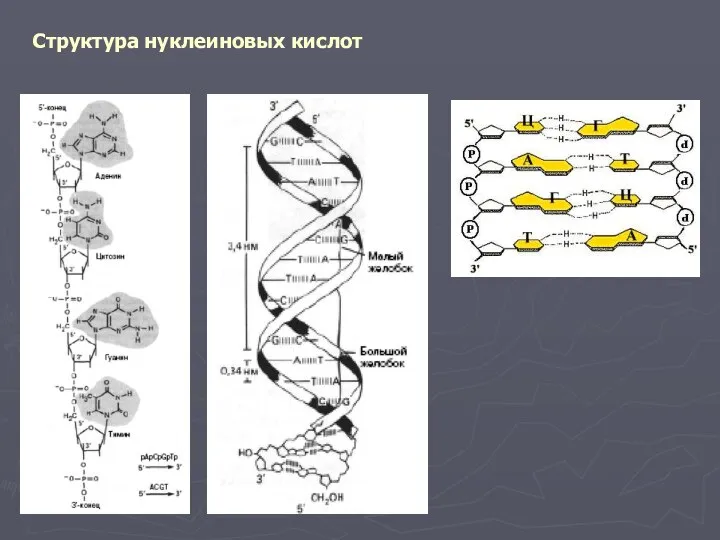
- 3. Структура нуклеиновых кислот
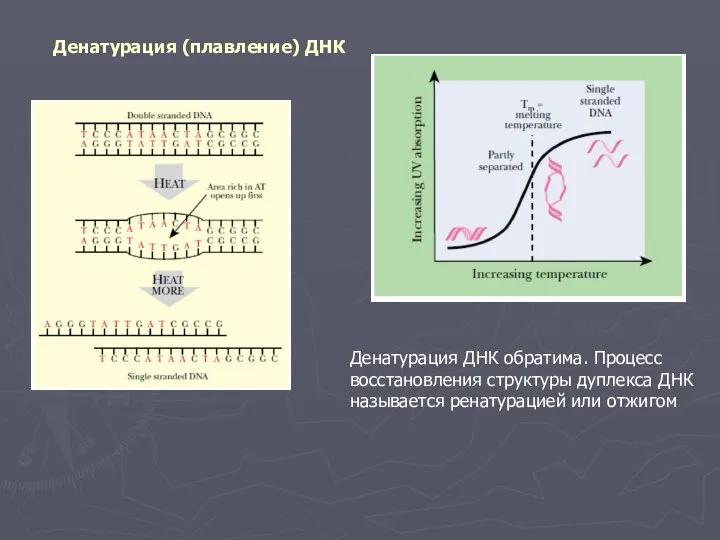
- 4. Денатурация (плавление) ДНК Денатурация ДНК обратима. Процесс восстановления структуры дуплекса ДНК называется ренатурацией или отжигом
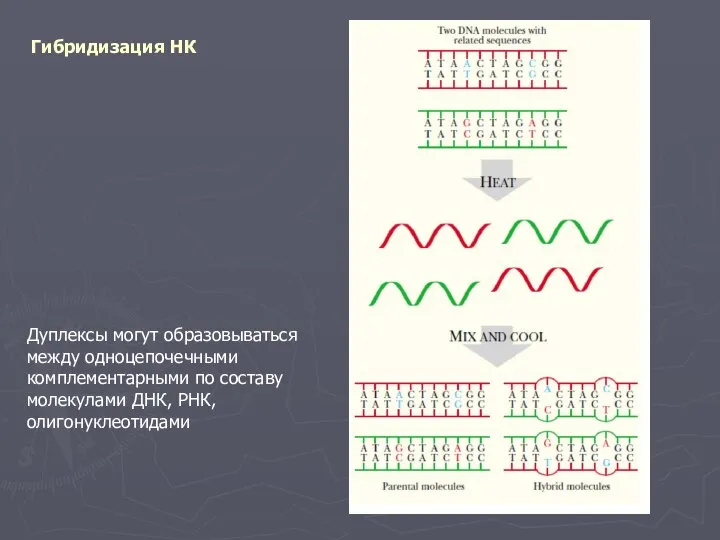
- 5. Гибридизация НК Дуплексы могут образовываться между одноцепочечными комплементарными по составу молекулами ДНК, РНК, олигонуклеотидами
- 6. Стабильность дуплексов нуклеиновых кислот определяется следующими факторами: длина цепей − длинные дуплексы удерживаются большим числом водородных
- 7. Мерой стабильности дуплекса нуклеиновых кислот является температура плавления (Tm). Это температура, соответствующая средней точке перехода между
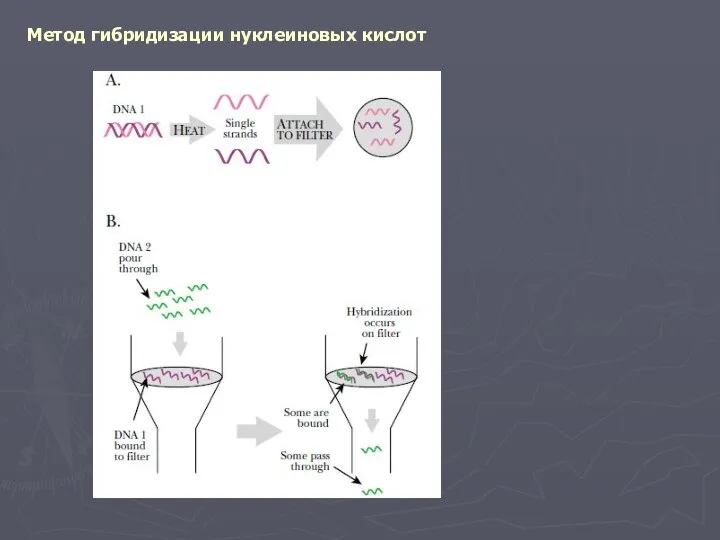
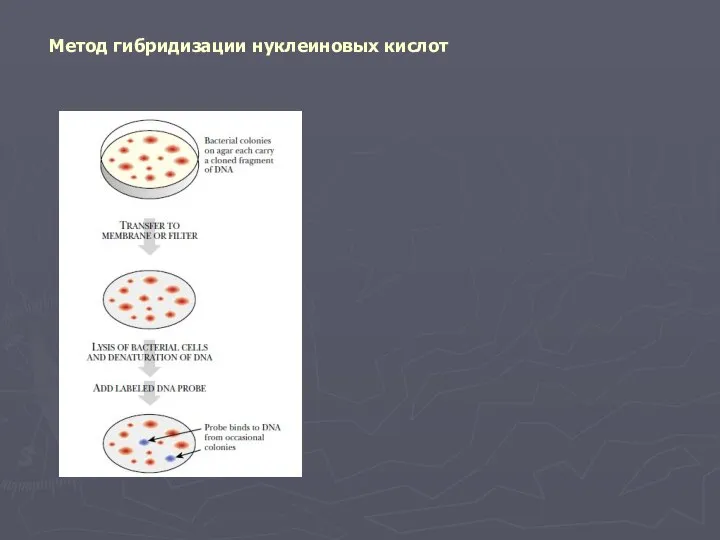
- 8. Метод гибридизации нуклеиновых кислот
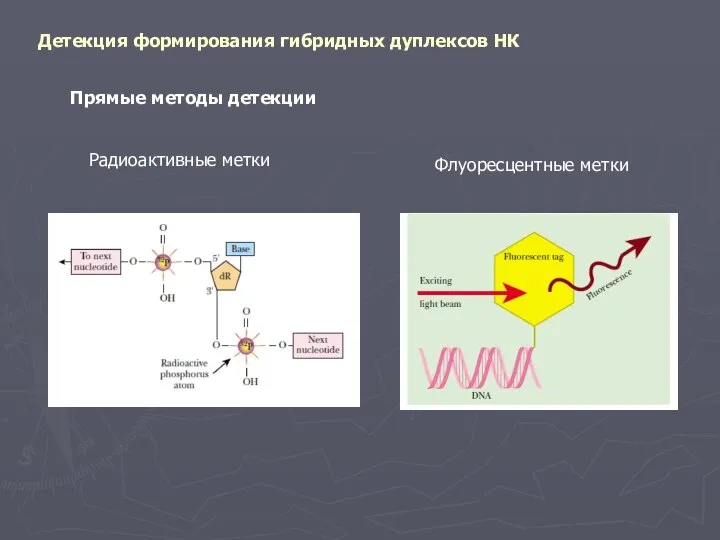
- 9. Детекция формирования гибридных дуплексов НК Прямые методы детекции Радиоактивные метки Флуоресцентные метки
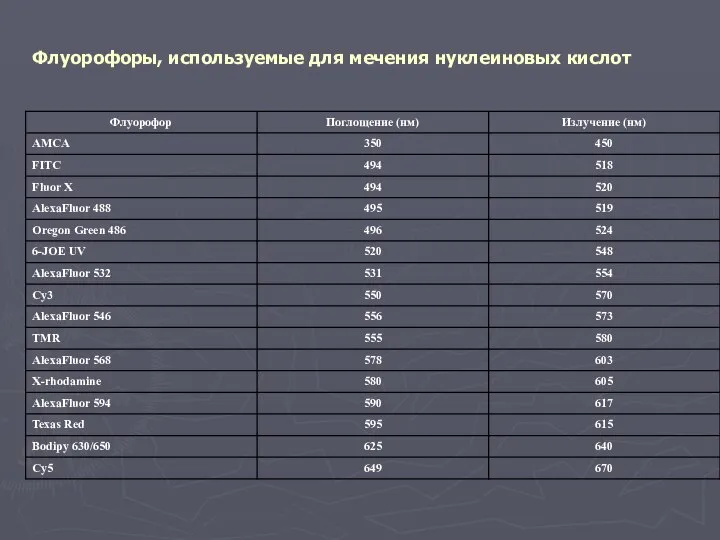
- 10. Флуорофоры, используемые для мечения нуклеиновых кислот
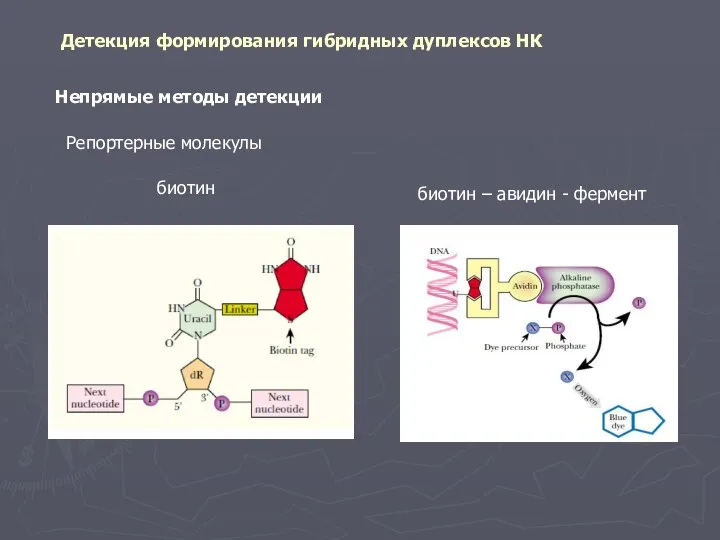
- 11. Непрямые методы детекции Детекция формирования гибридных дуплексов НК Репортерные молекулы биотин биотин – авидин - фермент
- 12. Метод гибридизации нуклеиновых кислот
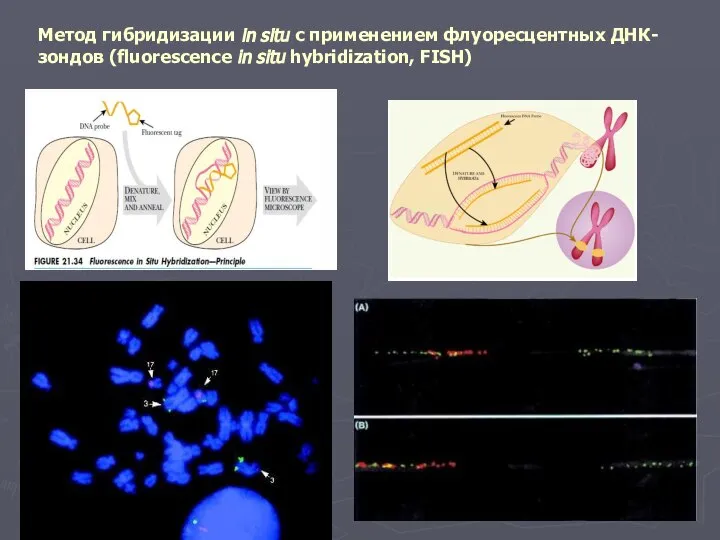
- 13. Метод гибридизации in situ с применением флуоресцентных ДНК-зондов (fluorescence in situ hybridization, FISH)
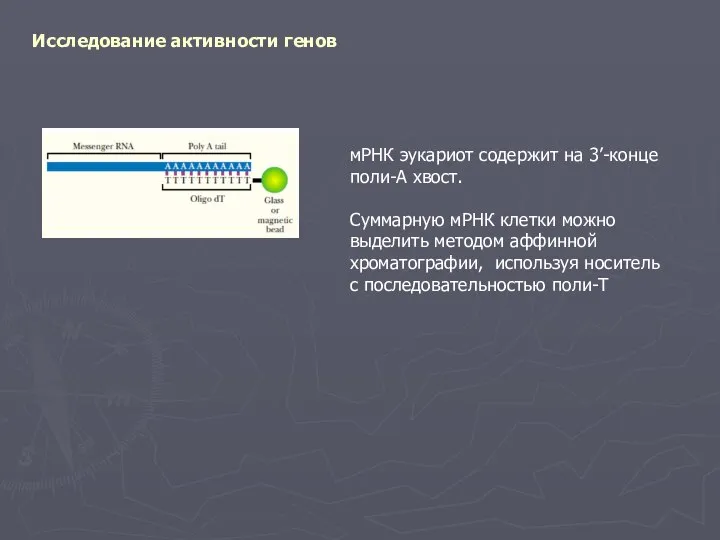
- 14. Исследование активности генов мРНК эукариот содержит на 3’-конце поли-А хвост. Суммарную мРНК клетки можно выделить методом
- 15. Исследование активности генов ДНК-микроматрицы и ДНК-биочипы
- 16. Исследование активности генов
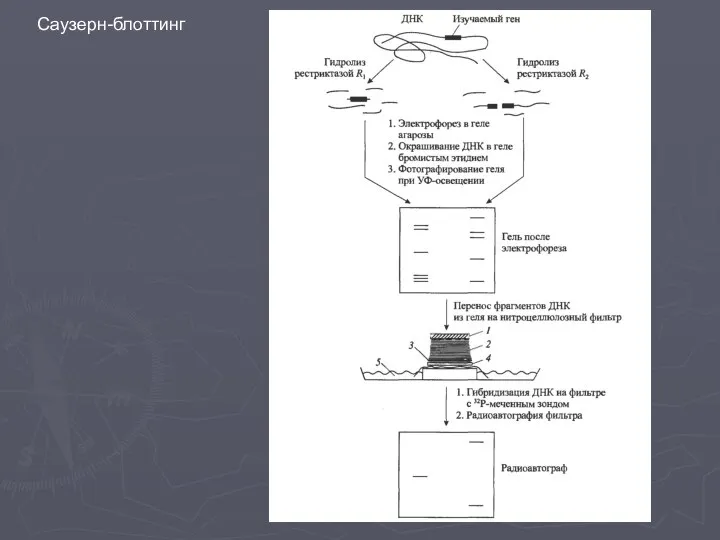
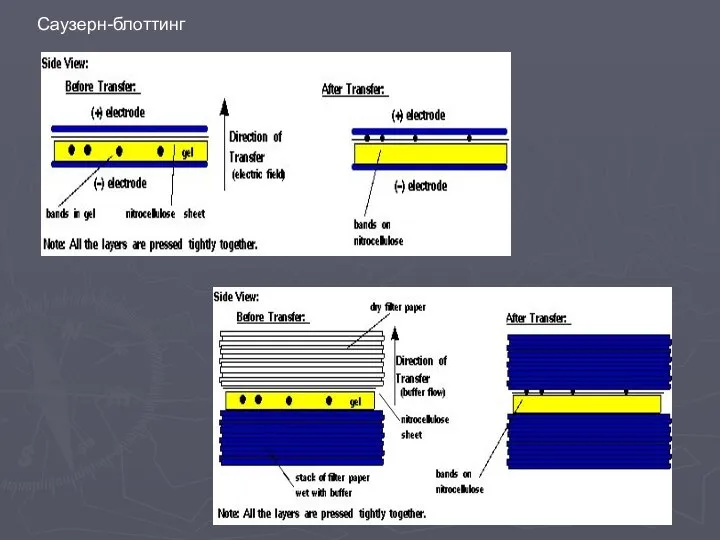
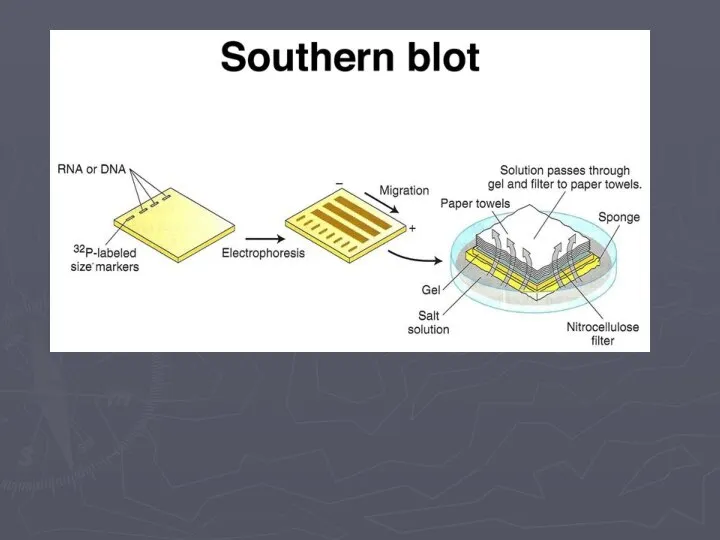
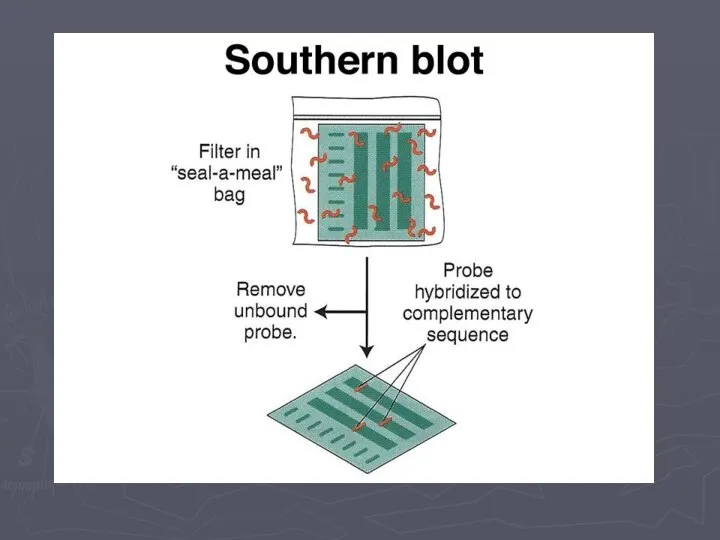
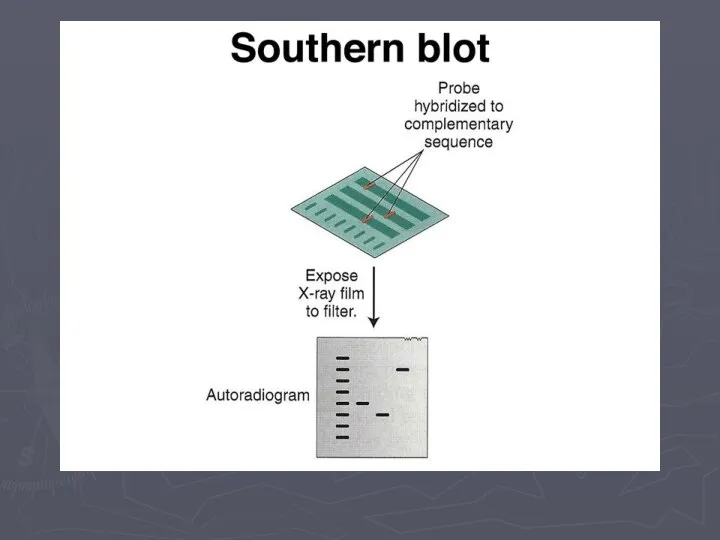
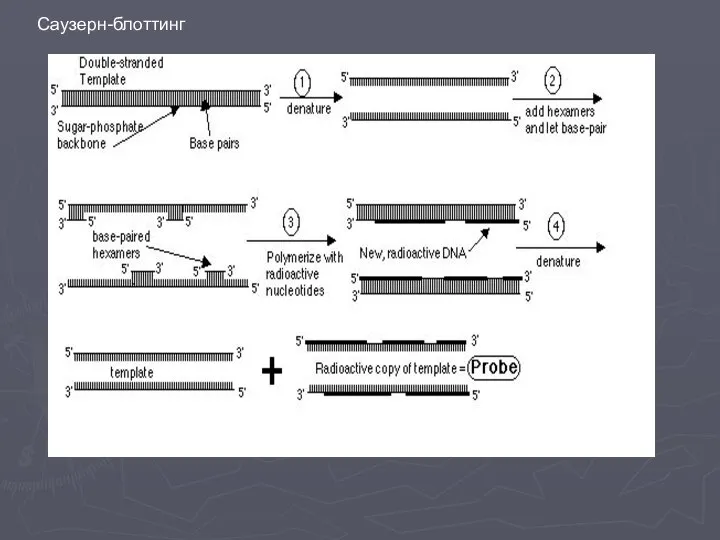
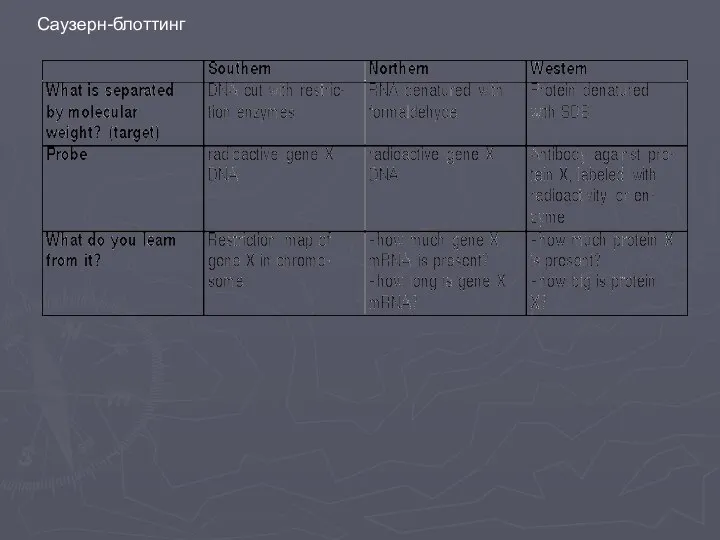
- 17. Саузерн-блоттинг
- 18. Саузерн-блоттинг
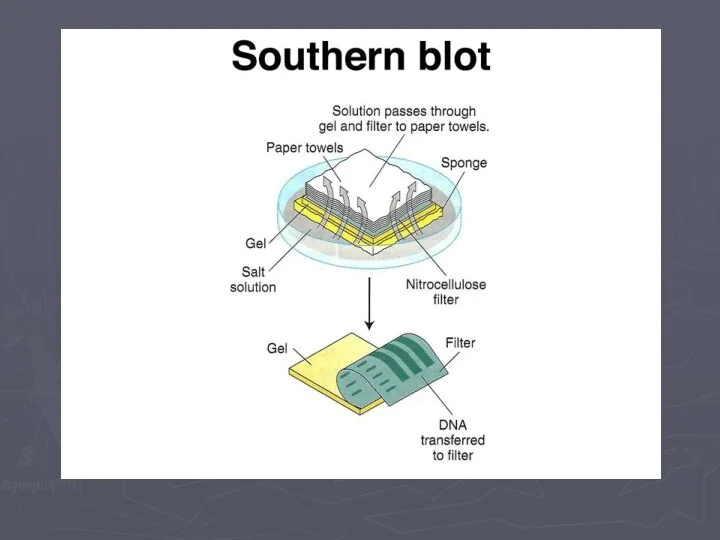
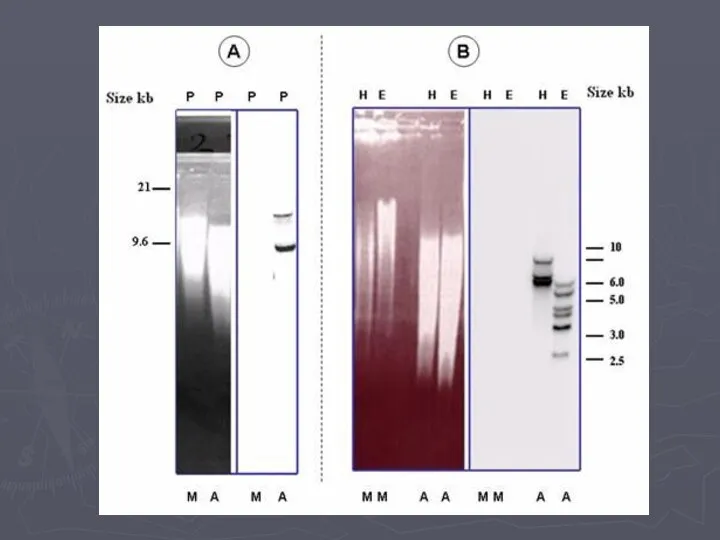
- 24. Саузерн-блоттинг
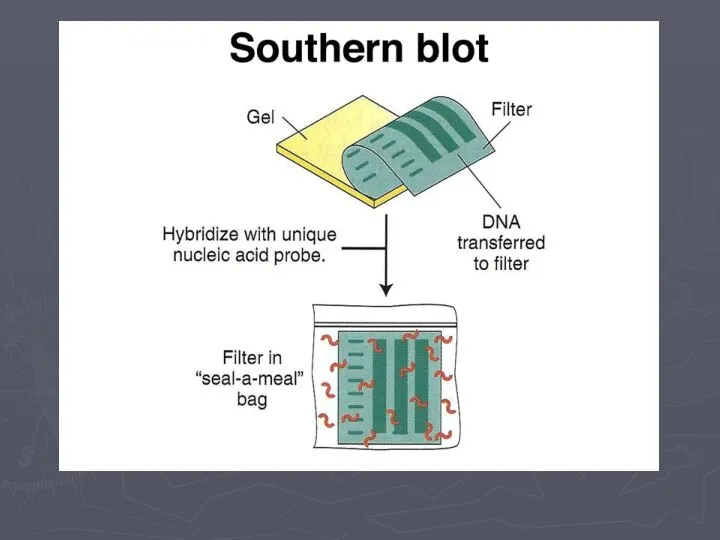
- 26. Саузерн-блоттинг
- 28. Скачать презентацию




 Свиньи. Характеристика
Свиньи. Характеристика Дыхание растений
Дыхание растений Происхождение человека. 6 класс
Происхождение человека. 6 класс 4. 1. Характеристика и систематика растений
4. 1. Характеристика и систематика растений Презентация на тему Биосфера - живая оболочка планеты
Презентация на тему Биосфера - живая оболочка планеты  Ботаника. Микология. Лишайники. Бактерии
Ботаника. Микология. Лишайники. Бактерии Подцарство одноклеточные. Тип саркодовые. Класс саркодовые
Подцарство одноклеточные. Тип саркодовые. Класс саркодовые Как прекрасен этот мир!
Как прекрасен этот мир! Анализаторы
Анализаторы Экологическое сортоиспытание гибридов арбузов в условиях Мозыркого Полесья
Экологическое сортоиспытание гибридов арбузов в условиях Мозыркого Полесья Дыхание растений. Тест
Дыхание растений. Тест Биология - наука о живой природе
Биология - наука о живой природе Клуб любителей кошек
Клуб любителей кошек Body clock
Body clock Египетская гладкошерстная кошка
Египетская гладкошерстная кошка Жизненный цикл клетки. 10 класс
Жизненный цикл клетки. 10 класс Сухопутные черепахи
Сухопутные черепахи Анатомия, физиология и патология зрительного анализатора
Анатомия, физиология и патология зрительного анализатора Презентация на тему Внешнее и внутреннее строение корня
Презентация на тему Внешнее и внутреннее строение корня  Изучение антимикробной активности слизи улитки achatina fulica
Изучение антимикробной активности слизи улитки achatina fulica Высшая нервная деятельность. Рефлексы
Высшая нервная деятельность. Рефлексы Подборка заданий линии 24 (задания 2 части ЕГЭ с ошибками в тексте) из сборников Рохлова
Подборка заданий линии 24 (задания 2 части ЕГЭ с ошибками в тексте) из сборников Рохлова Росянка (лат. Drósera)
Росянка (лат. Drósera) Презентация на тему Самые ядовитые и опасные пауки в мире
Презентация на тему Самые ядовитые и опасные пауки в мире  Презентация на тему Бактериологическое оружие и его воздействие на организм человека
Презентация на тему Бактериологическое оружие и его воздействие на организм человека  Зодіакальна система та здоров'я. Планування робочого часу. Біологічні ритми в живих системах
Зодіакальна система та здоров'я. Планування робочого часу. Біологічні ритми в живих системах Анатомия сердца
Анатомия сердца Грибы. Тест
Грибы. Тест