Слайд 2Роль железа в организме человека
Недостаточное количество этого микроэлемента может отражаться на

общем состоянии здоровья и самочувствии. Железо имеет одно из важнейших значений, ведь оно отвечает за выработку гемоглобина в крови, который поддерживает питание органов, тканей и систем, а также транспортирует кислород к тканям и органам.
Слайд 3Функции железа
Этот микроэлемент содержится в организме в малых количествах, но он выполняет
следующие функции: поддерживает иммунную систему; укрепляет костные ткани; поддерживает работу поджелудочной железы; нормализует кровообращение; повышает физическую активность; поддерживает функционирование нервной системы. Железо в организм
попадает вместе с пищей.
В продуктах животного
происхождения
микроэлемент содержится в
Легкоусвояемом виде.
Присутствует железо и в
растительной
продукции
Слайд 4Опасность недостатка железа
Если вовремя не восполнить уровень микроэлемента в крови, то может

развиться: анемия; сердечная недостаточность; аритмия; депрессия; постоянные инфекционные болезни из-за снижения иммунитета.
Железодефицитное состояние также относится к одной из актуальных проблем подросткового возраста. Уменьшение количества железа в организме приводит к нарушению образования гемоглобина и снижению темпов его синтеза.
Наиболее частыми причинами анемии в подростковом возрасте являются интенсивный рост подростка, занятия тяжелыми видами спорта, исходный низкий уровень железа на фоне несбалансированного питания, вегетарианства.
Слайд 5Количество железа в организме
Железа, которое содержится в теле человека, хватит на крупный

гвоздь. Это приблизительно 2,5–4,5 грамм. Казалось бы, совсем немного. Тем не менее влияние железа на многие жизненно важные процессы огромно. Рацион питания современного человека практически не позволяет получать достаточное количество железа с пищей. В среднем мы потребляем около 10–20% от ежедневной нормы железа. Остальное можно восполнить при помощи биодобавок и витаминных комплексов.
Слайд 6Железо
Железо один из наиболее распространенных элементов на Земле. Известно свыше 300 минералов,

из которых слагают месторождения железных руд. Важнейшие рудные минералы железа: магнитный железняк Fe3O4 (содержит 72, 4 % железа), гематит гетит а – FeO(OH), или Fe2O3H2O, лепидокротит у – FeO(OH) гидрогетит FE2O3 xH2O (около 62% железа). Изделия из метеоритного железа найдены в захоронениях, относятся к очень давним временам (4 – 5 тысячелетиях до н. э.)
Слайд 7История железа
Знакомство человека с железом произошло в давние времена. Есть основание полагать,

что образцы железа, которые держали в руках первобытные люди, были неземного происхождения, он входил в состав некоторых метеоритов. Прошли многие сотни и тысячи лет, прежде чем человек научился добывать железо из руды. С того момента началась эпоха железа, которая длится и до настоящего времени.
Слайд 8Железо как химический элемент
В периодической системе железо находится в четвертом периоде, в

побочной подгруппе 8 группы. Химический знак – Fe (феррум). Порядковый номер – 26, электронная формула. (нормальное состояние атома железа) (Возбужденное состояние атомов железа) Электронно – графическая формула. Степени окисления +2 и +3 (наиболее характерны), +1, +4, +6, +8. Электроотрицательность по Полингу 1,8. Атомный радиус 0.126 нм, ионные радиусы (в нм в скобках указаны координационные числа) для Fe 0.077 (4), 0,092 (6).







 Тварини - багатство Землі
Тварини - багатство Землі Химический состав клетки
Химический состав клетки Функциональная анатомия головного мозга
Функциональная анатомия головного мозга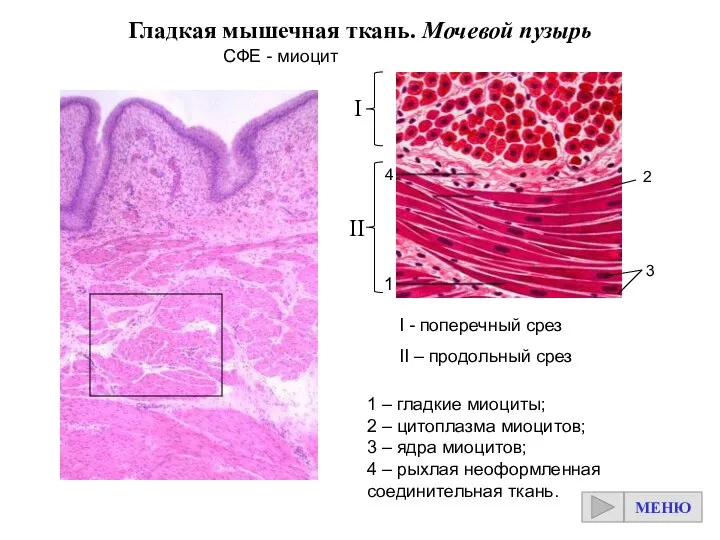 Гладкая мышечная ткань. Мочевой пузырь
Гладкая мышечная ткань. Мочевой пузырь Подключичная артерия
Подключичная артерия Бактерии: строение и жизнедеятельность
Бактерии: строение и жизнедеятельность Стебель
Стебель Строение прокариотической клетки
Строение прокариотической клетки Экологические системы
Экологические системы Гидробиология. Актуальная тематика исследовательских работ учащихся
Гидробиология. Актуальная тематика исследовательских работ учащихся Функциональная анатомия спинного мозга
Функциональная анатомия спинного мозга Cells and Tissues of the voice
Cells and Tissues of the voice Опорно-двигательная, нервная, система размножения и органы выделения животных. 6 класс
Опорно-двигательная, нервная, система размножения и органы выделения животных. 6 класс Породы собак
Породы собак Зртительные иллюзии
Зртительные иллюзии Ответьте на вопросы: На какие группы можно разделить растения В зависимости от приспособленности к условиям освещения? Какие рас
Ответьте на вопросы: На какие группы можно разделить растения В зависимости от приспособленности к условиям освещения? Какие рас Красная книга России
Красная книга России Красная книга Самарской области
Красная книга Самарской области Кишечнополостные. Жизненные формы
Кишечнополостные. Жизненные формы Энтомопатогенные грибы
Энтомопатогенные грибы Осень в жизни обитателей водоемов
Осень в жизни обитателей водоемов Глаз как оптическая система
Глаз как оптическая система Следы невиданных животных
Следы невиданных животных Корень. Корневые системы. Строение корня
Корень. Корневые системы. Строение корня Природа Казахстана
Природа Казахстана Красная Книга Тывы. Класс Птицы. 1
Красная Книга Тывы. Класс Птицы. 1 Биотехнологии
Биотехнологии Нейрокомпьютерный интерфейс. Система обмена информацией между мозгом и компьютером
Нейрокомпьютерный интерфейс. Система обмена информацией между мозгом и компьютером