Содержание
Слайд 2.
:
План рассмотрения строение электронных оболочек атомов I—III периодов
определяем общее число электронов в
.
:
План рассмотрения строение электронных оболочек атомов I—III периодов
определяем общее число электронов в

атоме, которое равно № (порядковому номеру элемента в периодической системе)
определяем число энергетических уровней в электронной оболочке (равно номеру периода, в котором находится элемент)
определяем число электронов на каждом уровне. На 1-м не больше двух, на 2-м не больше 8 электронов, на 3-м не больше 8. Хотя максимальное число электронов на 3-м уровне равно 18, атомы элементов 3 периода могут разместить на нем только 8 электронов.
На последнем внешнем уровне число электронов равно номеру группы, в которой расположен данный элемент.
определяем число энергетических уровней в электронной оболочке (равно номеру периода, в котором находится элемент)
определяем число электронов на каждом уровне. На 1-м не больше двух, на 2-м не больше 8 электронов, на 3-м не больше 8. Хотя максимальное число электронов на 3-м уровне равно 18, атомы элементов 3 периода могут разместить на нем только 8 электронов.
На последнем внешнем уровне число электронов равно номеру группы, в которой расположен данный элемент.
Слайд 31 период
Н + 1
1
n=1
S
1 S1
Нe + 2
2
n=1
S
1 S2
Одиночный электрон на незавершенной оболочке
2
1 период
Н + 1
1
n=1
S
1 S1
Нe + 2
2
n=1
S
1 S2
Одиночный электрон на незавершенной оболочке
2

спаренных электрона на завершенной оболочке
S - элементы
+
+
Слайд 42 период
Li + 3
2 1
n=1
n=2
1 S2 2 S1
Be + 4
2 2
n=1
n=2
1 S2
2 период
Li + 3
2 1
n=1
n=2
1 S2 2 S1
Be + 4
2 2
n=1
n=2
1 S2
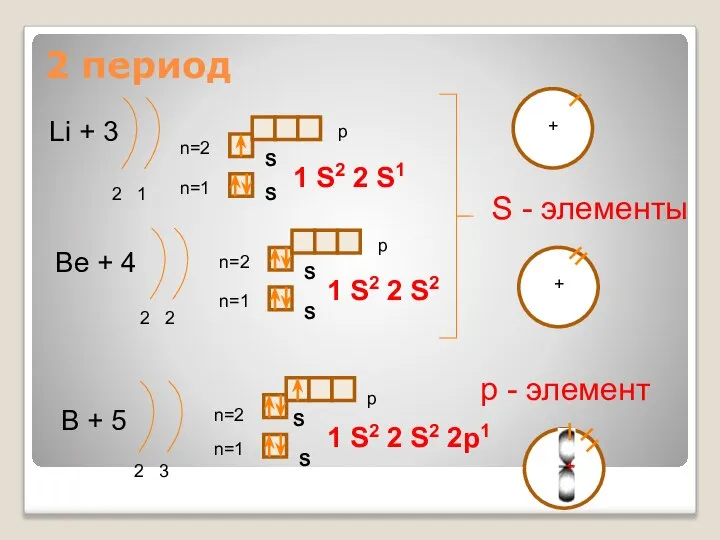
2 S2
B + 5
2 3
n=1
n=2
1 S2 2 S2 2p1
S - элементы
р - элемент
S
S
S
S
S
S
p
p
p
+
+
+
+
Слайд 52 период
С + 6
2 4
n=1
n=2
N + 7
2 5
n=1
n=2
O + 8
2 6
n=1
n=2
1 S2
2 период
С + 6
2 4
n=1
n=2
N + 7
2 5
n=1
n=2
O + 8
2 6
n=1
n=2
1 S2
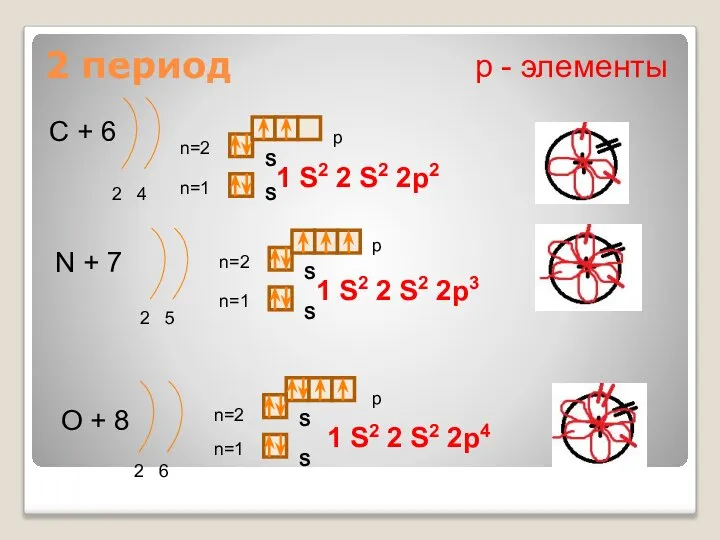
2 S2 2p4
р - элементы
1 S2 2 S2 2p2
1 S2 2 S2 2p3
S
S
S
S
S
S
p
p
p
- Предыдущая
Периодическая системаСледующая -
Гимнастика. Виды и дисциплины гимнастики Основные сведения о строении атома
Основные сведения о строении атома Сила тяжіння. Вага тіла. Невагомість
Сила тяжіння. Вага тіла. Невагомість Решение задач на вычисление значения сопротивления силы тока, напряжения в цепи переменного тока
Решение задач на вычисление значения сопротивления силы тока, напряжения в цепи переменного тока Серия автомобильных 2-стоечных подъемников грузоподъемностью 4 500 кг - RLP2-450
Серия автомобильных 2-стоечных подъемников грузоподъемностью 4 500 кг - RLP2-450 Динамика жидкости и твердого тела
Динамика жидкости и твердого тела Давление газов. Закон Паскаля
Давление газов. Закон Паскаля Конденсаторы. Схемы электрической цепи (Тест) (8 класс)
Конденсаторы. Схемы электрической цепи (Тест) (8 класс) Оборудование для ремонта бытовых электроприборов
Оборудование для ремонта бытовых электроприборов Гамма- излучение
Гамма- излучение Физическая викторина
Физическая викторина Ядерные реакции. Процесс столкновения микрочастицы с атомным ядром
Ядерные реакции. Процесс столкновения микрочастицы с атомным ядром Газовая хроматография
Газовая хроматография Электроемкость, конденсаторы
Электроемкость, конденсаторы Автотрансформаторы
Автотрансформаторы Сила
Сила Построение структур, обобщенные параметры, классификация и расчет составов ДНПКМ. Лекция 5
Построение структур, обобщенные параметры, классификация и расчет составов ДНПКМ. Лекция 5 Динамика. Сила
Динамика. Сила Законы отражения света. Свойства изображения в плоском зеркале. Законы преломления
Законы отражения света. Свойства изображения в плоском зеркале. Законы преломления Реактивная сила
Реактивная сила Научно-исследовательская работа. Парадоксы физики
Научно-исследовательская работа. Парадоксы физики Потенциальная энергия. (Лекция 4)
Потенциальная энергия. (Лекция 4) Режимы движения жидкости. Лекция 3
Режимы движения жидкости. Лекция 3 Закон сохранения импульса
Закон сохранения импульса Стихотворение Ученье - свет, а не ученье - тьма
Стихотворение Ученье - свет, а не ученье - тьма Презентация на тему Взаимодействие тел
Презентация на тему Взаимодействие тел  Закон вращательного движения абсолютно твердого тела. Гироскоп
Закон вращательного движения абсолютно твердого тела. Гироскоп Презентация на тему Эрнест Резерфорд. Планетарная модель атома
Презентация на тему Эрнест Резерфорд. Планетарная модель атома  Сила. Сила тяжести
Сила. Сила тяжести