Содержание
- 6. Испарение — процесс превращения жидкости в пар.
- 7. Вылетевшая молекула принимает участие в беспорядочном тепловом движении газа.
- 8. Конденсация — процесс превращения пара в жидкость.
- 9. Чем выше температура жидкости, тем быстрее движутся молекулы, приобретая достаточную кинетическую энергию для вылета из жидкости.
- 10. При испарении жидкость покидают более быстрые молекулы, поэтому средняя кинетическая энергия оставшихся молекул жидкости уменьшается. Mahlum
- 16. В первый момент, после того как жидкость нальют в сосуд и закроют его, жидкость будет испаряться
- 17. 1022
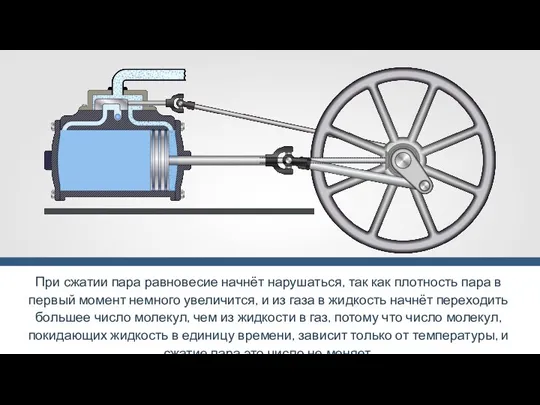
- 18. Пар, находящийся в динамическом равновесии со своей жидкостью, называют насыщенным паром. Это значит, что в данном
- 20. Концентрация молекул насыщенного пара при постоянной температуре не зависит от его объёма.
- 21. Давление пропорционально концентрации молекул.
- 22. Давление насыщенного пара — давление пара, при котором жидкость находится в равновесии со своим паром.
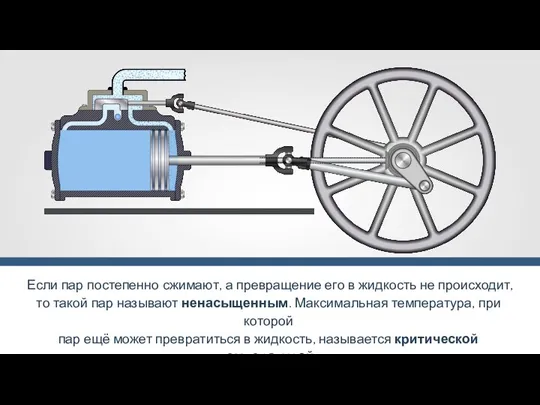
- 24. Состояние вещества при температуре выше критической называется газом; при температуре ниже критической, когда у пара есть
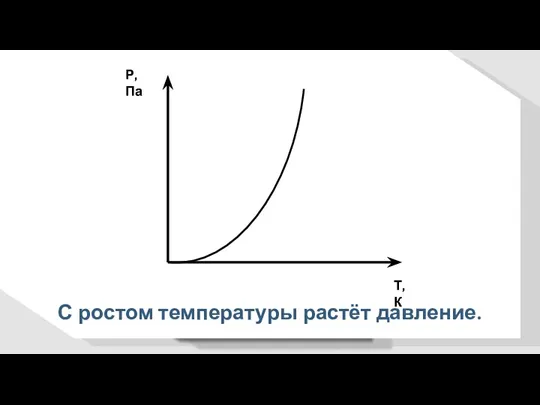
- 25. Р, Па Т, К С ростом температуры растёт давление.
- 26. При нагревании жидкости в закрытом сосуде часть жидкости превращается в пар. В результате давление насыщенного пара
- 27. При изменении температуры в закрытом сосуде меняется масса пара. Жидкость частично превращается в пар, или, напротив,
- 28. Кипение — это превращение жидкости в пар по всему объёму жидкости при постоянной температуре.
- 29. Каждая жидкость имеет свою температуру кипения. Жидкость кипит тогда, когда давление её насыщенного пара равно внешнему
- 30. Температура кипения — это температура жидкости, при которой давление её насыщенного пара равно внешнему давлению или
- 31. Особенности жидкости при кипении: – при постоянном внешнем давлении температура жидкости постоянна; – с повышением внешнего
- 33. Примеры изменения температуры кипения: – кипение воды при нормальном атмосферном давлении 760 мм рт.ст.; – кипение
- 34. Вода занимает около 70,8% поверхности земного шара. Живые организмы содержат от 50 до 99,7% воды. В
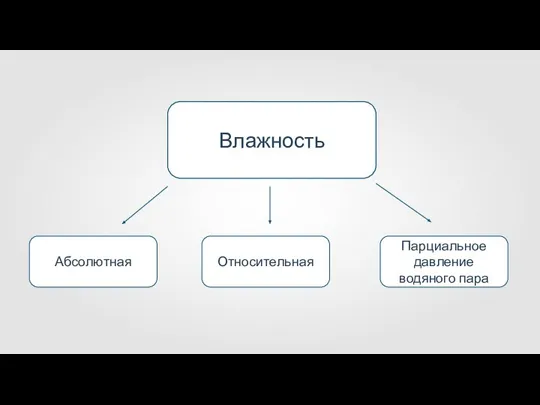
- 35. Влажность
- 36. Плотность водяного пара в воздухе измеряется в килограммах на метр кубический (кг/м³), т.е. показывает, сколько граммов
- 37. Чем выше температура воздуха, тем больше в нём может быть пара. +20 °С — 1 м3
- 38. Степень насыщения водяного пара зависит от: – количества водяных паров; – давления; – температуры.
- 40. Остров Сахалин Vihljun
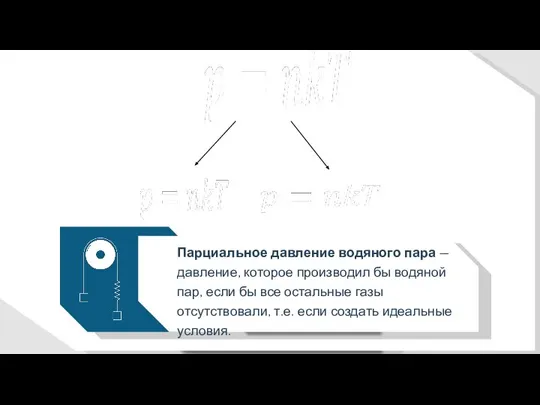
- 42. Парциальное давление водяного пара — давление, которое производил бы водяной пар, если бы все остальные газы
- 43. Атмосферное давление определяется суммой парциальных давлений компонент сухого воздуха и водяного пара.
- 44. NepGrower Относительная влажность — это величина, показывающая, насколько водяной пар при данной температуре близок к насыщению.
- 45. Относительной влажностью воздуха (φ) называют отношение парциального давления (р) водяного пара, содержащегося в воздухе при данной
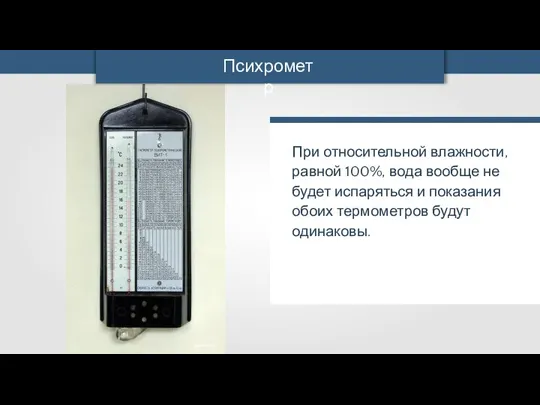
- 46. mpakmopucm mpakmopucm Психрометр
- 47. Schekinov Alexey Victorovich
- 48. mpakmopucm При относительной влажности, равной 100%, вода вообще не будет испаряться и показания обоих термометров будут
- 49. Точка росы — это температура, при которой пар, находящийся в воздухе становится насыщенным.
- 50. Точка росы характеризует влажность воздуха – выпадение росы под утро; – запотевание холодного стекла, если на
- 53. От влажности зависит интенсивность испарения влаги с поверхности кожи человека. Испарение влаги имеет большое значение для
- 57. Твёрдые тела – тела, которые со временем не меняют своей формы и объёма Твёрдые тела делятся
- 58. Кристаллы – твёрдые тела, у которых наблюдается упорядоченное расположение атомов или молекул Кристаллы делятся на два
- 59. Полиморфизм – свойство твёрдых тел существовать в состоянии с различной кристаллической решёткой. Например, алмаз и графит
- 60. Анизотропия – зависимость физических свойств кристалла от направления. То есть кристаллическая структура не симметрична, и существует
- 62. Скачать презентацию
















































 Работа и потенциал электростатического поля. Лекция 2
Работа и потенциал электростатического поля. Лекция 2 Возможности расчетов на сейсмические воздействия в программном комплексе ЛИРА 10.8
Возможности расчетов на сейсмические воздействия в программном комплексе ЛИРА 10.8 Источники света. Распространение света
Источники света. Распространение света Адронный коллайдер
Адронный коллайдер Кварки
Кварки ТОО VIVA-Мастер – авторизованный сервисный центр Pentax Medical в Казахстане
ТОО VIVA-Мастер – авторизованный сервисный центр Pentax Medical в Казахстане Методы определения твердости
Методы определения твердости Система путевого управления самолётом
Система путевого управления самолётом Строение и свойства веществ
Строение и свойства веществ Шум, вібрація. Електромагнітні поля різних частот як фактори навколишнього середовища, їх вплив на здоров’я, шляхи профілактики
Шум, вібрація. Електромагнітні поля різних частот як фактори навколишнього середовища, їх вплив на здоров’я, шляхи профілактики Общий вид стационарной ЭТЛ
Общий вид стационарной ЭТЛ Закон всемирного тяготения
Закон всемирного тяготения Презентация на тему Модели атомов. Опыт Резерфорда
Презентация на тему Модели атомов. Опыт Резерфорда  Осознание учеником роли эксперимента в физике
Осознание учеником роли эксперимента в физике Уравнение плоской гармонической волны
Уравнение плоской гармонической волны Зависимость сопротивления от температуры сверхпроводимость
Зависимость сопротивления от температуры сверхпроводимость Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения
Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения teploperedacha-_8_kl
teploperedacha-_8_kl Динамика. Экзаменационные задачи 1-14
Динамика. Экзаменационные задачи 1-14 Разъемные соединения
Разъемные соединения Законы Ньютона
Законы Ньютона Магнитопорошковая дефектоскопия (МПД)
Магнитопорошковая дефектоскопия (МПД) Инжекторный ДВС
Инжекторный ДВС Ядерный реактор
Ядерный реактор Задачи по технической механике. Сложение ускорений
Задачи по технической механике. Сложение ускорений Звуковые волны
Звуковые волны Презентация на тему Теория относительности и Альберт Эйнштейн
Презентация на тему Теория относительности и Альберт Эйнштейн  Скорость выполнения работы. Формула работы
Скорость выполнения работы. Формула работы