Содержание
- 2. I NUMERI QUANTICI Il numero quantico principale n indica il livello energetico e la dimensione degli
- 3. NUMERO QUANTICO SECONDARIO Nel 1915 Sommerfeld ampliò il modello di Bohr aggiungendo altre orbite quantizzate ellittiche.
- 4. NUMERO QUANTICO SECONDARIO Per l = 1 l'orbitale è a due lobi (orbitale p). Il nucleo
- 5. NUMERO QUANTICO SECONDARIO Per l = 2 l'orbitale è a quattro lobi (orbitale d). Il nucleo
- 6. NUMERO QUANTICO MAGNETICO Il numero quantico magnetico m, indica il numero di orientazioni di un dato
- 7. NUMERO QUANTICO DI SPIN Nel novembre del 1925 due fisici olandesi, G.E. Uhlenbeck e S.A. Goudsmit,
- 8. NUMERI QUANTICI (Riepilogo )
- 10. Скачать презентацию
Слайд 2I NUMERI QUANTICI
Il numero quantico principale n indica il livello energetico e la dimensione
I NUMERI QUANTICI
Il numero quantico principale n indica il livello energetico e la dimensione

Il numero quantico principale può assumere soltanto i valori interi 1, 2, 3, 4, 5, 6, 7.
Quando il valore del numero quantico principale cresce, gli orbitali diventano più grandi, la loro energia aumenta e gli elettroni sono più lontani dal nucleo.
Tutti gli orbitali che sono caratterizzati dallo stesso valore di n appartengono allo stesso livello di energia.
Il numero massimo di elettroni presenti nel livello n è pari a 2·n2. In realtà questo è valido per i primi 4 livelli. Quindi:
nel primo livello di energia (n = 1) ci potranno essere al massimo 2·12 = 2 elettroni
nel secondo livello di energia (n = 2) ci potranno essere al massimo 2·22 = 8 elettroni
nel terzo livello di energia (n = 3) ci potranno essere al massimo 2·32 = 18 elettroni
nel quarto livello di energia (n = 4) ci potranno essere al massimo 2·42 = 32 elettroni
NUMERO QUANTICO PRINCIPALE
n
4
3
2
1
5
6
7
Energia crescente
N
M
L
K
O
P
Q
2
8
18
32
21
9
2
Numero massimo di elettroni per livello = 2·n2
Слайд 3NUMERO QUANTICO SECONDARIO
Nel 1915 Sommerfeld ampliò il modello di Bohr aggiungendo altre
NUMERO QUANTICO SECONDARIO
Nel 1915 Sommerfeld ampliò il modello di Bohr aggiungendo altre
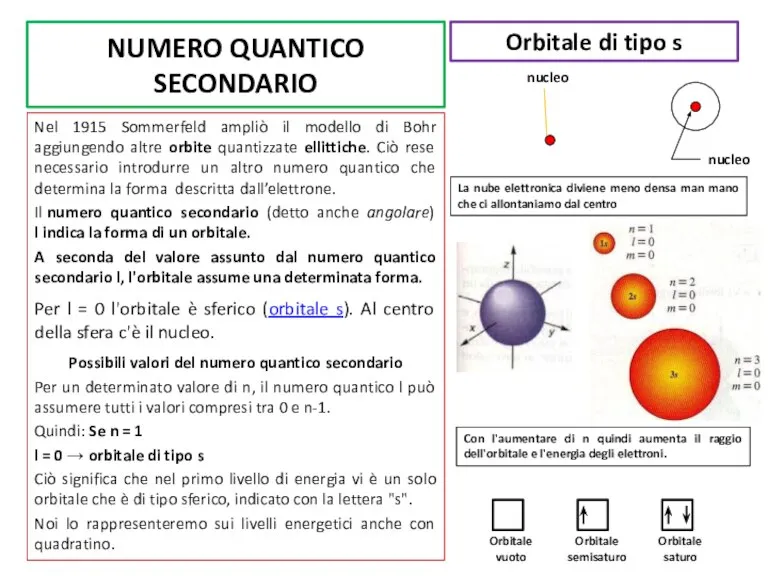
Il numero quantico secondario (detto anche angolare) l indica la forma di un orbitale.
A seconda del valore assunto dal numero quantico secondario l, l'orbitale assume una determinata forma.
Per l = 0 l'orbitale è sferico (orbitale s). Al centro della sfera c'è il nucleo.
Possibili valori del numero quantico secondario
Per un determinato valore di n, il numero quantico l può assumere tutti i valori compresi tra 0 e n-1.
Quindi: Se n = 1
l = 0 → orbitale di tipo s
Ciò significa che nel primo livello di energia vi è un solo orbitale che è di tipo sferico, indicato con la lettera "s".
Noi lo rappresenteremo sui livelli energetici anche con quadratino.
Orbitale di tipo s
Con l'aumentare di n quindi aumenta il raggio dell'orbitale e l'energia degli elettroni.
La nube elettronica diviene meno densa man mano che ci allontaniamo dal centro
Слайд 4NUMERO QUANTICO SECONDARIO
Per l = 1 l'orbitale è a due lobi (orbitale
NUMERO QUANTICO SECONDARIO
Per l = 1 l'orbitale è a due lobi (orbitale
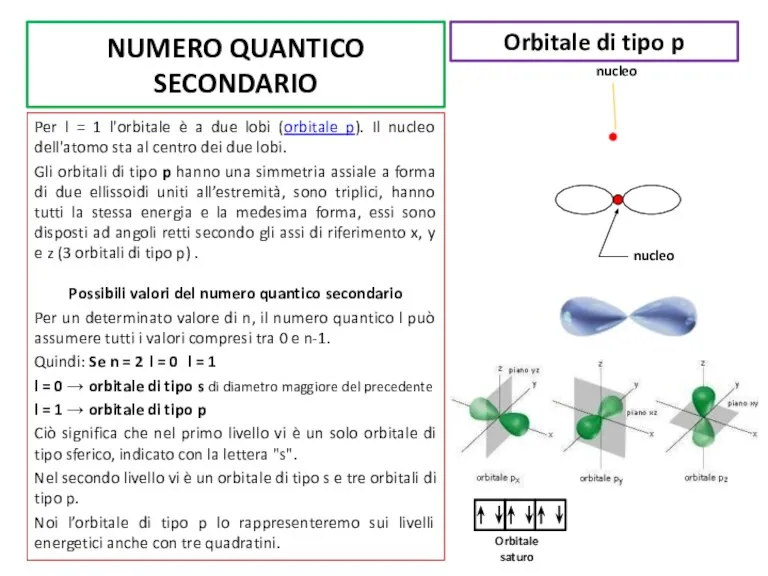
Gli orbitali di tipo p hanno una simmetria assiale a forma di due ellissoidi uniti all’estremità, sono triplici, hanno tutti la stessa energia e la medesima forma, essi sono disposti ad angoli retti secondo gli assi di riferimento x, y e z (3 orbitali di tipo p) .
Possibili valori del numero quantico secondario
Per un determinato valore di n, il numero quantico l può assumere tutti i valori compresi tra 0 e n-1.
Quindi: Se n = 2 l = 0 l = 1
l = 0 → orbitale di tipo s di diametro maggiore del precedente
l = 1 → orbitale di tipo p
Ciò significa che nel primo livello vi è un solo orbitale di tipo sferico, indicato con la lettera "s".
Nel secondo livello vi è un orbitale di tipo s e tre orbitali di tipo p.
Noi l’orbitale di tipo p lo rappresenteremo sui livelli energetici anche con tre quadratini.
Orbitale di tipo p
Слайд 5NUMERO QUANTICO SECONDARIO
Per l = 2 l'orbitale è a quattro lobi (orbitale
NUMERO QUANTICO SECONDARIO
Per l = 2 l'orbitale è a quattro lobi (orbitale
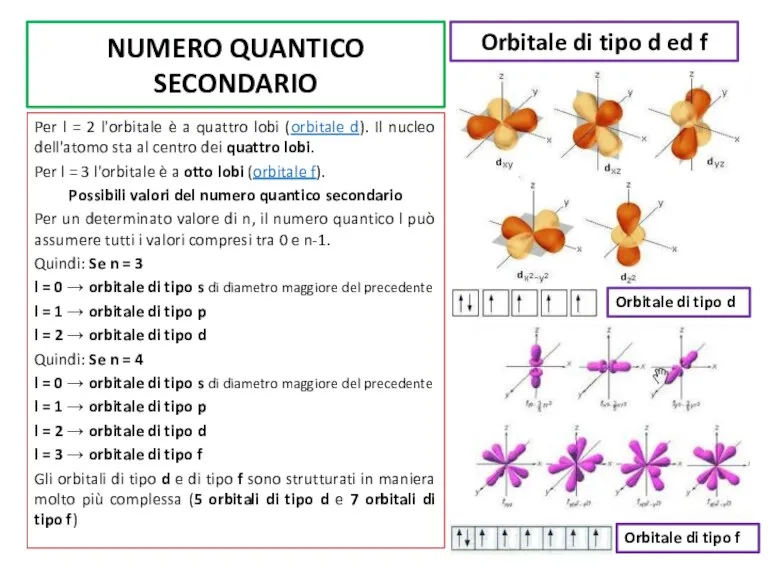
Per l = 3 l'orbitale è a otto lobi (orbitale f).
Possibili valori del numero quantico secondario
Per un determinato valore di n, il numero quantico l può assumere tutti i valori compresi tra 0 e n-1.
Quindi: Se n = 3
l = 0 → orbitale di tipo s di diametro maggiore del precedente
l = 1 → orbitale di tipo p
l = 2 → orbitale di tipo d
Quindi: Se n = 4
l = 0 → orbitale di tipo s di diametro maggiore del precedente
l = 1 → orbitale di tipo p
l = 2 → orbitale di tipo d
l = 3 → orbitale di tipo f
Gli orbitali di tipo d e di tipo f sono strutturati in maniera molto più complessa (5 orbitali di tipo d e 7 orbitali di tipo f)
Orbitale di tipo d
Orbitale di tipo d ed f
Orbitale di tipo f
Слайд 6NUMERO QUANTICO MAGNETICO
Il numero quantico magnetico m, indica il numero di orientazioni
NUMERO QUANTICO MAGNETICO
Il numero quantico magnetico m, indica il numero di orientazioni
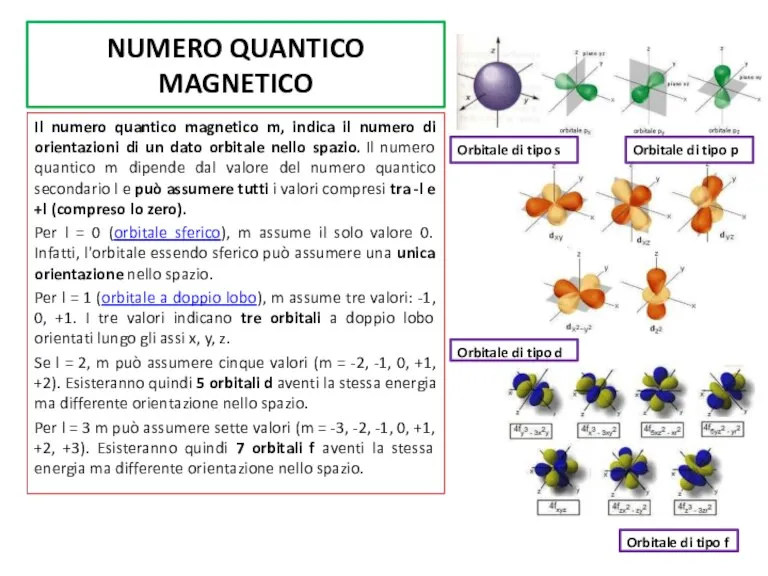
Per l = 0 (orbitale sferico), m assume il solo valore 0. Infatti, l'orbitale essendo sferico può assumere una unica orientazione nello spazio.
Per l = 1 (orbitale a doppio lobo), m assume tre valori: -1, 0, +1. I tre valori indicano tre orbitali a doppio lobo orientati lungo gli assi x, y, z.
Se l = 2, m può assumere cinque valori (m = -2, -1, 0, +1, +2). Esisteranno quindi 5 orbitali d aventi la stessa energia ma differente orientazione nello spazio.
Per l = 3 m può assumere sette valori (m = -3, -2, -1, 0, +1, +2, +3). Esisteranno quindi 7 orbitali f aventi la stessa energia ma differente orientazione nello spazio.
Orbitale di tipo d
Orbitale di tipo f
Orbitale di tipo p
Orbitale di tipo s
Слайд 7NUMERO QUANTICO DI SPIN
Nel novembre del 1925 due fisici olandesi, G.E. Uhlenbeck
NUMERO QUANTICO DI SPIN
Nel novembre del 1925 due fisici olandesi, G.E. Uhlenbeck

Inoltre, poiché l'elettrone possiede anche una carica elettrica, il suo movimento a trottola gli conferiva un'altra proprietà, quella cioè di una minuscola calamita con polo nord e polo sud.
Per descrivere l'orientazione del vettore di spin dell'elettrone, fu definito quindi un quarto numero quantico che, simboleggiato con ms, prese il nome di numero quantico di spin e può assumere soltanto due valori:
ms = + ½ e ms = - ½
Ciascun valore corrisponde a una rotazione in senso orario o in senso antiorario dell’elettrone attorno al proprio asse. Se ruota in senso orario si indica con una freccia verso l’alto (spin su) [ ↑ ], se ruota in senso antiorario la freccia sarà rivolta verso il basso (spin giù) [ ↓ ].
Слайд 8NUMERI QUANTICI (Riepilogo )
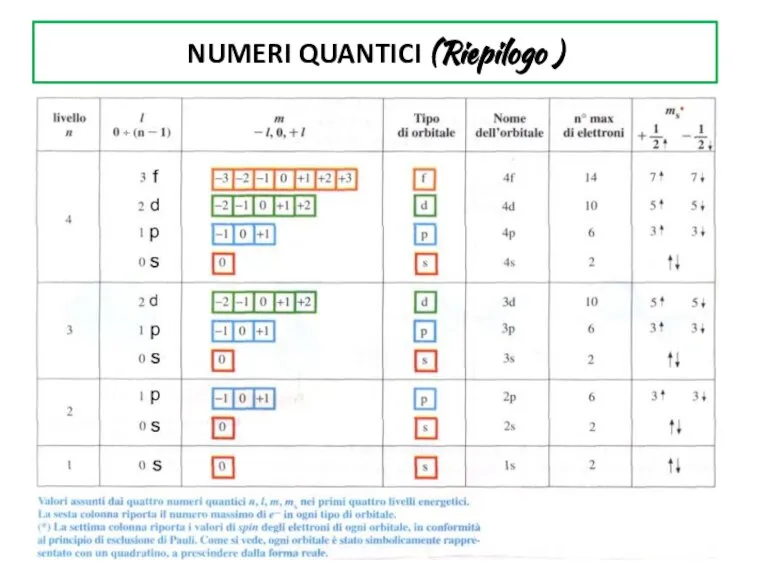
NUMERI QUANTICI (Riepilogo )
 Введение. (7 класс). Тест
Введение. (7 класс). Тест Презентация на тему Световые явления
Презентация на тему Световые явления  Механическая мощность
Механическая мощность Тепловые электрические станции
Тепловые электрические станции Закон сохранения полной механической энергии
Закон сохранения полной механической энергии Датчика изгиба (Роборука)
Датчика изгиба (Роборука) Электростатика. Сила Кулона
Электростатика. Сила Кулона Методическое пособие Мотошины, Колеса Даром
Методическое пособие Мотошины, Колеса Даром Трансформатор в линейном режиме
Трансформатор в линейном режиме Энергия магнитного поля
Энергия магнитного поля Радиальное биение
Радиальное биение Система питания двигателей автомобиля от газобаллонных установок
Система питания двигателей автомобиля от газобаллонных установок Косой изгиб. Построение эпюр нормальных напряжений по сечению при косом изгибе и внецентренном сжатии
Косой изгиб. Построение эпюр нормальных напряжений по сечению при косом изгибе и внецентренном сжатии Ворот-разновидность рычага
Ворот-разновидность рычага Явление фотоэффекта
Явление фотоэффекта Презентация на тему Электрическая цепь и её составные части
Презентация на тему Электрическая цепь и её составные части  Історія Електричної Лампи. Шаблон
Історія Електричної Лампи. Шаблон 21 061
21 061 ТО и ТР системы питания автомобилей
ТО и ТР системы питания автомобилей Количество вещества. Моль
Количество вещества. Моль Газовые законы
Газовые законы Энергия. Потенциальная энергия
Энергия. Потенциальная энергия Основы молекулярной физики
Основы молекулярной физики Презентация на тему Электрическое сопротивление проводника. Удельное сопротивление
Презентация на тему Электрическое сопротивление проводника. Удельное сопротивление  Электрические явления 8 класс
Электрические явления 8 класс Давление. Единицы давления
Давление. Единицы давления Демонстрационный вариант контрольных измерительных материалов для проведения в 2014 году государственной аттестации по физике
Демонстрационный вариант контрольных измерительных материалов для проведения в 2014 году государственной аттестации по физике Задачи Закон всемирного тяготения с решениями
Задачи Закон всемирного тяготения с решениями