Слайд 26. Микроволновая химия-1
Возникла на стыке физики и химии. Рассматривает химические превращения под

воздействием СВЧ-излучения.
СВЧ излучение способно в десятки и сотни раз увеличивать скорость химических реакций, проводить быстрый объемный нагрев жидких и твердых сред.
В 2011 г. решением Правительства РФ утверждена технологическая платформа «СВЧ-ТЕХНОЛОГИИ».
Слайд 3Задачи технологической платформы «СВЧ-технологии»
Определение перспективных направлений развития СВЧ технологий и продуктов, обеспечивающих

существенное улучшение качественных характеристик СВЧ продукции и мировое лидерство российской продукции и технологий;
Разработка приборов и оборудования для СВЧ технологий в соответствии с требованиями потребителей.
Слайд 4Микроволновое излучение
Электромагнитные колебания с частотой примерно от 300 МГц до 300 ГГц;
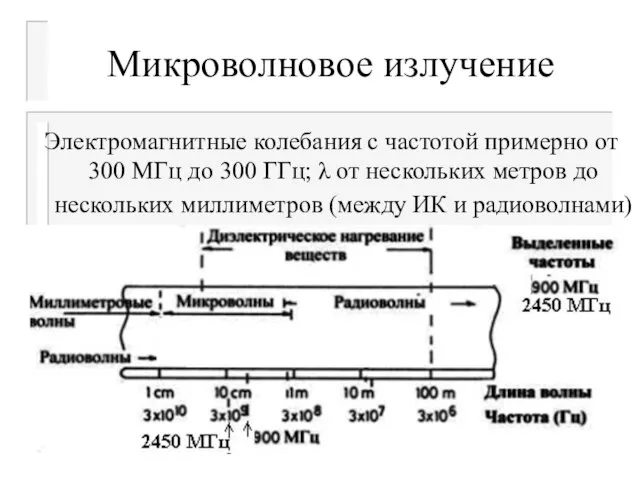
λ от нескольких метров до нескольких миллиметров (между ИК и радиоволнами)
Слайд 5Микроволновое излучение
Не является ионизирующим. Следовательно, не может привести к ионизации атома, поскольку

энергия кванта микроволнового излучения составляет ~ 1⋅10–4 – 0,1 кДж/моль.
В 1946 году было открыто тепловое воздействие микроволн на пищевые продукты, а в 1950 – был получен первый патент на изобретение бытовой микроволновой печи.
Слайд 6Микроволновое излучение
Для использования электромагнитного излучения в промышленной и быту были регламентированы, в

частности, следующие частоты: 2450, 2375 и 915 МГц. В быту микроволновые печи работают на частоте 2450 МГц (длина волны 12,25 см).
Микроволновое излучение нашло широкое применение физике, химии и химической технологии, медицине и в других областях науки и техники.
Слайд 76.2. Взаимодействие микроволнового излучения с веществом
Микроволновое (МВ) излучение может взаимодействовать с

газами, жидкостями и твердыми веществами. Для химической практики наиболее интересно взаимодействие МВ-излучения с жидкими и твердыми веществами. При взаимодействии (МВ) излучения с твердыми веществами может происходить его отражение, поглощение или прохождение через объем образца без поглощения.
Слайд 8Три группы материалов
По характеру взаимодействия с МВ-излучением все твердые материалы разделяют на

три группы:
1. Металлы, гладкая поверхность которых полностью отражает микроволны; при этом нагревания металла не наблюдается, так как практически отсутствуют потери энергии МВ-излучения в его объем – волноводы служат для передачи СВЧ.
Слайд 9Три группы материалов
2. Диэлектрики без потерь, которые пропускают микроволновое излучение через

свой объем почти без изменений (например, фарфор, различные стекла, полиэтилен, полистирол, тефлон и т.д.)
3. Диэлектрики с потерями, прохождение МВ-излучения через объем которых сопровождается нагреванием образца.
Слайд 10Типы поляризации вещества
При наложении внешнего поля на неполярную молекулу возникают силы, противоположно
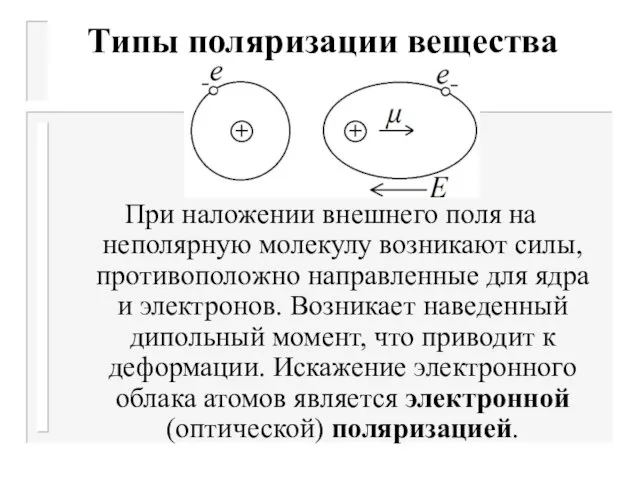
направленные для ядра и электронов. Возникает наведенный дипольный момент, что приводит к деформации. Искажение электронного облака атомов является электронной (оптической) поляризацией.
Слайд 11Типы поляризации вещества
Ионная поляризация возникает в ионных молекулах. Электростатические силы ионной решетки
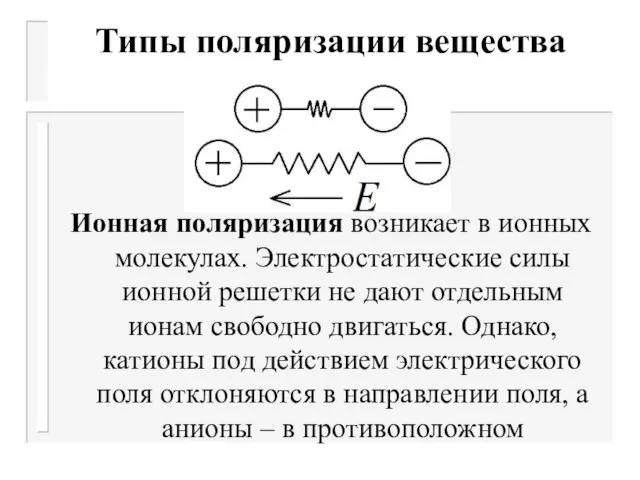
не дают отдельным ионам свободно двигаться. Однако, катионы под действием электрического поля отклоняются в направлении поля, а анионы – в противоположном
Слайд 12Электронная и ионная поляризации
На традиционно используемых частотах радиодиапазона смещение частиц при электронной

и ионной поляризации происходит практически без инерционно, поэтому выделения тепла в диэлектрике не происходит.
Слайд 13Дипольная поляризация
При введении полярной молекулы в электрическое поле происходит ее переориентация. Диполи
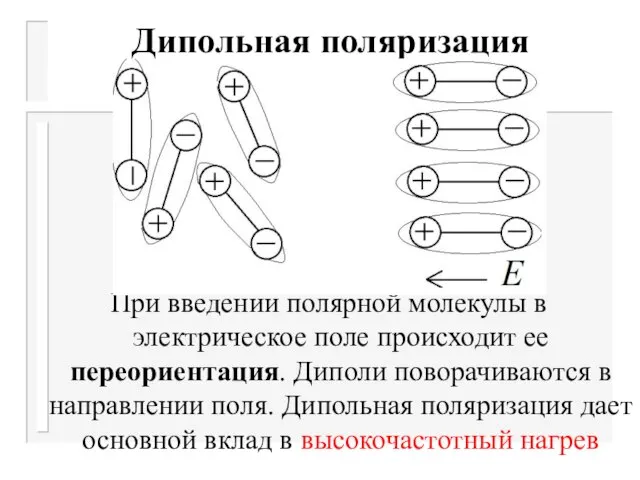
поворачиваются в направлении поля. Дипольная поляризация дает основной вклад в высокочастотный нагрев
Слайд 14Дипольная поляризация
В случае дипольной поляризации перемещение частиц осуществляется с трением, на преодоление

которого расходуется энергия, которая и вызывает нагрев диэлектрика .
При наложении внешнего поля дипольные молекулы изменяют свою ориентацию в соответствии с направлением поля. При этом вначале следует ориентация диполей, затем поле изменяет свою направленность и происходит разупорядочивание и переориентация дипольных молекул.
Слайд 15Дипольная поляризация
На частоте, например, 2450 МГц ориентация и последующее разупорядочение диполей и

их переориентация происходят несколько миллиардов раз за одну секунду. В микроволновом поле диполи уже не успевают следовать за изменением поля и возникает поглощение микроволновой энергии. В результате вещество быстро нагревается. Трансформация СВЧ-энергии поля в тепловую происходит за счет выделения теплоты поляризации «связанных зарядов» в диэлектрике.
Слайд 16Основные электромагнитные характеристики вещества
Электрическая проводимость
κ – удельная электропроводность (ЭП), [См/м];
![Основные электромагнитные характеристики вещества Электрическая проводимость κ – удельная электропроводность (ЭП), [См/м];](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/861099/slide-15.jpg)
1 сименс=1/Ом
R – сопротивление, [Ом]; R = ρ (L/S)
ρ – удельное сопротивление, [Ом∙м]
κ* = κ′+iκ″– комплексная ЭП; κ*= i ωεоε*, i=
κ′–активная, κ″–реактивная составляющие ЭП
F–частота, Гц; ω=2πF – круговая частота, рад/с
κ∞ – предельная высокочастотная (ВЧ) ЭП
Слайд 17Основные электромагнитные характеристики вещества
Диэлектрическая проницаемость
ε–относительная диэлектрическая проницаемость (ДП);
εо = 8,854·10–12 Ф/м

– абсолютная ДП вакуума,
ε* = ε′– i ε″ – комплексная ДП;
ε′ – активная, ε″ – реактивная составляющие ДП (коэффициент диэлектрических потерь)
tgδ = ε″/ε′ – тангенс потерь, εs – статическая,
ε∞ – оптическая ДП, τ – время дипольной диэлектрической релаксации
Слайд 18Диэлектрическая проницаемость
Относительная диэлектрическая проницаемость (ДП) вещества показывает во сколько раз сила взаимодействия

между двумя зарядами в этом веществе меньше, чем в вакууме. Численно ДП ε равна отношению электрической ёмкости конденсатора, заполненного этим веществом С к ёмкости конденсатора в вакууме Со:
ε = С/Со.
Абсолютная ДП вещества εа равна εа = ε·εо .
εо– абсолютная ДП вакуума (εо = 8,854·10–12 Ф/м).
Слайд 19Диэлектрическая проницаемость
ДП газов близка к 1 (ε воздуха = 1,0006); твердых веществ

5 – 10 (NaCl – 6, стекла 5 – 20 в зависимости от состава), сегнетоэлектрики – BaTiO3 ε >1000).
Неполярные растворители: ε~n2 (2 – 4).
Полярные растворители: ацетон – 20,
метанол – 32, вода – 80, формамид – 110,
N-метилформамид – 190.
Слайд 20Дипольная релаксация
Поляризация диэлектрика в переменном электрическом поле зависит от частоты.
Частотная зависимость электромагнитных

свойств любого вещества обычно описывается в терминах комплексной диэлектрической проницаемости (ДП)
ε* = ε′ – jε″.
ε′ – активная, ε″ – реактивная составляющие комплексной ДП
Слайд 21Дипольная релаксация
При низких частотах электромагнитного поля ДП полярного растворителя сохраняет свое постоянное

значение εs, которое называется статической ДП.
При повышении частоты дипольные молекулы растворителя не успевают следовать за изменением внешнего поля.
Слайд 22Дипольная релаксация
Активная составляющая ДП полярного диэлектрика ε′ уменьшается, достигая в пределе величины
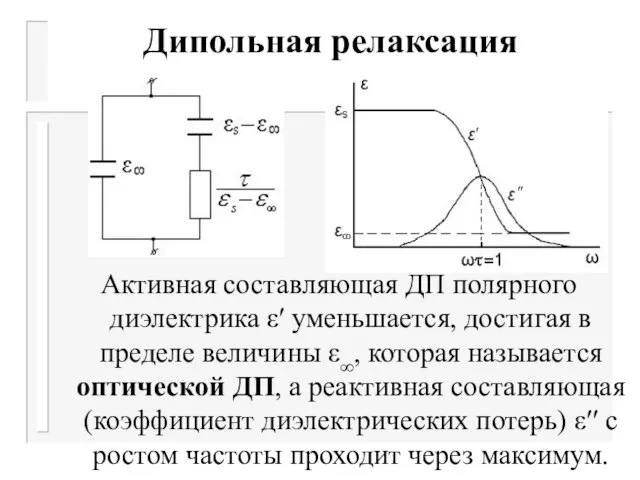
ε∞, которая называется оптической ДП, а реактивная составляющая (коэффициент диэлектрических потерь) ε′′ с ростом частоты проходит через максимум.
Слайд 23Дипольная релаксация
Для воды при комнатной температуре εs = 80; ε∞=5,0. Для спиртов

εs меньше εs(Н2О);
ε∞(спиртов)=2,0.
Коэффициент диэлектрических потерь ε′′ достигает максимального значения при условии ωτ =1 (ω = 2 πF).
Вода: τ=8,3*10–12 с. ω=1/τ=1,20*1011,
Частота F=1,20*1011/6,28=19,1 ГГц.
Слайд 24Теория дисперсии ДП Дебая
Зависимость ДП от частоты полярных диэлектриков описал П. Дебай:
,
в

уравнениях Дебая ω – круговая частота
(ω = 2 πF), τ – время дипольной релаксации (время, в течении которого поляризация в веществе после выключения поля уменьшается в е раз; е=2,71828 ).
Слайд 25Диэлектрические потери
Максимум коэффициента диэлектрических потерь ε′′ имеет место при условии ωτ =

1, т.е. когда круговая частота равна обратному времени дипольной диэлектрической релаксации. Тангенс диэлектрических потерь tgδ представляет собой отношение токов проводимости IR к токам смещения Ic:
tgδ=IR/Ic=κ/ωεεо= ε′′/ε′
Слайд 26Тангенс диэлектрических потерь
tgδ = ε′′/ε′. Вода: τ=8,3*10–12 с.
ε′′(max) на частоте
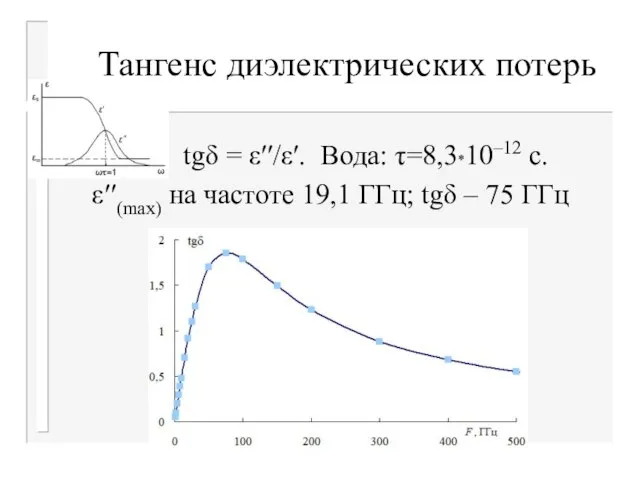
19,1 ГГц; tgδ – 75 ГГц
Слайд 27Тангенс диэлектрических потерь
tgδ = ε′′/ε′. Этанол: τ=160*10–12 с.
ε′′(max) на частоте
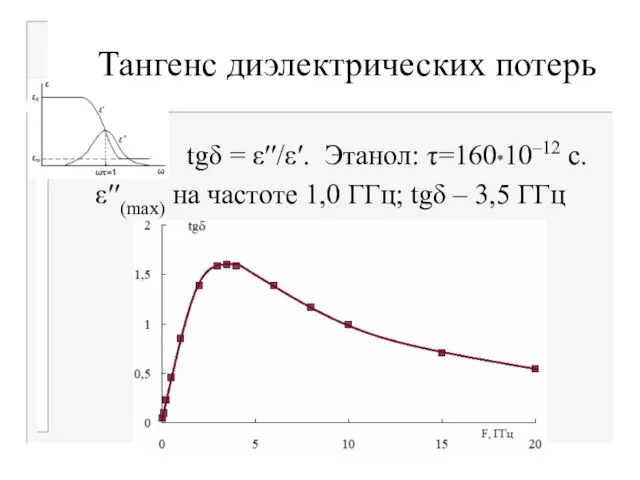
1,0 ГГц; tgδ – 3,5 ГГц
Слайд 28Тангенс диэлектрических потерь
При переходе от этанола (τ=160 пс) к метанолу (τ=50 пс),
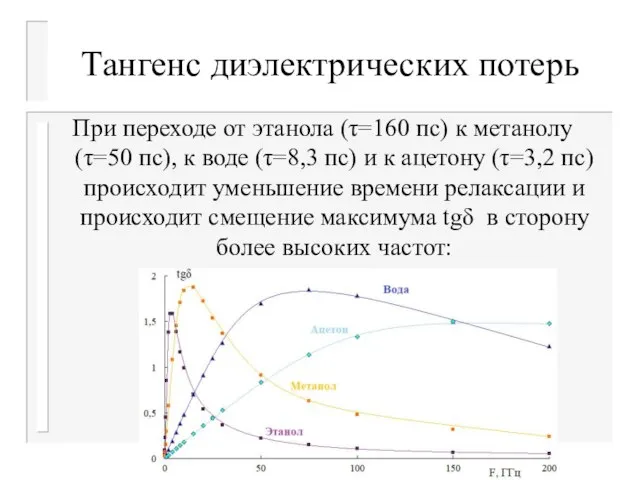
к воде (τ=8,3 пс) и к ацетону (τ=3,2 пс) происходит уменьшение времени релаксации и происходит смещение максимума tgδ в сторону более высоких частот:
Слайд 29Тангенс диэлектрических потерь
Зависимость частоты F, при которой tgδ достигает максимума(max) от скорости
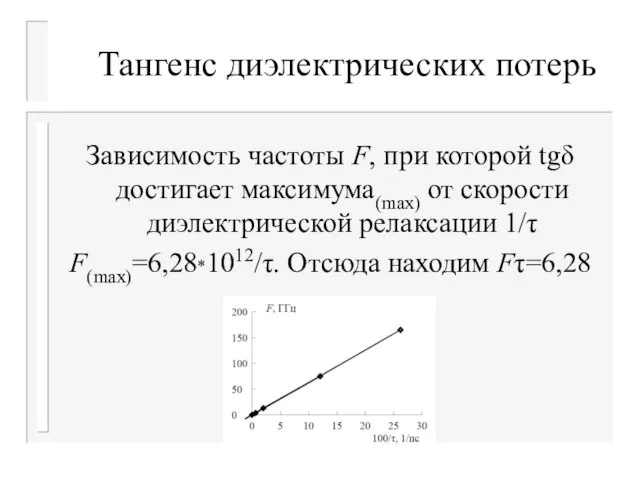
диэлектрической релаксации 1/τ
F(max)=6,28*1012/τ. Отсюда находим Fτ=6,28
Слайд 30ε′′ Тангенс диэлектрических потерь
Зависимость ε′′ и tgδ от частоты:
ε′′ достигает максимального

значения при условии ωτ=1 или Fτ =1/2π.
tgδ достигает максимального значения при условии Fτ =2π.
Слайд 31Круговая диаграмма дипольной диэлектрической релаксации
Описываемая уравнениями Дебая дисперсия может быть также представлена

в виде круговых диаграмм (диаграмм Коула-Коула). Объединяя выражения Дебая получаем уравнение окружности:
Слайд 32
Диаграмма Коула представляет собой полуокружность с радиусом (εs-ε∞)/2 и с центром на

оси абсцисс на расстоянии (εs+ε∞)/2. При ω → 0 диаграмма пересекает ось абсцисс при значении ДП, равном εs. Если ω→∞, кривая отсекает на оси абсцисс значение ε∞. Повышение частоты приводит к перемещению точки на круговой диаграмме против часовой стрелки.
Слайд 33Статическая ДП
Диэлектрическая проницаемость вещества εs зависит от его природы, температуры, а в

растворах также от природы растворителя и концентрации.
Аномально высокое значение ДП воды и некоторых других протонных полярных жидкостей, связано с их строением, в частности, с поляризацией системы водородных связей
Слайд 34Время дипольной релаксации
Если ДП полярного растворителя можно условно назвать структурной его характеристикой,

то время дипольной релаксации является кинетической характеристикой. Время дипольной диэлектрической релаксации τ характеризует ориентационную подвижность молекул растворителя (чем меньше τ, тем более подвижны его молекулы).
Слайд 35Расчет по уравнениям Дебая
Используя уравнения Дебая рассчитаем активную и реактивную составляющие

комплексной ДП воды и метанола и сравним значения тангенса потерь растворителей на промышленной частоте 2450 МГц. Тангенс потерь есть отношение токов проводимости к токам смещения (tgδ= ε″/ε′).
Вода: εs=78,3; τ = 8,3·10-12 с
Метанол: εs=32,6; τ = 50,2·10-12 с
Слайд 36Расчет по уравнениям Дебая; F=2450 МГц (λ=12,2 см)
Вода. εs=78,3; τ = 8,3·10-12

с
ω=6,28·2450·106=1,54·1010 .
ωτ=1,54·1010 ·8,3·10-12 =0,128. (ωτ)2=0,0164.
ε′=5 + (78,3 – 5 )/(1+ 0,0164)=5+72,1=77,1. ε″ = 72,1·ωτ=9,23.
tgδ= ε″/ε′=9,23:77,1= 0,12.














![Основные электромагнитные характеристики вещества Электрическая проводимость κ – удельная электропроводность (ЭП), [См/м];](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/861099/slide-15.jpg)




















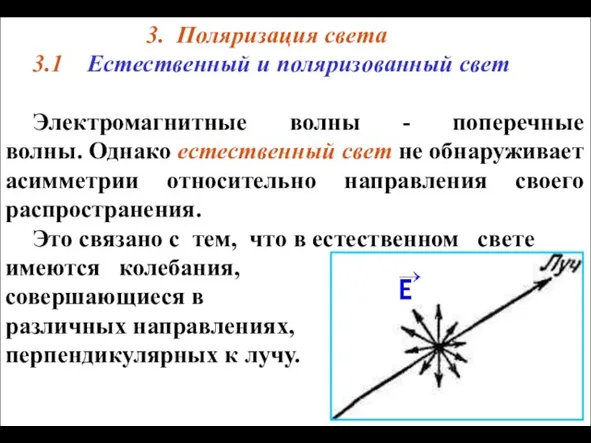 Поляризация света
Поляризация света Кинематика. Операции с векторами
Кинематика. Операции с векторами 4 (1)
4 (1) Разработка технологического процесса сборки головки блока цилиндров автомобиля ВАЗ 21214. Расчет экономических показателей
Разработка технологического процесса сборки головки блока цилиндров автомобиля ВАЗ 21214. Расчет экономических показателей Презентация на тему Снег
Презентация на тему Снег  Измерение объёма взвешиванием
Измерение объёма взвешиванием Давление в жидкости и газе
Давление в жидкости и газе Презентация на тему Механические свойства твердых тел
Презентация на тему Механические свойства твердых тел  Сказка про радио
Сказка про радио Энергия электромагнитных волн. Вектор Пойнтинга. Колебания и волны. 17
Энергия электромагнитных волн. Вектор Пойнтинга. Колебания и волны. 17 Фізика – мистецтво пізнання
Фізика – мистецтво пізнання Нанотехнологии
Нанотехнологии Строение вещества. Атомы и молекулы
Строение вещества. Атомы и молекулы Тела,вещества,частицы (1)
Тела,вещества,частицы (1) Кинематика
Кинематика Расчёт расхода электроэнергии
Расчёт расхода электроэнергии Электрическая цепь
Электрическая цепь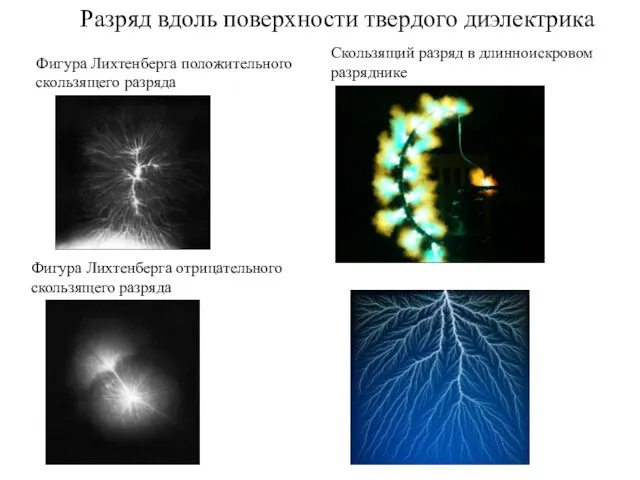 Разряд вдоль поверхности твердого диэлектрика. Лекция 4
Разряд вдоль поверхности твердого диэлектрика. Лекция 4 Апертурные искажения. Форма и функция прозрачности развертывающего элемента
Апертурные искажения. Форма и функция прозрачности развертывающего элемента Презентация на тему Электромагнитная природа света
Презентация на тему Электромагнитная природа света  Ручное солнце. Когда термоядерные реакторы станут реальностью?
Ручное солнце. Когда термоядерные реакторы станут реальностью? Оптика и основы микроскопии
Оптика и основы микроскопии Физические величины, характеризующие организм человека
Физические величины, характеризующие организм человека Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения
Применение ядерной энергии в различных отраслях. Доза радиоактивного излучения Способы измерения размеров малых тел
Способы измерения размеров малых тел Физика. Физические явления
Физика. Физические явления Спінтарископ
Спінтарископ Напряжение. Конспект урока. 8 класс
Напряжение. Конспект урока. 8 класс