Содержание
- 2. ТЕСТ Вариант 1. 1. Однородная система, состоящая из частиц растворѐнного вещества, растворителя и продуктов их взаимодействия:
- 3. Вариант 1. 1. Б 2. А 3. В 4. В 5. А, В, Г Вариант 2.
- 4. В конце XIX века шведский химик Сванте Аррениус проводил исследование различных растворов по отношению к электрическому
- 5. Электролитическая диссоциация
- 6. Цель урока: 1. Изучить понятия электролиты и неэлектролиты. 2. Рассмотреть механизм электролититической диссоциации веществ
- 7. Вещества, растворы которых проводят электрический ток, называются электролитами. Вещества, растворы которых не проводят электрический ток, называются
- 8. Электролитическая диссоциация - процесс распада молекул электролита на ионы в растворе или расплаве. 1887 г. -
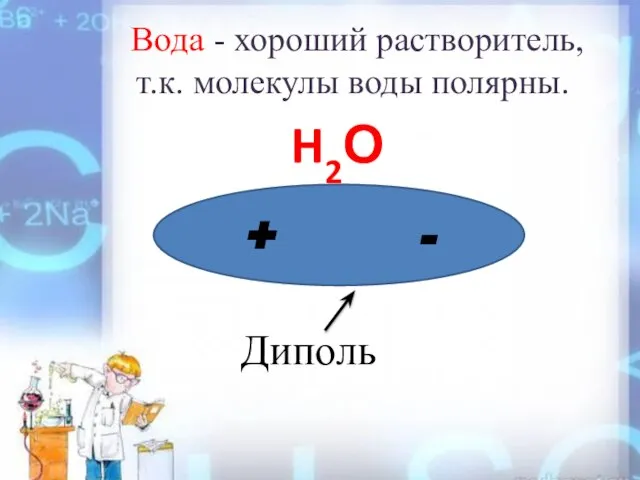
- 9. Вода - хороший растворитель, т.к. молекулы воды полярны. + - H2О Диполь
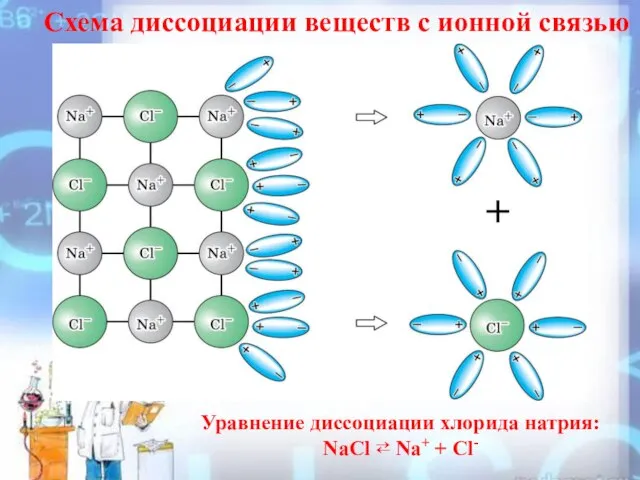
- 10. Схема диссоциации веществ с ионной связью Уравнение диссоциации хлорида натрия: NaCl ⇄ Na+ + Cl-
- 11. Степень электролитической диссоциации - это отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе.
- 12. Классификация электролитов по степени электролитической диссоциации Сильные электролиты Слабые электролиты ●все соли ●слабые кислоты ●сильные кислоты
- 13. Положения ТЭД: 1. Электролиты в растворах и расплавах диссоциируют на ионы. 2. Диссоциация – обратимый процесс.
- 14. Составьте уравнения диссоциации для веществ, являющихся сильными электролитами. В1. AgNO3, HBr, Fe(OH)2 В2. HI, PbBr2, H2SiO3
- 15. В1. AgNO3 ⇄ Ag+ + NO3- HBr ⇄ H+ + Br- В2. HI ⇄ H+ +
- 16. Домашнее задание : На 3 - параграф 35, выучить конспект в тетради. На 4 - параграф
- 17. Рефлексия
- 19. Скачать презентацию














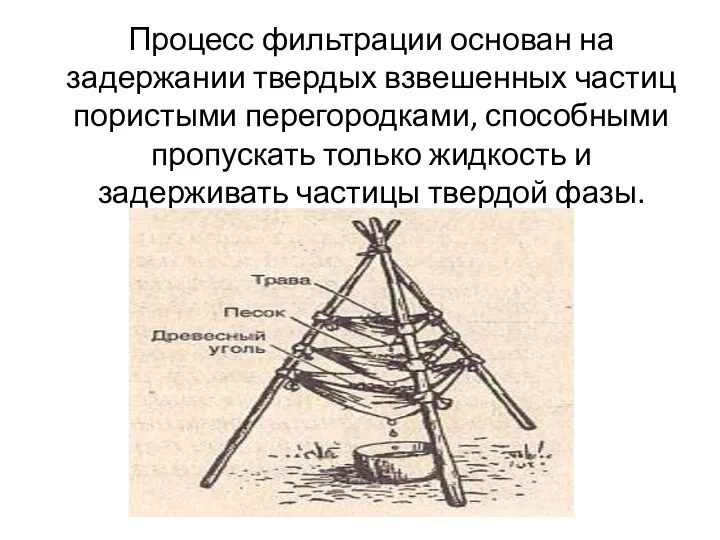 Процесс фильтрации - задержание твердых взвешенных частиц
Процесс фильтрации - задержание твердых взвешенных частиц Металлы
Металлы Применение алканов
Применение алканов Уравнения химических реакций
Уравнения химических реакций Алюминий. Строение и свойства атома
Алюминий. Строение и свойства атома Пластик: польза или вред
Пластик: польза или вред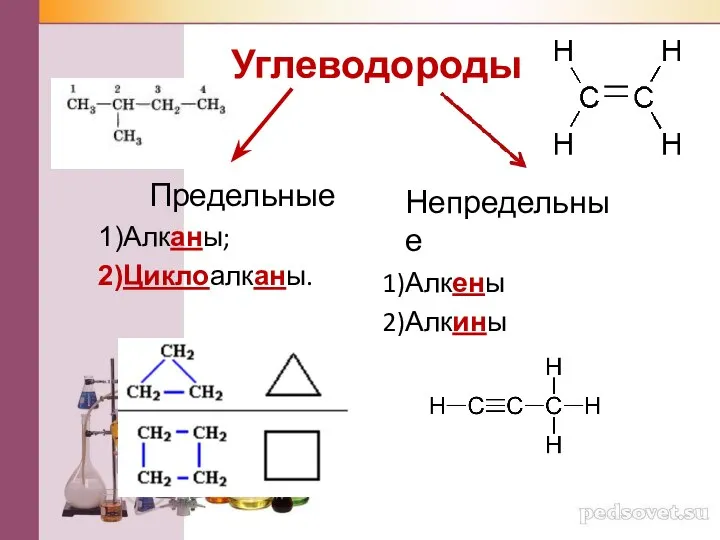 Углеводороды
Углеводороды Химическая связь и ее типы
Химическая связь и ее типы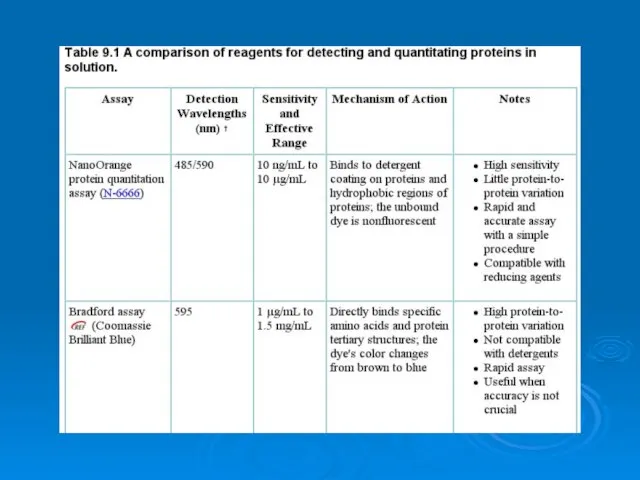 Analysis of proteins
Analysis of proteins Презентация на тему М.В. Ломоносов
Презентация на тему М.В. Ломоносов  ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ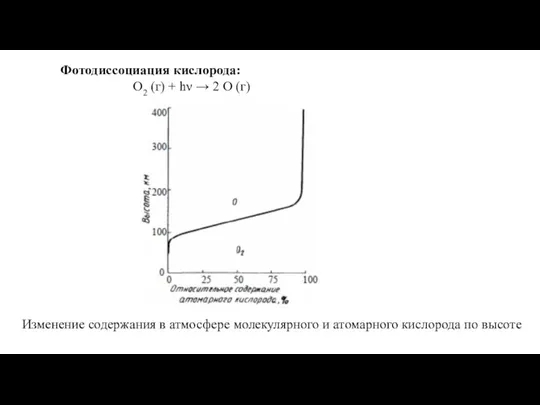 Фотодиссоциация кислорода
Фотодиссоциация кислорода Массовая доля элемента, 8 класс
Массовая доля элемента, 8 класс Фармаколого-фармакогностическое исследование биологически активных добавок, применяемых для похудения
Фармаколого-фармакогностическое исследование биологически активных добавок, применяемых для похудения Органические соединения углеводороды
Органические соединения углеводороды Иттрий-алюминиевый гранат и иттрий-алюминиевый перовскит
Иттрий-алюминиевый гранат и иттрий-алюминиевый перовскит Химические методы. CVD, СВС, термоциклирование вблизи температуры фазового перехода
Химические методы. CVD, СВС, термоциклирование вблизи температуры фазового перехода Химия. Электролитическая диссоциация. (9 класс)
Химия. Электролитическая диссоциация. (9 класс) Номенклатура и изомерия аренов
Номенклатура и изомерия аренов Презентация на тему Почему протекают химические реакции
Презентация на тему Почему протекают химические реакции  Природные и искусственные материалы. Естествознание 6 класс
Природные и искусственные материалы. Естествознание 6 класс Подготовка к олимпиаде по химии. Некоторые идеи составления и решения нестандартны задач
Подготовка к олимпиаде по химии. Некоторые идеи составления и решения нестандартны задач химия конеч 3.0
химия конеч 3.0 Решение расчетных задач на нахождение химической формулы вещества
Решение расчетных задач на нахождение химической формулы вещества 02. Классификация органических веществ
02. Классификация органических веществ Арены. Бензол
Арены. Бензол Пайданалылған майларды қолдана отырып көмірді брикеттер алу
Пайданалылған майларды қолдана отырып көмірді брикеттер алу Определение содержания витамина С в домашних условиях
Определение содержания витамина С в домашних условиях