Слайд 3Все элементы побочной подгруппы относятся к редким и рассеянным, практически не имеют

собственных руд, встречаются в виде полиметаллов, чаше всего с железом Fe(NbO3)2, Fe(TaO3)2. Получают электролизом расплавов соответствующих солей.
Физические свойства резко зависят от чистоты металла, так чистый ниобий имеет температуру плавления 1700оС, а с примесью углерода 2200оС. Тоже относится к пластичности и твердости.
Слайд 5Впервые ванадий был фактически открыт в 1781 г. профессором минералогии из Мехико

Андресом Мануэлем Дель Рио в свинцовых рудах. Он обнаружил новый металл и предложил для него название "панхромий" из-за широкого диапазона цвета его соединений, сменив затем на "эритроний". Дель Рио не имел авторитета в научном мире Европы, и европейские химики усомнились в его результатах. Затем и сам Дель Рио потерял уверенность в своём открытии и заявил, что открыл всего лишь хромат свинца.
В 1830 году ванадий был открыт заново шведским химиком Нильсом Сефстрёмом в железной руде. Новому элементу название дали Берцелиус и Сефстрём. Ванадий образует соединения с красивой окраской, отсюда и название элемента, связанное с именем скандинавской богини красоты Ванадис.
Слайд 7Нио́бий был открыт в 1801 г. английским учёным Ч. Хатчетом в минерале (колумбите), найденном в

бассейне р. Колумбии, и потому получил название «колумбий».
В 1844 г. немецкий химик Генрих Розе переименовал его в «ниобий» в честь дочери Тантала Ниобы, чем подчеркнул сходство между ниобием и танталом. Однако в некоторых странах (США, Англии) долго сохранялось первоначальное название элемента — колумбий, и только в 1950г. решением Международного союза чистой и прикладной химии (ИЮПАК, IUPAC) элементу окончательно было присвоено название ниобий.
Слайд 10Тантал открыт в 1802 г. шведским химиком А. Г. Экебергом в двух минералах, найденных в Финляндии и Швеции. В

последующем тантал и колумбий считали тождественными. Лишь в 1844 г. немецкий химик Розе доказал, что минерал колумбит содержит два различных элемента — ниобий и тантал.
Пластичный металлический тантал впервые получен немецким учёным В. Больтеном в 1903 г.
Элемент назван по имени героя древнегреческой мифологии Тантала, из-за трудностей его получения в чистом виде.
Слайд 11Химические свойства
Довольно инертные в химическом отношении элементы, взаимодействуют в виде порошков при

высоких температурах с кислородом, серой, углеродом, галогенами:
4V + 5O2 = 2V2O5
2Ta + 5Cl2 = 2TaCl5
2V + 3S = V2S3
Nb + C = NbC
В расплавленном состоянии хорошо адсорбируют водород и азот.
Слайд 12Очень устойчивы к агрессивным средам. Ванадий растворяется в концентрированной азотной кислоте и

царской водке, а на ниобий и тантал действует только смесь азотной и плавиковой кислот при длительном нагревании:
V + 5HNO3 = HVO3 + 5NO2 + 2H2O
3Nb + 5HNO3 + 18HF = 3H[NbF6] + 5NO + 10H2O
В щелочах не растворяются, но при окислительном сплавлении можно получить соли анионного типа:
2Nb + Na2CO3 + 5NaNO3 =
2NaNbO3 + CO2 + 5NaNO2
Слайд 13С кислородом образуют ряд оксидов следующих составов: VO, V2O3 - основного характера,VO2

- амфотерный, V2O5, Nb2O5, Ta2O5 - кислотного характера.
Металлический ниобий можно получить восстановлением его соединений, например хлорида ниобия или фтор-ниобата калия, при высокой температуре:
K2NbF7 + 5Na → Nb + 2KF + 5NaF
Соли ниобиевых кислот называют ниобатами. Их получают в результате обменных реакций после сплавления пятиокиси ниобия с содой:
Nb2O5 + 3Na2CO3 → 2Na3NbО4 + 3CO2
Слайд 14Довольно хорошо изучены соли нескольких ниобиевых кислот, в первую очередь метаниобиевой HNbO3,

а также диниобаты и пентаниобаты (K4Nb2O7, К7Nb5О16 · mH2O). А соли, в которых элемент №41 выступает как катион, обычно получают прямым взаимодействием простых веществ, например
2Nb + 5Cl2 → 2NbCl5
Ярко окрашенные игольчатые кристаллы пентагалогенидов ниобия (NbCl5 – желтого цвета, NbBr5 – пурпурно-красного) легко растворяются в органических растворителях – хлороформе, эфире, спирте. Но при растворении в воде эти соединения полностью разлагаются, гидролизуются с образованием ниобатов:
NbCl5 + 4Н2О → 5HCl + Н3NbO4
Гидролиз можно предотвратить, если в водный раствор добавить какую-либо сильную кислоту.
Слайд 15Применение эти элементы находят как легирующие добавки к высококачественным сталям. Тантал успешно

заменяет золото при изготовлении агрессивно стойкой химической посуды, в медицине.
Ниобиевые нити не вызывают раздражения живой ткани и хорошо сращиваются с ней. Восстановительная хирургия успешно использует такие нити для сшивания порванных сухожилий, кровеносных сосудов и даже нервов.














 Полимеры
Полимеры кристаллические решетки (2) (2)
кристаллические решетки (2) (2) Алканы. Строение и изомерия
Алканы. Строение и изомерия Строение атома
Строение атома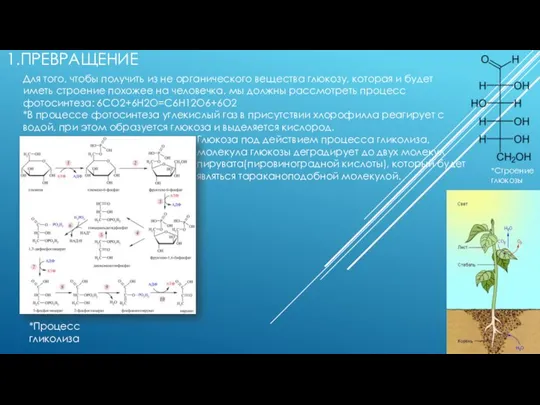 Превращение из не органического вещества в глюкозу
Превращение из не органического вещества в глюкозу Валентные возможности атомов элементов
Валентные возможности атомов элементов Презентация на тему Виды химической связи
Презентация на тему Виды химической связи  564481
564481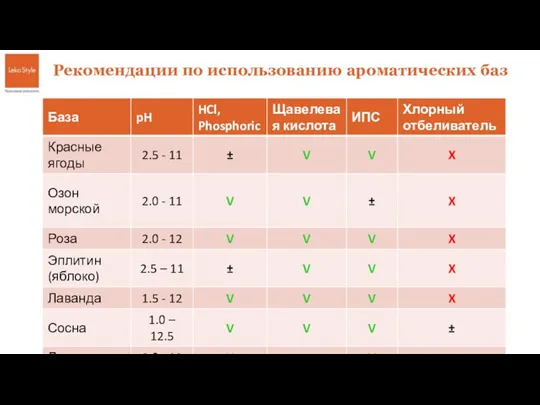 Базы для кислых и щелочных сред
Базы для кислых и щелочных сред Расчеты по химическим уравнениям реакций
Расчеты по химическим уравнениям реакций Строение вещества
Строение вещества Сложные неорганические вещества
Сложные неорганические вещества Чистые вещества и смеси
Чистые вещества и смеси Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона
Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона Реакции нуклеофильного присоединения с участием карбонильной группы
Реакции нуклеофильного присоединения с участием карбонильной группы Фармаколого-фармакогностическое исследование биологически активных добавок, применяемых для похудения
Фармаколого-фармакогностическое исследование биологически активных добавок, применяемых для похудения Классификация химических реакций
Классификация химических реакций Тренажер. Химические свойства солей
Тренажер. Химические свойства солей Изомерия, её виды
Изомерия, её виды Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Растворы
Растворы Химия — это наука о веществах, их свойствах и превращениях
Химия — это наука о веществах, их свойствах и превращениях Металлы. Кроссворд
Металлы. Кроссворд Твердые материалы для художественно-оформительских работ
Твердые материалы для художественно-оформительских работ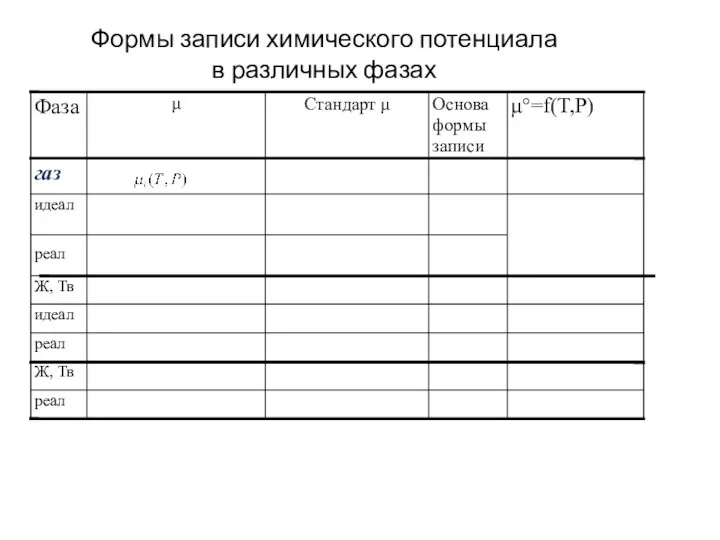 Формы записи химического потенциала в различных фазах
Формы записи химического потенциала в различных фазах Азот
Азот Плотность вещества
Плотность вещества Металлы II А подгруппы
Металлы II А подгруппы