Содержание
- 2. Лекция 4 Кулонометрия. Кулонометрическое титрование
- 3. Кулонометрия. Кулонометрическое титрование Кулонометрия - электрохимический метод анализа, основанный на измерении количества электричества Q, необходимого для
- 4. Разновидности Кулонометрии В зависимости от происходящих электродных процессов кулонометрические методы подразделяют на: прямую кулонометрию косвенную кулонометрию
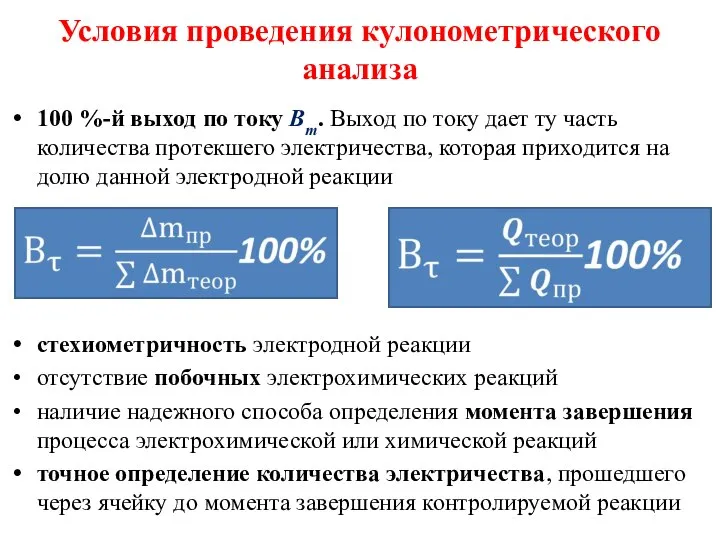
- 5. Условия проведения кулонометрического анализа 100 %-й выход по току Вт. Выход по току дает ту часть
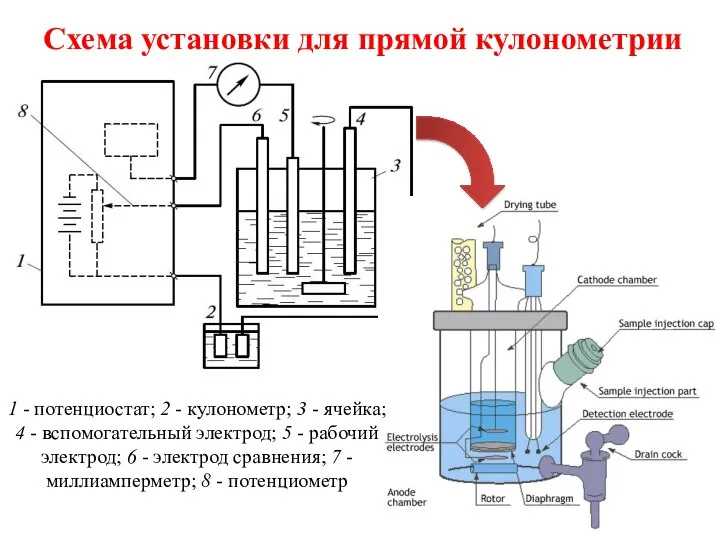
- 6. Схема установки для прямой кулонометрии 1 - потенциостат; 2 - кулонометр; 3 - ячейка; 4 -
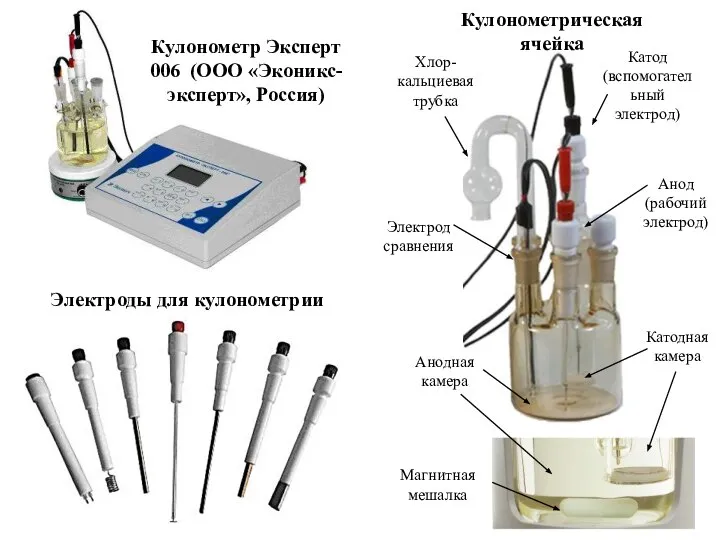
- 7. Кулонометр Эксперт 006 (ООО «Эконикс-эксперт», Россия) Кулонометрическая ячейка Магнитная мешалка Электроды для кулонометрии
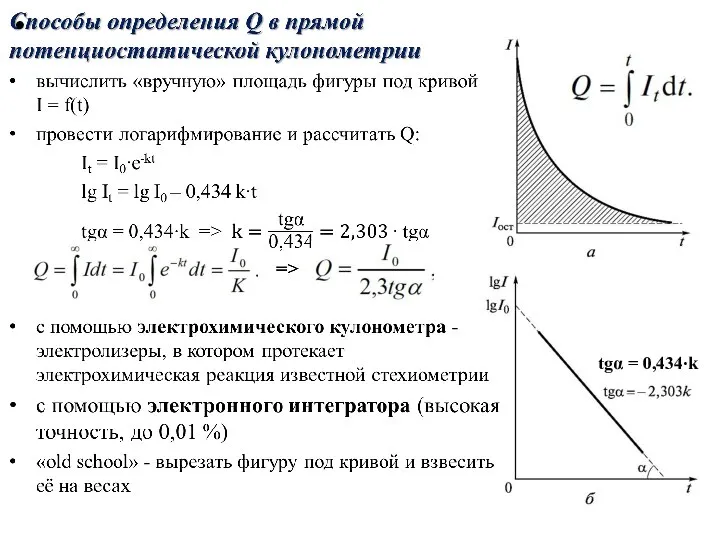
- 8. Прямая потенциостатическая кулонометрия E = const Выбор потенциала рабочего электрода проводят на основании кривых «сила тока-потенциал»
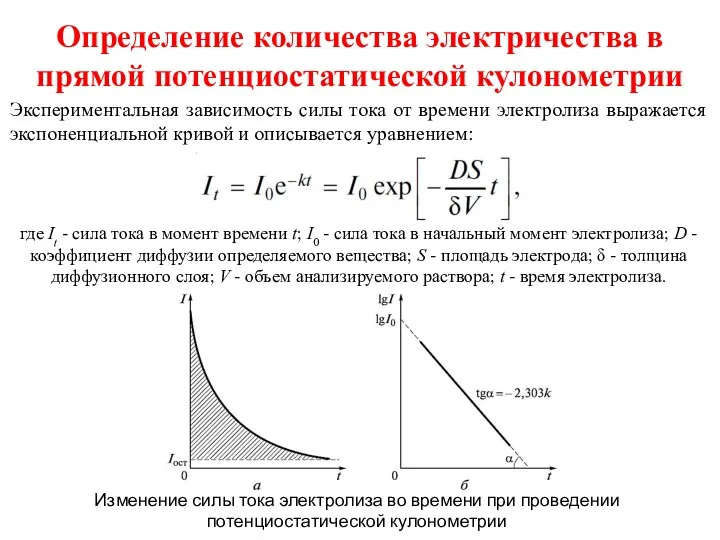
- 9. Определение количества электричества в прямой потенциостатической кулонометрии Экспериментальная зависимость силы тока от времени электролиза выражается экспоненциальной
- 10. tgα = 0,434∙k
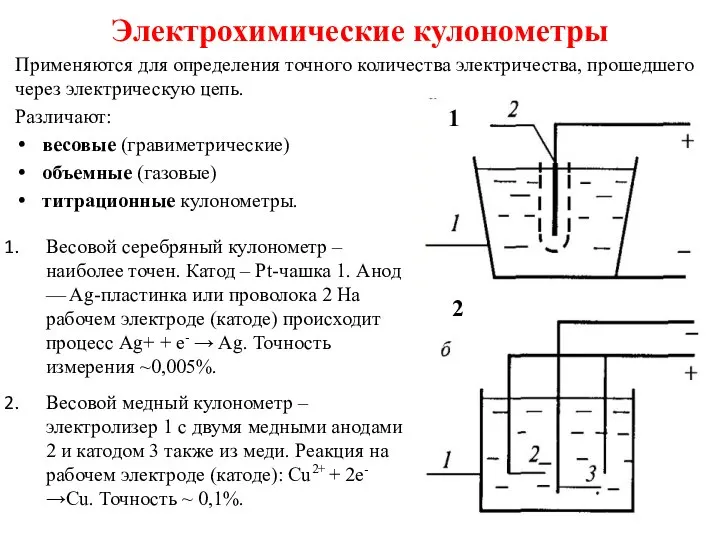
- 11. Электрохимические кулонометры Применяются для определения точного количества электричества, прошедшего через электрическую цепь. Различают: весовые (гравиметрические) объемные
- 12. Преимущества и области применения прямой потенциостатической кулонометрии Безэталонный (абсолютный) метод! Используется для определения растворенных веществ. Нижняя
- 13. Кулонометрическое титрование КТ - основано на взаимодействии определяемого вещества с титрантом, который получают электролизом; титрант в
- 14. Примеры генераторных реакций титранта в кулонометрическом титровании
- 15. Требования осуществления Кулонометрического титрования 100%-й выход по току при электрогенерации титранта быстрое колич. протекание химической реакции
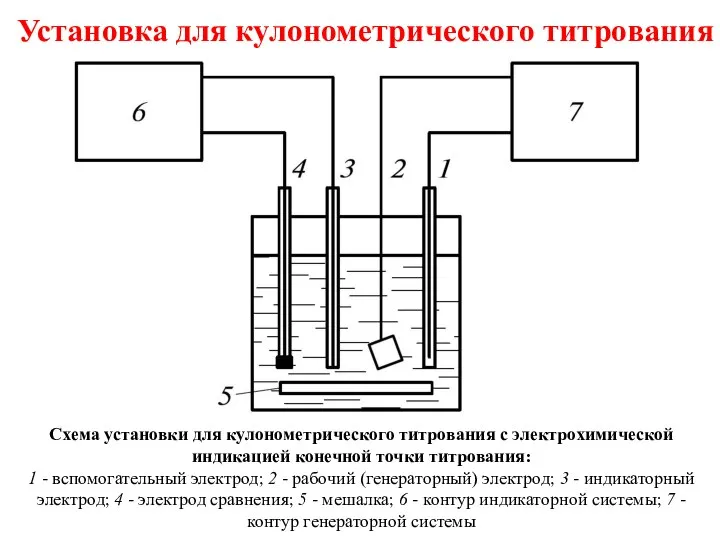
- 16. Установка для кулонометрического титрования Схема установки для кулонометрического титрования с электрохимической индикацией конечной точки титрования: 1
- 17. Способы индикации конечной точки тирования Визуальные индикаторные методы (крахмал, метиловый оранжевый, фенолфталеин и т.д.) Потенциометрический (Pt
- 18. Преимущества кулонометрического титрования Можно опр. очень малые количества в-в с большой точностью. Можно использ. нестойкие титранты
- 19. Примеры аналитического применения кулонометрического титрования
- 20. Кулонометрическое титрование воды по Фишеру (Карл Фишер, 1935 г.) Реактив Фишера: Спирт – ROH (метанол или
- 22. Скачать презентацию












 Неделя химии в МБОУ (викторина)
Неделя химии в МБОУ (викторина) Свойства основных липопротеинов (ЛП) плазмы крови
Свойства основных липопротеинов (ЛП) плазмы крови Углеводы
Углеводы Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9
Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9 Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Неметаллы в ПСХЭ
Неметаллы в ПСХЭ Органическая химия. Теория строения органических веществ
Органическая химия. Теория строения органических веществ Строение атома
Строение атома Презентация 1
Презентация 1 Теория активированного комплекса
Теория активированного комплекса Строение атома
Строение атома Кислоты в химии
Кислоты в химии Природные источники углеводородов
Природные источники углеводородов Природные кислоты и щелочи. Индикаторы
Природные кислоты и щелочи. Индикаторы Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа
Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа Химическая технология. Структура ВКР
Химическая технология. Структура ВКР Интеллектуальная игра по химии «Металлы»
Интеллектуальная игра по химии «Металлы» Аминокислоты и их применение
Аминокислоты и их применение Углеволокно (карбон)
Углеволокно (карбон) Спирты (алканолы)
Спирты (алканолы) Дисперсные системы в пищевой промышленности
Дисперсные системы в пищевой промышленности Фосфор
Фосфор Пересчет данных анализа, выраженных в ионной форме
Пересчет данных анализа, выраженных в ионной форме Степень окисления. Составление формул бинарных соединений
Степень окисления. Составление формул бинарных соединений Металлы тоже воевали… 8 класс
Металлы тоже воевали… 8 класс Презентация на тему Серебро
Презентация на тему Серебро  Классификация химических реакций
Классификация химических реакций Sinteticheskie_Materialy_I_Ikh_Rol_1
Sinteticheskie_Materialy_I_Ikh_Rol_1