Содержание
- 2. Гидролиз – это обменная реакция между химическим соединением и водой, приводящая к разложению водой исходного вещества.
- 3. Пожалуй, начнем с повторения: Какие процессы являются необратимыми? Какие вещества относят к слабым электролитам? Что такое
- 4. Рассмотрим разные случаи гидролиза
- 5. NO2 K+ OH- H + [ ]- Гидролиз по аниону Каким основанием и какой кислотой (с
- 6. KNO2 + H2O K+ + NO2- + H2O K+ + OH- + HNO2↑ NO2- + H2O
- 7. SO42- H+ [ ]+ Zn 2+ OH - Гидролиз по катиону Каким основанием и какой кислотой
- 8. При протекании первой ступени гидролиза соли многокислотного основания ион цинка вошел в состав более сложного катиона
- 9. (ZnOH)2SO4 + H2O Zn(OH)2 + H2SO4 2ZnOH+ + SO42- + 2H2O 2Zn(OH)2 + 2H+ + SO42-
- 10. Al2S3 H2O + Al(OH)3 + H2S 2 3 6 Гидролиз по катиону и аниону Чем принципиально
- 11. А какой случай стоит еще попробовать?
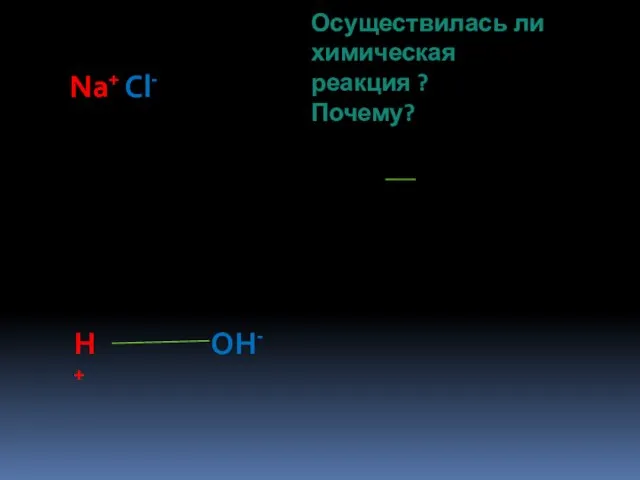
- 12. Na+ Cl- H+ OH- Осуществилась ли химическая реакция ? Почему?
- 13. Можно ли усилить гидролиз? Да, нагреванием. Посмотрим эксперимент: Усиление гидролиза солей при нагревании раствора
- 14. Выводы: Определение гидролиза солей: Взаимодействие в водных растворах катионов и (или) анионов солей с молекулами воды,
- 15. Типы гидролиза: по катиону; по аниону; по катиону и по аниону Выводы:
- 16. Выводы: С точки зрения обратимости: Соли многоосновных кислот и многокислотных оснований диссоциируют Каждая последующая ступень гидролиза
- 17. соли, образованные сильным основанием и слабой кислотой соли, образованные слабым основанием и сильной кислотой соли, образованные
- 18. Кроссворд Заполни пробелы в предложении Найди соответствия
- 19. ИНДИКАТОРЫ (от лат. indicator — указатель) — вещества, позволяющие следить за составом среды или за протеканием
- 20. К слабым электролитам относятся: почти все органические кислоты (CH3COOH, C2H5COOH и др.); некоторые неорганические кислоты (H2CO3,
- 22. Скачать презентацию



![NO2 K+ OH- H + [ ]- Гидролиз по аниону Каким основанием](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/889537/slide-4.jpg)

![SO42- H+ [ ]+ Zn 2+ OH - Гидролиз по катиону Каким](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/889537/slide-6.jpg)












 Метаболизм азота
Метаболизм азота Важнейшие классы неорганических соединений. Соли
Важнейшие классы неорганических соединений. Соли Термохимия. Задания
Термохимия. Задания Кислоты. Классификация. Номенклатура
Кислоты. Классификация. Номенклатура 9-12 Гидролиз солей -
9-12 Гидролиз солей - Получение метанола из синтез-газа
Получение метанола из синтез-газа Предмет органической химии
Предмет органической химии Альдегиды и кетоны
Альдегиды и кетоны Железоуглеродистые сплавы. Диаграмма равновесного состояния железо-цементит. Фазы и структурные составляющие
Железоуглеродистые сплавы. Диаграмма равновесного состояния железо-цементит. Фазы и структурные составляющие Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Альдегиды и кетоны
Альдегиды и кетоны Сахароза (С12Н22О11)
Сахароза (С12Н22О11) Классификация реакций в органической химии
Классификация реакций в органической химии Комплексные соединения
Комплексные соединения Презентация на тему Основания и их классификация
Презентация на тему Основания и их классификация 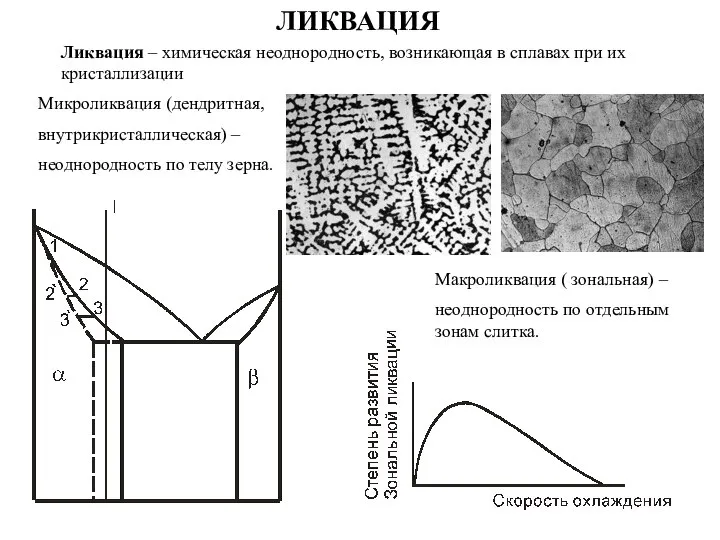 Ликвация. Микроликвация
Ликвация. Микроликвация Синтез-газ
Синтез-газ Реакции замещения
Реакции замещения Синтез 7,7 - дихлоробицикло [4.1.0] гептана
Синтез 7,7 - дихлоробицикло [4.1.0] гептана Углерод и его аллотропные модификации. Органическая химия - химия углерода
Углерод и его аллотропные модификации. Органическая химия - химия углерода Использование элементов модульной технологии на уроках химии
Использование элементов модульной технологии на уроках химии Физические свойства водорода
Физические свойства водорода Презентация на тему Витамины. Урок химии 10 класс
Презентация на тему Витамины. Урок химии 10 класс  Алюминий
Алюминий Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Презентация по Химии "Ковалентная химическая связь"
Презентация по Химии "Ковалентная химическая связь"  Презентация на тему Изотопы
Презентация на тему Изотопы  Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса
Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса